
| A. | CO2 H2O | B. | C2H4 CH4 | C. | Cl2 CH4 | D. | NH3 HCl |
分析 非极性键为:同种元素的原子间形成的共价键;极性键为:不同元素的原子间形成的共价键;
极性分子为:正电荷中心和负电荷中心不相重合的分子;非极性分子:正电荷中心和负电荷中心相重合的分子;分子极性的判断方法为:分子的极性由共价键的极性及分子的空间构型两个方面共同决定,据此分析.
解答 解:A.二氧化碳为极性键形成的非极性分子,水的分子空间构型为V形,为极性键形成的极性分子,故A错误;
B.C2H4 CH4中化学键都是不同元素构成的,属于极性键;二者分子中正电荷中心和负电荷中心相重合,属于非极性分子,故B正确;
C.Cl2中只含有非极性键,为非极性分子;甲烷为极性键形成的非极性分子,故C错误;
D.氨气和氯化氢都是由极性键形成的分子,二者正电荷中心和负电荷中心不相重合,属于极性分子,故D错误;
故选B.
点评 本题考查了键的极性和分子的极性判断,题目难度不大,侧重于对学生灵活运用基础知识解决实际问题的能力的培养.


科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ②③ | C. | ①③ | D. | ②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲烷在点燃前需进行验纯 | |
| B. | 甲烷能使酸性高锰酸钾溶液褪色 | |
| C. | 甲烷的一氯代物只有一种结构证明甲烷是正四面体结构而非平面正方形结构 | |
| D. | 甲烷不能发生氧化反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
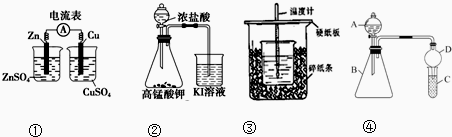
| A. | 装置①:检验电流的方向 | |
| B. | 装置②:探究氧化性:KMnO4>Cl2>I2 | |
| C. | 装置③:测定中和热 | |
| D. | 装置④:A、B、C中分别加入HCl、Na2CO3、Na2SiO3判断Cl、C、Si的非金属性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 增加CO的量 | B. | 增大压强 | C. | 升高温度 | D. | 加入稀有气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SiH4的空间构型是正四面体 | |
| B. | 在NH4+和[Cu(NH3)4]2+中都存在配位键 | |
| C. | 原子晶体中原子以共价键结合,具有键能大、硬度大的特性 | |
| D. | SO2、SO3都是极性分子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 叙述 | 评价 |
| A | 乙酸乙酯在H218O中水解,产物乙醇中将含有18O | 错,根据酯的水解规律,产物乙酸中将含有18O同位素,而乙醇则没有 |
| B | 淀粉与20%的硫酸混合液在沸水浴中充分加热后滴加碘水无蓝色现象,则说明淀粉水解完全 | 错,淀粉水解后未加碱中和至溶液呈碱性 |
| C | 溴乙烷与NaOH溶液共热充分反应后,再加入AgNO3溶液,能观察到浅黄色沉淀 | 对,溴乙烷水解产生了溴离子 |
| D | 可以用新制的Cu(OH)2悬浊液鉴别乙醇溶液、乙酸溶液和葡萄糖溶液 | 错,用新制的Cu(OH)2悬浊液鉴别乙醇溶液和乙酸溶液 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
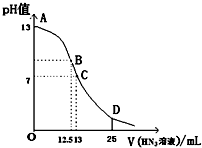 纯的叠氮酸(HN3)是无色液体,常用做引爆剂,常温下向25mL 0.1mol•L-1NaOH溶液中加入0.2mol•L-1HN3的溶液,滴加过程中的pH值的变化曲线(溶液混合时的体积变化忽略不计)如图.下列说法正确的是( )
纯的叠氮酸(HN3)是无色液体,常用做引爆剂,常温下向25mL 0.1mol•L-1NaOH溶液中加入0.2mol•L-1HN3的溶液,滴加过程中的pH值的变化曲线(溶液混合时的体积变化忽略不计)如图.下列说法正确的是( )| A. | 若用已知浓度的NaOH溶液滴定HN3溶液来测定HN3的浓度时应用甲基橙作指示剂 | |
| B. | 常温下,向0.2mol•L-1HN3的溶液中加水稀释,则 $\frac{c({{N}_{3}}^{-})}{c(O{H}^{-})•c(H{N}_{3})}$不变 | |
| C. | 分别中和PH均为4的HN3溶液和HCl溶液,消耗0.1mol•L-1NaOH溶液的体积相同 | |
| D. | D点时溶液中离子浓度存在如下关系:c(H+)+c(HN3)=c(N3-)+c(OH-) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com