
1下列说法正确的是( )
A.若NaA、NaB溶液的pH分别为9和8,则酸性一定是HA<HB;
B. CH3COONa水解产生CH3COOH和OH-,向水解液中加入少量冰醋酸会因其中和OH-而使水解平衡右移;
C.中和pH和体积均相同的盐酸和醋酸溶液,消耗NaOH的物质的量相同
D.因Al3++3H2O 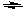 Al(OH)3+3H+,为抑制水解,配制AlCl3溶液时需将AlCl3溶解在稀盐酸中;
Al(OH)3+3H+,为抑制水解,配制AlCl3溶液时需将AlCl3溶解在稀盐酸中;
科目:高中化学 来源: 题型:
下列离子方程式书写正确的是( )
A.向NaHSO4溶液加入Ba(OH)2溶液至中性:H++SO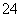 +Ba2++OH-===BaSO4↓+H2O
+Ba2++OH-===BaSO4↓+H2O
B.已知Ka(HClO)>Ka2(H2CO3),则有:2ClO-+CO2(少量)+H2O===CO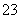 +2HClO
+2HClO
C.金溶于王水生成AuCl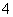 离子和NO:Au+4H++4Cl-+NO
离子和NO:Au+4H++4Cl-+NO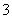 ===AuCl
===AuCl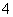 +NO↑+2H2O
+NO↑+2H2O
D.酸性条件下碘酸钾溶液与碘化钾溶液发生反应生成碘单质:IO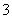 +5I-+3H2O===3I2+6OH-
+5I-+3H2O===3I2+6OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
如图是在一定温度下,向不同电解质溶液中加入新物质时溶液的导电性能发生变化,其电流强度(I)随新物质加入量(m)的变化曲线,以下四个导电性实验,其中与A图变化趋势一致的是__________,与B图变化趋势一致的是__________,与C图变化趋势一致的是________。
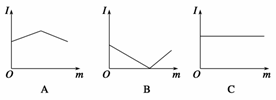
①氢氧化钡溶液中滴入硫酸溶液至过量;
②醋酸溶液中滴入氨水至过量;
③澄清石灰水中通入CO2至过量;
④氯化铵溶液中逐渐加入适量氢氧化钠固体。
查看答案和解析>>
科目:高中化学 来源: 题型:
3t℃时,水的离子积为 Kw,该温度下将a mol/L一元酸HA与b mol/L一元碱 BOH等体积混合,若混合后溶液呈中性,下列说法一定正确的是( )
A.混合液中,=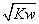 B.混合液的pH=7
B.混合液的pH=7
C.a=b D.混合液中,c(B+)=c(A-)+c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
混合下列各组物质使之充分反应,加热蒸干产物并在300 ℃灼烧至质量不变,最终残留固体不是纯净物的是( )。
A.向红褐色的Fe(OH)3固体中加入过量盐酸
B.等物质的量浓度、等体积的(NH4)2SO4与BaCl2溶液
C.等物质的量的NaHCO3与Na2O2固体
D.向NaBr溶液中通入过量氯气
查看答案和解析>>
科目:高中化学 来源: 题型:
NH4Cl溶于重水(D2O)生成一水合氨和水合氢离子的化学式是( )
A.NH3·D2O和HD2O+ B.NH3·HDO和D3O+ C.NH2D·D2O和DH2O+ D.NH2D·HDO和D3O+
查看答案和解析>>
科目:高中化学 来源: 题型:
在常温下,下列五种溶液:①0.1 mol·L-1 NH4Cl ②0.1 mol·L-1 CH3COONH4
③0.1 mol·L-1 NH4HSO4 ④0.1 mol·L-1 NH3·H2O和0.1 mol·L-1 NH4Cl混合液
⑤0.1 mol·L-1 NH3·H2O。
请根据要求填写下列空白:
(1)溶液①呈________性(填“酸”、“碱”或“中”),其原因是________________________(用离子方程式表示)。
(2)在上述五种溶液中,pH最小的是________;c(NH )最小的是________(填序号)。
)最小的是________(填序号)。
(3)比较溶液②、③中c(NH )的大小关系是②________③(填“>”“<”或“=”)。
)的大小关系是②________③(填“>”“<”或“=”)。
(4)在溶液④中,__________的浓度为0.1 mol·L-1;NH3·H2O和__________的物质的量浓度之和为0.2 mol·L-1。
(5)常温下,测得溶液②的pH=7,则说明CH3COO-的水解程度________(填“>”“<”或“=”)NH 的水解程度,CH3COO-与NH
的水解程度,CH3COO-与NH 浓度的大小关系是:c(CH3COO-)________c(NH
浓度的大小关系是:c(CH3COO-)________c(NH )(填“>”“<”或“=”)。
)(填“>”“<”或“=”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
硫酸铜在生产、生活中应用广泛。某化工厂用含少量铁的废铜渣为原料生产胆矾的流程如下:
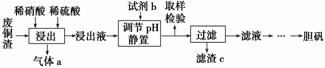
(1)写出浸出时铜与稀硫酸、稀硝酸反应生成硫酸铜的化学方程式:________________。
(2)取样检验是为了确认Fe3+是否除净,你的检验方法是____________。
(3)滤渣c是__________。
(4)气体a可以被循环利用,用化学方程式表示气体a被循环利用的原理为2NO+O2===2NO2、____________。
(5)一定温度下,硫酸铜受热分解生成CuO、SO2气体、SO3气体和O2气体,且n(SO3)∶n(SO2)=1∶2,写出硫酸铜受热分解的化学方程式:________________。
某同学设计了如下图所示的实验装置分别测定生成的SO2、SO3气体的质量和O2气体的体积。此设计有不合理之处,请说明理由:______________。
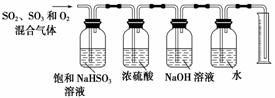
查看答案和解析>>
科目:高中化学 来源: 题型:
某硫酸镁和硫酸铝的混合溶液中,c(Mg2+)=2 mol·L-1,c(SO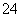 )=6.5 mol·L-1,若将200 mL此混合液中的Mg2+和Al3+ 分离,至少应加入1.6 mol·L-1的苛性钠溶液( )
)=6.5 mol·L-1,若将200 mL此混合液中的Mg2+和Al3+ 分离,至少应加入1.6 mol·L-1的苛性钠溶液( )
A.0.5 L B.1.625 L
C.1.8 L D.2 L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com