
| A���ﵽ��ѧƽ��ʱ��N2����ȫת��ΪNH3 |
| B���ﵽ��ѧƽ��ʱ��N2��H2�� NH3�����ʵ���Ũ�Ȳ�һ����� |
| C����������������ѹǿ��ƽ��������Ӧ�����ƶ���ƽ�ⳣ������ |
| D��������1 mol N2ͬʱ������ 2 mol NH3 ʱ���÷�Ӧ�ﵽƽ��״̬ |


 ʱ�����������ҵԭ���ܳ�����ϵ�д�
ʱ�����������ҵԭ���ܳ�����ϵ�д� ����νӽ̲���ĩ���Ԥϰ�人������ϵ�д�
����νӽ̲���ĩ���Ԥϰ�人������ϵ�д� ������ҵ��ٳɳ����½������������ϵ�д�
������ҵ��ٳɳ����½������������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��CH3COOH�ĵ���ƽ�ⳣ������Ϊԭ����10�� |
| B��CH3COO-��CH3COOH��Ũ��֮������Ϊԭ����10�� |
| C��CH3COO-��H+��Ũ��֮����СΪԭ����0.1 |
| D��CH3COOH��CH3COO-��Ũ��֮�ͼ�СΪԭ����0.1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��0.5mol/L��MgCl2��Һ�У�����Cl- ����Ϊ1 NA |
| B����״���£�22.4LH2O���еķ�����Ϊ1 NA |
| C��5.6g��Fe�����������ᷴӦʱ��ʧȥ�ĵ�����Ϊ0.2 NA |
| D�����³�ѹ�£�1.06g Na2CO3���е�Na+������Ϊ0.02 NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A������1molFeCl3����Һ�����ˮ�У����Ƶõ�Fe��OH��3��������ΪNA |
| B����״���£�22.4LSO3���еķ�����ΪNA |
| C��1mol���������к��е�Si-O����ĿΪ2NA |
| D��16.9 g BaO2��������������������Ϊ0.2NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��ϡ���������Ƭ�ϣ�2Fe+6H+=2Fe3++3H2�� |
| B��̼��������Һ��ϡ�����ϣ�HCO3-+H+=H20+C02�� |
| C������ͭ��Һ������������Һ��ϣ�CuS04+20H-=Cu��OH��2��+SO42- |
| D����������Һ���Ȼ�����Һ��ϣ�AgN03+C1-=AgCl��+NO3- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��Na2CO3 |
| B��KOH |
| C��Fe2��SO4��3 |
| D��KHCO3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
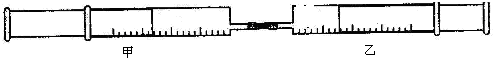
| ʵ����� | ����Ͳ������ | ����Ͳ������ | ����Ͳ���� |
| 1 | 10mlFeSO4 | 10mlNH3 | ���ɰ�ɫ���������ɫ |
| 2 | 15mlCl2 | 40mlNH3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��Na+��Cu2+��NO3-��Cl- |
| B��Na+��Zn2+��OH-��Br- |
| C��K+��SO42-��Cl-��Mg2+ |
| D��Ba2+��Na+��OH-��CO32- |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com