
(15分) 化合物A和B都是重要的化工原料。B和E都能与FeCl3溶液发生显色反应,B、C、D结构中都有两个化学环境完全相同的甲基,B中苯环上的一硝基取代物只有两种。X是石油裂解的主要产物,通过质谱法测得其相对分子质量为42。
已知:

请回答下列问题:
(1)下列叙述正确的是______。
a.化合物Y能使酸性高锰酸钾溶液褪色
b.化合物X的结构简式为CH2=CHCH3
c.化合物C、D互为同系物
d.A与NaOH溶液反应,理论上1 mol A最多消耗2 mol NaOH
(2)X→Y的反应类型是______,化合物B的结构简式是________,化合物C的结构简式是________。
(3)写出Y→D + E的化学方程式____________________________。
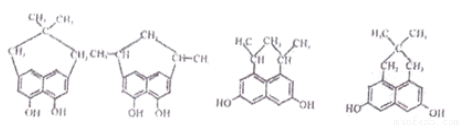
(4)写出同时满足下列条件的B的两种同分异构体的结构简式(不考虑立体异构) 。
a.有两个化学环境相同的甲基,含稠环芳烃的结构单元
b.苯环上的一硝基取代物只有两种,遇FeCl3溶液显色
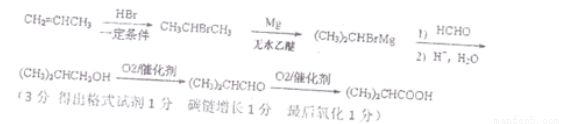
(5)以X和甲醛为原料合成化合物C,请设计合成路线(无机试剂及溶剂任选)。
注:合成路线参照如下示例流程图:

(1)ab;(2)加成反应,  ,(CH3)2CHCOOH 。
,(CH3)2CHCOOH 。
(3) 。
。
(4) 。
。
(5)
【解析】
试题分析:根据题给信息和工艺流程图知,X是石油裂解的主要产物,通过质谱法测得其相对分子质量为42,可知X为丙烯;丙烯和苯发生加成反应生成Y异丙苯。E能与FeCl3溶液发生显色反应,结合分子式C6H6O可知,E为苯酚;D结构中都有两个化学环境完全相同的甲基,结合D的分子式C3H6O和Y的结构可知D为丙酮;B能与FeCl3溶液发生显色反应可知B中含有酚羟基,B结构中都有两个化学环境完全相同的甲基,B中苯环上的一硝基取代物只有两种,结合B的分子式可知,B结构简式为: ;A为酯,在碱性环境中水解再酸化得C应为酸,结合X的结构及C结构中都有两个化学环境完全相同的甲基,C的结构简式为(CH3)2CHCOOH。(1)a、Y为异丙苯,其中与苯环相连的碳原子上有氢原子,可以被酸性高锰酸钾氧化,正确;b、X是丙烯,结构简式为CH2=CHCH3,正确;c、C为3—甲基丙酸,D为丙酮,不是同系物,错误;d、由A水解生成B、C的结构可知,含有2mol酚羟基,2mol羧基,应消耗4molNaOH,错误;选ab;(2)X→Y的反应类型是加成反应,化合物B的结构简式是
;A为酯,在碱性环境中水解再酸化得C应为酸,结合X的结构及C结构中都有两个化学环境完全相同的甲基,C的结构简式为(CH3)2CHCOOH。(1)a、Y为异丙苯,其中与苯环相连的碳原子上有氢原子,可以被酸性高锰酸钾氧化,正确;b、X是丙烯,结构简式为CH2=CHCH3,正确;c、C为3—甲基丙酸,D为丙酮,不是同系物,错误;d、由A水解生成B、C的结构可知,含有2mol酚羟基,2mol羧基,应消耗4molNaOH,错误;选ab;(2)X→Y的反应类型是加成反应,化合物B的结构简式是 ,化合物C的结构简式是(CH3)2CHCOOH 。(3)根据上述分析和题给信息知,Y→D + E的化学方程式为
,化合物C的结构简式是(CH3)2CHCOOH 。(3)根据上述分析和题给信息知,Y→D + E的化学方程式为
 。
。
(4)B为 ,符合a.有两个化学环境相同的甲基,含稠环芳烃的结构单元,b.苯环上的一硝基取代物只有两种,苯环上有两种氢原子,遇FeCl3溶液显色,有酚羟基,同分异构体的结构简式为
,符合a.有两个化学环境相同的甲基,含稠环芳烃的结构单元,b.苯环上的一硝基取代物只有两种,苯环上有两种氢原子,遇FeCl3溶液显色,有酚羟基,同分异构体的结构简式为 ,共4种。
,共4种。
(5)X为丙烯,C为(CH3)2CHCOOH,结合提示,可设计成以下合成路线:

考点:考查有机合成与有机综合推断,涉及反应类型的判断,结构简式、化学方程式及同分异构体的书写,有机合成路线的设计。


 字词句篇与同步作文达标系列答案
字词句篇与同步作文达标系列答案科目:高中化学 来源:2013-2014湖北省大冶市春季期末考试高二化学试卷(解析版) 题型:填空题
(15分)
(1)纳米技术制成的金属燃料、非金属固体燃料、氢气等已应用到社会生活和高科技领域。单位质量的A和B单质燃烧时均放出大量热,可用作燃料。已知A和B为短周期元素,其原子的第一至第四电离能如下表所示:
电离能(kJ/mol) | I1 | I2 | I3 | I4 |
A | 932 | 1821 | 15390 | 21771 |
B | 738 | 1541 | 7733 | 10540 |
①某同学根据上述信息,推断B的核外电子排布如下图所示,该同学所画的电子排布图违背了 ,B元素位于周期表五个区域中的 _______区。

②ACl2分子中A的杂化类型为 ,ACl2的空间构型为 。
(2)Fe原子或离子外围有较多能量相近的空轨道能与一些分子或离子形成配合物。
①与Fe原子或离子形成配合物的分子或离子应具备的结构特征是 。
②六氰合亚铁离子[Fe(CN)6]4—中不存在 。
A共价键 B非极性键 C配位键 D.σ键 E.π键
③写出一种与 CN—互为等电子体的单质分子式 。
(3)一种Al-Fe合金的立体晶胞如下图所示。请据此回答下列问题:
①确定该合金的化学式 。
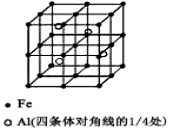
②若晶体的密度=ρ g/cm3,则此合金中最近的两个Fe原子之间的距离(用含ρ的代数式表示,不必化简)为 cm。
查看答案和解析>>
科目:高中化学 来源:2013-2014湖北省四校下学期期中考试高一化学试卷(解析版) 题型:选择题
下列说法正确的是
A.流水、风力是一次能源,电力、蒸汽是二次能源
B.普通锌锰电池是一次电池,碱性锌锰电池是二次电池
C.同周期元素形成的简单离子中,原子序数越大的离子半径越小
D.原子核外电子层数越多,原子半径一定越大
查看答案和解析>>
科目:高中化学 来源:2013-2014海口市第二学期高二化学期中考试(B卷)试卷(解析版) 题型:选择题
皮肤上沾了少量苯酚,正确的处理方法是( )
A.先用稀NaOH溶液洗,再用水冲洗 B.先用水洗,再用酒精冲洗
C.先用酒精洗,再用水冲洗 D.用布擦去后再用水冲洗
查看答案和解析>>
科目:高中化学 来源:2013-2014浙江省绍兴市柯桥区高三第二次模拟考试理综化学试卷(解析版) 题型:选择题
如图是甲醇/过氧化氢燃料电池内部结构示意图。 工作时,甲醇和过氧化氢分别进入燃料电池的燃料腔和氧化剂腔,在各自催化剂的作用下发生反应,并向外界输出电能。下列说法不正确的是

A.该电池的正极反应式:H2O2+2H++2e—=2H2O
B.燃料腔中的多孔石墨电极为该燃料电池的负极,负极产生的H+ 通过质子交换膜流向正极
C.电池工作时,1 mol甲醇被氧化有6 mol电子转移
D.电路中的电子经正极、负极、质子交换膜后再回到正极,形成闭合回路
查看答案和解析>>
科目:高中化学 来源:2013-2014浙江省高三下学期联考理综化学试卷(解析版) 题型:选择题
下列说正确的是
【已知:HClO的Ka=3.0×l0-8;H2CO3的Ka1= 4.3×l0-7,Ka2=5.6×l0-11;Ksp(BaSO4)= 1.1 ×10-10;Ksp(BaCO3)= 5.1 ×10-9】
A.相同条件下,pH相同的NaClO和Na2CO3溶液,物质的量浓度前者小于后者
B.常温下,将CH3COONa溶液和稀盐酸混合至溶液pH=7时:
c(Na+)>c(CH3COO-)>c(Cl-) >c(CH3COOH)>c(H+)=c(OH-)
C.向饱和Na2CO3溶液中通入足量的CO2,溶液变浑浊,由此证明了NaHCO3溶解度比Na2CO3小
D.氯碱工业使用的食盐水需先除去其中的Ca2+、Mg2+、SO42-等杂质。除杂时,粗盐水中可先加入过量的BaCl2溶液,至沉淀不再产生后,再加入过量的Na2CO3和NaOH,充分反应后滤去沉淀,所得滤液中仍含有一定量的SO42-
查看答案和解析>>
科目:高中化学 来源:2013-2014浙江省湖州市高三二模理综化学试卷(解析版) 题型:实验题
(15分)乙酰苯胺是一种白色有光泽片状结晶或白色结晶粉末,是磺胺类药物的原料,可用作止痛剂、退热剂、防腐剂和染料中间体。
乙酰苯胺的制备原理为: 
实验参数:
名称 | 式量 | 性状 | 密度/g/cm3 | 沸点/℃ | 溶解度 | |
苯 胺 | 93 | 无色油状液体, 具有还原性 | 1.02 | 184.4 | 微溶于水 | 易溶于乙醇、乙醚等 |
乙 酸 | 60 | 无色液体 | 1.05 | 118.1 | 易溶于水 | 易溶于乙醇、乙醚 |
乙酰苯胺 | 135 | 白色晶体 | 1.22 | 304 | 微溶于冷水,溶于热水 | 易溶于乙醇、乙醚 |
实验装置:(见右图)
注:刺形分馏柱的作用相当于二次蒸馏,用于沸点差别不太大的混合物的分离
实验步骤:
步聚1:在100ml圆底烧瓶中加入无水苯胺9.1mL,冰醋酸17.4mL,锌粉0.1g,安装仪器,加入沸石,给反应器均匀加热,使反应液在微沸状态下回流,
调节加热温度,使柱顶温度控制在105℃左右,反应约60~80min,反应生成的水及少量醋酸被蒸出,当反应基本完成时,停止加热。
步聚2: 在搅拌下,趁热将烧瓶中的物料以细流状倒入盛有100mL冰水的烧杯中,剧烈搅拌,并冷却烧杯至室温,粗乙酰苯胺结晶析出,抽滤、洗涤、干燥,得到乙酰苯胺粗品。
步聚3: 将此粗乙酰苯胺进行重结晶,待结晶完全后抽滤,尽量压干滤饼。产品放在干净的表面皿中晾干,称重,计算产率。
请回答下列问题:
(1)实验中加入锌粉的目的是
(2)为何要控制分馏柱上端的温度在105?C左右
(3)通过什么现象可判断反应基本完成
(4)步聚1加热可用 (填“水浴”或“油浴”),步聚2中结晶时,若冷却后仍无晶体析出,可采用的方法是 。
(5)洗涤乙酰苯胺粗品最合适的试剂是 。
A. 用少量冷水洗 B. 用少量热水洗
C. 先用冷水洗,再用热水洗 D. 用酒精洗
(6)该实验最终得到纯品8.1克,则乙酰苯胺的产率是 。
查看答案和解析>>
科目:高中化学 来源:2013-2014浙江省温州市业水平考试适应性测试化学试卷(解析版) 题型:选择题
W、X、Y、Z是原子序数依次增大的同一短周期元素,W、X是金属元素,Y、Z是非金属元素。W、X各自的最高价氧化物对应的水化物可以反应生成盐和水,W与Y可形成化合物W2Y。下列说法不正确的是
A.W2Y为离子化合物
B.X的硝酸盐水溶液显酸性
C.这四种元素对应的简单离子半径最大的是Y离子
D.Z单质的水溶液通入Y的低价氧化物,溶液的pH 增大
查看答案和解析>>
科目:高中化学 来源:2013-2014浙江省高二下学期期中化学试卷(解析版) 题型:选择题
三位科学家因在烯烃复分解反应研究中的杰出贡献而荣获2005年度诺贝尔化学奖,烯烃复分解反应可示意如下:
下列化合物中,经过烯烃复分解反应可以生成 的是 ( )
的是 ( )

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com