
| 实验编号 | 样品和辅助试剂 | 消耗盐酸体积(mL) |
| 1 | 10.00mL溶液、0.2g催化剂、20mL浓硫酸 | 33.45 |
| 2 | 10.00mL溶液、0.2g催化剂、20mL浓硫酸 | 33.90 |
| 3 | 10.00mL溶液、0.2g催化剂、20mL浓硫酸 | 33.50 |
| 4 | x |
| 级别 | 优等品 | 一等品 | 合格品 |
| 总尿素含量%≥ | 46.4 | 46.2 | 46.0 |
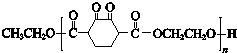
分析 (1)滴加盐酸(NH4)2B4O7转化为H3BO3,硼的化合价未变化,发生类似复分解反应,还有氯化铵生成;
(2)用水蒸气将NH3吹出,所以加热圆底烧瓶产生水蒸气,进入试管中将生成的氨气吹出;加热产生水蒸气,装置内压强增加,防止装置中压力过大而发生危险,冷却时防止发生倒吸,起安全管作用;
(3)依据编号1、2、3分析可知编号为4的实验应加入的样品和辅助试剂,实验组与对照组的无关变量的影响是相等的,这样通过空白对照实验,对比实验的结果,排除无关变量的影响,则可认定为是来自实验变量的效果,使实验结果更有说服力;
(4)根据N元素守恒,及滴定反应找出N原子与HCl的关系式,根据关系式计算,注意盐酸的体积取3次滴定的平均值减去xml;若x=2.77得到氮元素含量,转化为尿素含量分析判断,总尿素含量低于46.0%的为不合格品.
解答 解:(1)硼的化合价未变化,发生类似复分解反应,反应方程式为(NH4)2B4O7+2HCl+5H2O=4 H3BO3+2NH4Cl,H3BO3为一元弱酸,在水中发生反应H3BO3+H2O?[B(OH)4]-+H+.
故答案为:(NH4)2B4O7+2HCl+5H2O=4H3BO3+2NH4Cl;
(2)加热圆底烧瓶产生水蒸气,进入试管中将生成的氨气吹出;加热产生水蒸气,装置内压强增加,长导管防止装置中压力过大而发生危险,冷却时防止发生倒吸,起安全管作用,
故答案为:圆底烧瓶;作为安全管,防止装置中压力过大而发生危险;防止冷却时发生倒吸;
(3)依据编号1、2、3分析可知编号为4的实验应加入的样品和辅助试剂为10.00mL蒸馏水、0.2g催化剂、20mL浓硫酸,空白、等量对照使用目的是消除其他试剂、实验操作等因素引起的误差,
故答案为:10.00mL蒸馏水、0.2g催化剂、20mL浓硫酸;空白、等量对照以消除其他试剂、实验操作等因素引起的误差;
(4)盐酸的体积为$\frac{33.45+33.90+33.50}{3}$-xml=(33.62-x)×10-3L,
令10ml该液态奶的含氮量的质量为mg,则
2N~(NH4)2B4O7~2HCl
28g 2mol
mg 0.2500mol•L-1×(33.62-x)×10-3L
所以m=3.5(33.62-x)×10-3g,
100ml中即10.0g含氮量3.5(33.62-x)×10-3g×$\frac{100}{10}$=35(33.62-x)×10-3g
含氮量的质量=35(33.62-x)×10-3×$\frac{1000}{10}$g/Kg=117.67-3.5x,
若x=2.77,则肥中的氮含量117.67-3.5×2.77=107.975g/1000g
100g含氮元素10.7975g,转化为尿素质量含量=$\frac{10.7975g}{14g/mol}$×$\frac{1}{2}$×60g/mol=23.1g,则尿素含量<46%,是不合格品,
故答案为:117.67-3.5x;不合格品.
点评 本题知识涉及元素化合物、实验原理、化学计算、化学仪器的使用等,侧重考查学生对实验方案理解、元素化合物的知识,难度较大.


科目:高中化学 来源: 题型:解答题
 )是人造棉的主要成分之一,合成路线如下:
)是人造棉的主要成分之一,合成路线如下: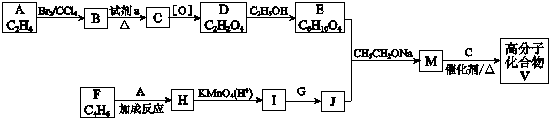
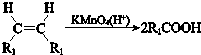
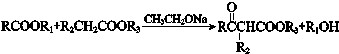 (R、R1、R2、R3表示烃基)
(R、R1、R2、R3表示烃基)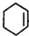 .
.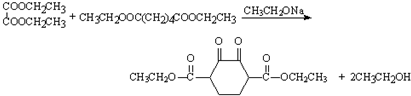 .
.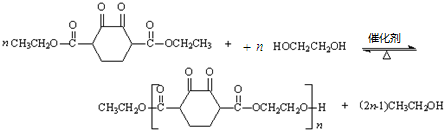 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在标准状况下,0.5 molNO与0.5 molO2混合后气体分子数为0.75 NA | |
| B. | 某温度下纯水的pH=6,该温度下10 L pH=11的NaOH溶液中含OH-的数目为NA | |
| C. | 0.1molAlCl3完全转化为氢氧化铝胶体,生成O.l NA个胶体粒子 | |
| D. | 以Mg、Al为电极,NaOH溶液为电解质溶液的原电池中,导线上流过NA个电子,则正极放出H2的体积为11.2 L |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
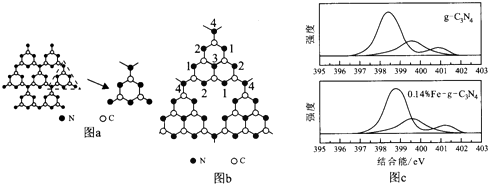
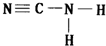 .
.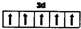 .
.查看答案和解析>>
科目:高中化学 来源: 题型:推断题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | “元质”即现代之“元素”,现在人类发现的化学元素多于六十四种 | |
| B. | “养、轻、淡”即“氧、氢、氮”三种元素,现代的元素命名更具科学性 | |
| C. | 上文提到的八种“元质”包括四种金属“元质”和四种非金属“元质” | |
| D. | “微渺”因极其微小,故“微渺”是组成物质的基本微粒,不可再分 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 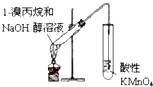 用于检验溴丙烷消去产物 | B. | 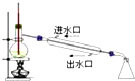 用于石油的分馏 | ||
| C. | 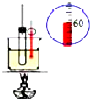 用于实验室制硝基苯 | D. | 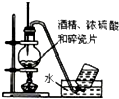 用于实验室制备乙烯 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 某气体能使品红溶液褪色,则该气体是SO2 | |
| B. | 向无色溶液中加入氯水后振荡,再加入CCl4振荡,下层显示紫红色,则原溶液中有I- | |
| C. | 向某溶液中加入硝酸酸化Ba(NO3)2溶液,产生白色沉淀,则原溶液中有SO42- | |
| D. | 向某溶液中加入NaOH,产生可使湿润的蓝色石蕊试纸变红的气体,则原溶液中有NH4+ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com