

 ��E����ˮ��õ�FΪCH2=C��CH3��CH2OH����GΪCH2=C��CH3��CHO��HΪCH2=C��CH3��COOH��H��CH3OH�õ���IΪCH2=C��CH3��COOCH3����JΪ�Ӿ۷�Ӧ�IJ���ṹ��ʽΪ
��E����ˮ��õ�FΪCH2=C��CH3��CH2OH����GΪCH2=C��CH3��CHO��HΪCH2=C��CH3��COOH��H��CH3OH�õ���IΪCH2=C��CH3��COOCH3����JΪ�Ӿ۷�Ӧ�IJ���ṹ��ʽΪ ���ݴ˽��
���ݴ˽�� ��E����ˮ��õ�FΪCH2=C��CH3��CH2OH����GΪCH2=C��CH3��CHO��HΪCH2=C��CH3��COOH��H��CH3OH�õ���IΪCH2=C��CH3��COOCH3����JΪ�Ӿ۷�Ӧ�IJ���ṹ��ʽΪ
��E����ˮ��õ�FΪCH2=C��CH3��CH2OH����GΪCH2=C��CH3��CHO��HΪCH2=C��CH3��COOH��H��CH3OH�õ���IΪCH2=C��CH3��COOCH3����JΪ�Ӿ۷�Ӧ�IJ���ṹ��ʽΪ ��
�� ��ˮ�ⷴӦ����Ӧ�ķ���ʽΪ
��ˮ�ⷴӦ����Ӧ�ķ���ʽΪ ��
��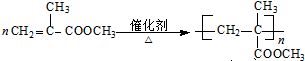 ��
�� ��
�� ��
��


| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��1molNH4+�к�������Ϊ11NA |
| B��1molOH-�к�������Ϊ10NA |
| C��1molNa+�к�������Ϊ10NA |
| D��1molF-���е��������������֮��Ϊ10NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ʵ�鲽�� | Ԥ�������� |
| ����1��ȡ��������ֱ����Թ��У�����һ����������ˮ�ܽ� | ����ȫ���ܽ���û��S���� |
| ����2��ȡ����Һ���HCl | |
| ����3 ȡ����Һ���HCl��BaCl2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
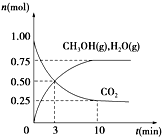 ��1����ѧ����H2��CO2�����״�ȼ�ϣ�Ϊ̽���÷�Ӧԭ������������ʵ�飺ij�¶��£����ݻ�Ϊ2L���ܱ������г���1mol CO2��3.25mol H2����һ�������·�Ӧ�����CO2��CH3OH��g����H2O��g�������ʵ�����n����ʱ��ı仯��ϵ��ͼ��ʾ��
��1����ѧ����H2��CO2�����״�ȼ�ϣ�Ϊ̽���÷�Ӧԭ������������ʵ�飺ij�¶��£����ݻ�Ϊ2L���ܱ������г���1mol CO2��3.25mol H2����һ�������·�Ӧ�����CO2��CH3OH��g����H2O��g�������ʵ�����n����ʱ��ı仯��ϵ��ͼ��ʾ��| ���� ��� | �¶ȣ��棩 | ��ʼ���ʵ�����mol�� | ƽ�����ʵ�����mol�� | |
| CH3OH��g�� | CH3OCH3��g�� | H2O��g�� | ||
| �� | 387 | 0.20 | 0.080 | 0.080 |
| �� | 387 | 0.40 | ||
| �� | 207 | 0.20 | 0.090 | 0.090 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| 9 |
| 4 |
| ��ʼŨ�� | �� | �� | �� |
| c��H2��/mol/L | 0.010 | 0.020 | 0.020 |
| c��CO2��/mol/L | 0.010 | 0.010 | 0.020 |
| A����Ӧ��ʼʱ�����еķ�Ӧ������죬���еķ�Ӧ�������� |
| B��ƽ��ʱ������c��CO2���Ǽ��е�2������0.012mol/L |
| C��ƽ��ʱ�����кͱ���H2��ת���ʾ���60% |
| D��ƽ��ʱ������CO2��ת���ʴ���60% |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����Ӧ�У����ֽ����������ֽ������� |
| B���μӷ�Ӧ�Ľ���Na��Mg��Al�����ʵ���֮��Ϊ6��3��2 |
| C��þ�����ʵ���Ϊ0.1mol |
| D��V=2.24 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com