
| A | B | C | D | |
| 强电解质 | NaCl | H2SO4 | CaCO3 | HNO3 |
| 弱电解质 | HF | BaSO4 | HClO | CH3COOH |
| 非电解质 | Cl2 | CS2 | C2H5OH | H2S |
| A、A | B、B | C、C | D、D |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
A、 碘的CCl4溶液中分离I2并回收CCl4 |
B、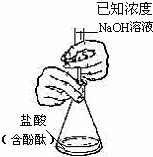 滴定法测定盐酸溶液的浓度 |
C、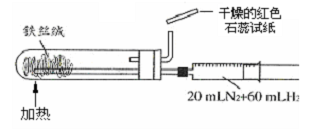 合成氨并检验氨的生成 |
D、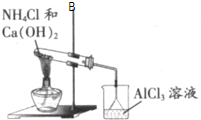 制备Al(OH)3沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、等量的硫蒸气和硫固体分别完全燃烧,后者放出热量多 |
| B、由C(石墨)→C(金刚石)△H=+1.9 kJ?mol-1可知,金刚石比石墨稳定 |
| C、在稀溶液中:H++OH-=H2O△H=-57.3 kJ?mol-1,若将含1 mol CH3COOH的醋酸溶液与含1 mol NaOH的溶液混合,放出的热量小于57.3 kJ |
| D、在101 kPa时,2 g H2完全燃烧生成液态水,放出285.8 kJ热量,氢气燃烧的热化学方程式表示为2H2(g)+O2(g)=2H2O(l)△H=+285.8 kJ?mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、二者在水中的溶解度不同,碳酸氢钠的溶解度大于碳酸钠的溶解度 |
| B、二者热稳定性不同,碳酸钠的热稳定性小于碳酸氢钠的热稳定性 |
| C、二者都能与盐酸反应放出二氧化碳气体,反应快慢相同 |
| D、二者在一定的条件下可以相互转化 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、二氧化硅的水溶液显酸性,所以,二氧化硅是酸性氧化物 |
| B、二氧化碳通入水玻璃可得到硅酸,说明碳酸的酸性比硅酸强 |
| C、高温时二氧化硅与纯碱反应放了二氧化碳,所以硅酸的酸性比碳酸强 |
| D、二氧化硅是酸性氧化物,因此,它不能溶于任何酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:
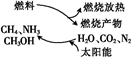 “世界环境日”主题之一是促进物质的循环利用.有专家提出:如果对燃料燃烧产物如CO2、H2O、N2等利用太阳能让它们重新组合,使之能够实现如图转化,在此构想中太阳能最终转化为( )
“世界环境日”主题之一是促进物质的循环利用.有专家提出:如果对燃料燃烧产物如CO2、H2O、N2等利用太阳能让它们重新组合,使之能够实现如图转化,在此构想中太阳能最终转化为( )| A、化学能 | B、热能 |
| C、生物能 | D、电能 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、300 mL 2 mol?L-1的蔗糖溶液中所含分子数为0.6NA |
| B、在标准状况下,2.8g N2和2.8g CO所含电子数不相等 |
| C、0.2 mol H2O2完全分解转移的电子数为0.2NA |
| D、在常温常压下,2.24L SO2与O2的混合气体中所含氧原子数为0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Na2CO3 |
| B、Na2CO3、Na2O2 |
| C、Na2CO3、NaOH |
| D、Na2CO3、Na2O2、NaOH |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、碳酸钙溶液和盐酸溶液混合:CO32-+2H+═CO2↑+H2O |
| B、硫酸溶液和氢氧化钠溶液混合:H++OH-═H2O |
| C、少量金属钠放入冷水中:Na+2H2O═Na++2OH-+H2↑ |
| D、铁与足量稀盐酸反应:2Fe+6H+=2Fe3++3H2↑ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com