
����Ŀ����ѧ��Ӧ����Ϊ�ɼ����Ѻ��¼��γɵĹ��̣���ѧ���ļ������γɣ����1mol��ѧ��ʱ�ͷţ������գ�������������֪����P4O6�ķ��ӽṹ����ͼ��ʾ�����ṩ���»�ѧ���ļ��ܣ�kJmol��1��P��P��198 P��O��360 O�TO��498��ӦP4�����ף�+3O2��P4O6�������仯Ϊ�� �� 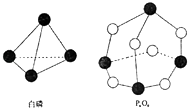
A.�ͷ�1638kJ������
B.����1638kJ������
C.�ͷ�126kJ������
D.����126kJ������
 ����С״Ԫ��������������ϵ�д�
����С״Ԫ��������������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ϊ�˳�ȥ�����е�CaCl2��MgCl2��Na2SO4����ɳ���ɽ���������ˮ��Ȼ�����������������ٹ��ˣ��ڼӹ���NaOH��Һ���ۼ���������ܼӹ���Na2CO3��Һ���ݼӹ���BaCl2��Һ�����в���˳��������ʵ���
A. �٢ܢڢݢ� B. �ܢ٢ڢݢ� C. �ڢݢܢ٢� D. �ݢڢܢۢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������ѧ��Ӧ��ƽ�ⳣ����K1��K2��K3�����¶ȵĹ�ϵ�ֱ����±���ʾ����ش� 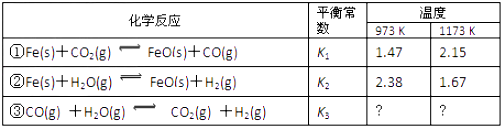
������Ӧ��ƽ�ⳣ���ֱ�ΪK1��K2��K3�ƶϷ�Ӧ��Ϊ��H30��������ɡ����������ݷ�Ӧ�ٺͷ�Ӧ�ڿ��Ƶ���K1��K2��K3�Ĺ�ϵʽ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ���ǣ� ��
A. ������ˮ������һ���ǵ����
B. Һ̬�Ȼ����ܵ���
C. Һ̬�Ȼ����ܵ���
D. ����״̬�����ǵ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��H7N9����������һ�����������У��о��������ò����������У����2�������ϼ���ʧȥ���ԣ����ೣ������ҩ������������ء�Ư�ۡ������ȣ�Ҳ�����Խ��ò���ɱ��
��1��������ˮ�к��ж�����������ɫʯ����Һ������ˮ�У���Һ�Ժ�ɫ�����õ�����____����һ�������Һ��ɫ����ȥ�������õ�����______��
��2����ҵ����ȡƯ�۵ķ�Ӧ����ʽΪ��___________��
��3����֪���������Ũ�������ܲ�����������ѧ��Ӧ����ʽΪ��2KMnO4 +16HCl ![]() 2MnCl2+2KCl+8H2O+5Cl2��
2MnCl2+2KCl+8H2O+5Cl2��
�÷�Ӧ��������Ϊ________������˫���ŷ���ʾ����ת�Ƶ������_________________
��4����Ư����Һ�еμ�̼������Һ���а�ɫ�������ɣ�д��������Ӧ�����ӷ���ʽ___��
��5������������ͨ��FeBr2��Һ�У�д���÷�Ӧ�����ӷ���ʽ__________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ���ǣ� �� 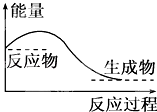
A.�κλ�ѧ��Ӧ�������������ı仯
B.H2O��g���TH2O��l���ù��̷ų��������ȣ����Ըù����ǻ�ѧ�仯
C.��ѧ��Ӧ�������ı仯������Ϊ�����ı仯
D.������ͼ��ʾ�Ĺ��̣������������Ĺ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й����Ƽ��仯�����˵������ȷ���ǣ� ��
A.��2.3 g NaͶ�뵽97.7 gˮ�г�ַ�Ӧ��������Һ����������Ϊ4.0%
B.��ͬ���������ֱ��������������NaOH��Һ��Ӧ�������������ʵ���֮��Ϊ1��3
C.��CO2��H2O�Ļ������a mol����������Na2O2�����ַ�Ӧ�����ɵ�O2�ڱ�״���µ����Ϊ11.2a L
D.120 mL����0.20 mol̼���Ƶ���Һ��200 mL������еμӷ�Ӧ�����ܽ�ǰ�ߵ�����ߣ����Ǻ��ߵ���ǰ�ߣ��μ���ȫ��������������ͬ������������ȣ��������Ũ�ȿ���Ϊ2 mol/L
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����̼����������������Ԫ�صĻ�����㷺��������Ȼ�磬�ش��������⣺
��1����̬��ԭ�ӵ���Χ�����Ų�ʽΪ��Fe3+��Fe2+�ȶ���ԭ���� ��
��2���ڶ������У�Ԫ�صĵ�һ�����ܴ���B��N֮���Ԫ�����֣�
��3��NF3�����ӹ�ҵ�������ĵ����ӿ�ʴ���壬NF3���ӵĿռ乹��Ϊ����NF3�У�Nԭ�ӵ��ӻ��������Ϊ ��
��4����ʯī�ṹ���Ƶ��������������У�����Bԭ����Nԭ��֮��Ļ�ѧ��Ϊ �� ���������Ϊ ��
��5��S��Fe�γɵ�ij������侧����ͼ��ʾ��������ʵĻ�ѧʽΪ �� ����þ������ܶ�Ϊ�� g/cm3 �� ��NA��ʾ�����ӵ���������þ����о��������Sԭ��֮��ľ���Ϊ���г�����ʽ���ɣ�cm�� 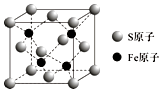
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������մ��һЩ��ˮϴ�����IJ������ϴ�ӷ�����ȷ���ǣ� ��
�ٲ������Թ��ڱ��ϵĵ⣬�þƾ�ϴ�� ��ʢ�Ź����ӵ��Լ�ƿ�в����ı��ӣ��þƾ�ϴ�� ����������Ӧ���Թܱ�����������ϡ��ˮϴ�� ��մ�����Թ��ڱ��ϵ��������ȼ�Һϴ��
A.�٢ۢ�B.�ڢۢ�C.�٢ڢ�D.�٢ڢۢ�
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com