
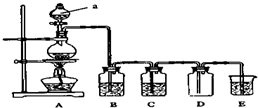
 如图是实验室中制备气体或验证气体性质的装置图.
如图是实验室中制备气体或验证气体性质的装置图.分析 (1)熟悉仪器图形,说出其名称;
(2)①二氧化锰与浓盐酸在加热条件下反应生成氯化锰、水和氯气;
②浓盐酸易挥发,制取的氯气中含有氯化氢,氯化氢易溶于水氯气在水中溶解度较小,可以用饱和食盐水除去氯化氢;
氯气有毒,直接排放引起空气污染,氯气能够与氢氧化钠反应生成氯化钠、次氯酸钠和水,可用氢氧化钠溶液吸收氯气;
(3)先验证二氧化硫后验证二氧化碳,二氧化硫具有漂白性,要先在B装置中放入品红溶液验证二氧化硫;由于二氧化硫也能与石灰水反应产生沉淀会干扰二氧化碳的验证,所以在验证二氧化碳之前要保证把二氧化硫除去,这样就需要在C装置中放入酸性高锰酸钾溶液,D中装入品红溶液,检验二氧化硫是否除尽,最后用澄清石灰水检验二氧化碳的存在.
解答 解:(1)仪器a的名称是分液漏斗;
故答案为:分液漏斗;
(2)①二氧化锰与浓盐酸在加热条件下反应生成氯化锰、水和氯气,离子方程式:MnO2+4H++2Cl-═Mn2++Cl2+2H2O;
故答案为:MnO2+4H++2Cl-═Mn2++Cl2+2H2O;
②浓盐酸易挥发,制取的氯气中含有氯化氢,氯化氢易溶于水氯气在水中溶解度较小,可以用饱和食盐水除去氯化氢;氯气有毒,直接排放引起空气污染,氯气能够与氢氧化钠反应生成氯化钠、次氯酸钠和水,可用氢氧化钠溶液吸收氯气;
故答案为:饱和NaCl溶液;吸收氯气防污染;
(3)先验证二氧化硫后验证二氧化碳,二氧化硫具有漂白性,要先在B装置中放入品红溶液验证二氧化硫;由于二氧化硫也能与石灰水反应产生沉淀会干扰二氧化碳的验证,所以在验证二氧化碳之前要保证把二氧化硫除去,这样就需要在C装置中放入酸性高锰酸钾溶液,D中装入品红溶液,检验二氧化硫是否除尽,最后用澄清石灰水检验二氧化碳的存在;
①二氧化硫具有漂泊性,能够使品红溶液褪色,据此检验二氧化硫的存在;
故答案为:B;品红溶液褪色;
②证明SO2具有还原性装置为C,现象酸性高锰酸钾褪色;
故答案为:C中KMnO4溶液褪色;
③为排除二氧化硫对二氧化碳检验的干扰,应在D中加入品红溶液,检验SO2是否除尽;
故答案为:检验SO2是否除尽;
④如果D中品红不褪色,说明二氧化硫除尽,则能够使澄清石灰水变浑浊的其他
D中品红不褪色且E中石灰水变浑浊的气体为二氧化碳;
故答案为:D中品红不褪色且E中石灰水变浑浊.
点评 本题考查了氯气的制备,二氧化硫、二氧化碳的检验,熟悉装置的特点及各物质的性质是解题关键,题目难度中等.


 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案科目:高中化学 来源: 题型:解答题
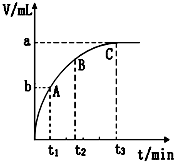 某课外兴趣小组对H2O2的分解速率做了如下实验探究.
某课外兴趣小组对H2O2的分解速率做了如下实验探究.| 30%H2O2 | 15%H2O2 | 10%H2O2 | 5%H2O2 | |
| 无催化剂、不加热 | 几乎不反应 | 几乎不反应 | 几乎不反应 | 几乎不反应 |
| 无催化剂、加热 | 360 | 480 | 540 | 720 |
| MnO2催化剂、加热 | 10 | 25 | 60 | 120 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
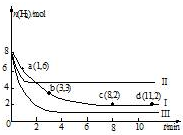 一定温度下,向容积为2L的恒容密闭容器中充入6molCO2和8molH2,发生反应:
一定温度下,向容积为2L的恒容密闭容器中充入6molCO2和8molH2,发生反应:| A. | 该反应在0~8min内CO2的平均反应速率是0.375mol•L-1•min-1 | |
| B. | 若起始时向上述容器中充入3molCO2和4molH2,则平衡时H2的条件分数大于20% | |
| C. | 若起始是向上述容器中充入4molCO2、2molH2、2molCH3OH和1molH2O(g),则此是反应向正反应方向进行 | |
| D. | 改变条件得到曲线II、III,则曲线II、III改变的他分别是升高温度、充入氢气 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 工业制金属钠:电解饱和食盐水 | |
| B. | 工业制溴:某些植物有富集溴的能力,从海产品中提取溴是工业上获取溴的重要途径 | |
| C. | 冶炼铝:电解Al2O3,同时加入冰晶石(Na3AlF6),目的是为了降低Al2O3熔融温度 | |
| D. | 硫酸工业:在氧气充足的情况下,从接触室进入吸收塔的气体中不可能含有SO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 已知:A是石油裂解气的主要成份,A的产量通常用来衡量一个国 家的石油化工水平.现以A为主要原料合成乙酸乙酯,其合成路线如图所示.
已知:A是石油裂解气的主要成份,A的产量通常用来衡量一个国 家的石油化工水平.现以A为主要原料合成乙酸乙酯,其合成路线如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
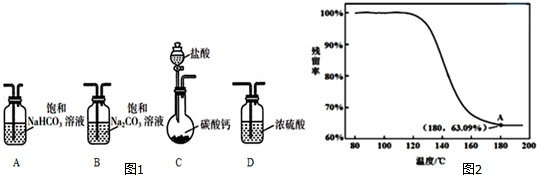
NaHCO3溶液 BaCl2浓度 | 0.2mol•L-1 | 0.1mol•L-1 | 0.02mol•L-1 |
| 0.2mol•L-1 | 浑浊 | 浑浊 | 少许浑浊 |
| 0.1mol•L-1 | 浑浊 | 少许浑浊 | 无现象 |
| 0.02mol•L-1 | 少许浑浊 | 无现象 | 无现象 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 6.72L CO | B. | 6.6g CO2 | C. | 8 g SO2 | D. | 9.6g H2SO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 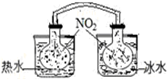 依据两容器内气体颜色变化,判断反应2NO2(g)?N2O4(g)平衡移动的方向 | |
| B. | 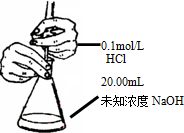 测定锥形瓶内的NaOH的浓度 | |
| C. | 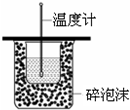 测定中和热 | |
| D. | 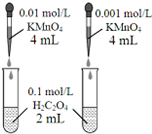 依据褪色快慢比较浓度对反应速率的影响 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题


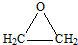 .
.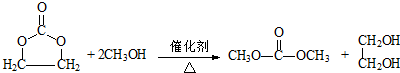 .
.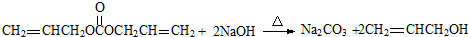 .
. .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com