
| A. | 是氧化剂 | B. | 是还原剂 | ||
| C. | 既是氧化剂又是还原剂 | D. | 既不是氧化剂又不是还原剂 |
科目:高中化学 来源: 题型:选择题
| A. | 侯氏制碱法的工艺过程中应用了物质溶解度的差异 | |
| B. | 除去KNO3中混杂的NaCl,可用重结晶的方法,是因为氯化钠在水中溶解度大 | |
| C. | 用量筒量取20mL 0.5 mol•L-1H2SO4于烧杯中,加水80mL,配制成0.1 mol•L-1H2SO4溶液 | |
| D. | 将足量的Na2O、Na2O2分别加入到酚酞溶液中,最终溶液均为红色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,44g CO2中含有2NA个π键 | |
| B. | 1mol•L-1NaCl溶液含有NA个Na+ | |
| C. | 0.5mol Cu和足量浓硝酸反应可以生成22.4LNO2 | |
| D. | 过量的液溴与铁反应,若反应中消耗1mol铁,则转移的电子数目为2NA个 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 反应容器内的压强不随时间改变 | |
| B. | 反应容器内P、Q、R、S四者共存 | |
| C. | P的生成速率和S的生成速率相等 | |
| D. | 反应容器内的气体总物质的量不随时间变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,11.2L NH3所含的原子数为2NA | |
| B. | 常温常压下,80g SO3含有的氧原子数为3NA | |
| C. | 标准状况下,22.4L H2中所含原子数为NA | |
| D. | 标准状况下,22.4L H2O中所含分子数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 单质的熔、沸点逐渐降低 | B. | 与H2反应越来越容易 | ||
| C. | F-、Cl-、Br-、I-的还原性逐渐增强 | D. | 单质的氧化性逐渐增强 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 亚硫酸钠溶液显碱性:SO32-+2H2O=H2SO3+2OH- | |
| B. | (NH4)2FeSO4溶液与过量NaOH溶液混合制取氢氧化亚铁:Fe2++2OH-=Fe(OH)2 | |
| C. | NaAlO2溶液中通入过量CO2制取氢氧化铝:2AlO2-+CO2+3H2O=2Al(OH)3+CO32- | |
| D. | 铁红溶于HI酸溶液:Fe2O3+6H++2I-=2Fe2++I2+3H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 体系的压强不再改变 | |
| B. | 体系的温度不再改变 | |
| C. | 消耗1molN2的同时,新生成3molH2 | |
| D. | 反应消耗的N2、H2与产生的NH3的速率υ(N2):υ(H2):υ(NH3)═1:3:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
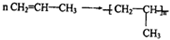
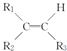 $\stackrel{KMnO_{4}(H+)}{→}$
$\stackrel{KMnO_{4}(H+)}{→}$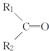 +R3-COOH,
+R3-COOH,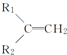 $\stackrel{KMnO_{4}(H+)}{→}$
$\stackrel{KMnO_{4}(H+)}{→}$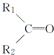 +CO2
+CO2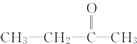 ),则此烯烃的结构简式是CH2=C(CH3)C2H5.
),则此烯烃的结构简式是CH2=C(CH3)C2H5.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com