
科学家近年来研制出一种新型细菌燃料电池,利用细菌将有机物转化为氢气,氢气进入以硫酸为电解质的燃料电池发电。电池负极反应为 ( )
A H2+2OH--2e-=2H2O B O2+4H++4e-=2H2O
C H2-2e-=2H+ D O2+2H2O+4e-=4OH-
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
镁是海水中含量较多的金属元素,单质镁、镁合金以及镁的化合物在科学研究和工业生产中用途非常广泛。
(1)Mg2Ni是一种储氢合金,已知:
Mg(s)+H2(g)=MgH2(s) △H1=—74.5kJ·mol-1
Mg2Ni(s)+2H2(g)=Mg2NiH4(s) △H2=—64.4kJ·mol-1
Mg2Ni(s)+2 MgH2(s)=2Mg(s)+ Mg2NiH4(s) △H3
则△H3=____________ kJ·mol-1
(2)工业上可用电解熔融的无水氯化镁获得镁。其中氯化镁晶体脱水是关键的工艺之一。一种正在试验的氯化镁晶体脱水的方法是:先将MgCl2·6H20转化为MgCl2·NH4Cl·nNH3,然后在700℃脱氨得到无水氯化镁,脱氨反应的化学方程式为_________________________;用惰性电极电解熔融氯化镁,阴极的电极反应式为______________________________
(3)储氢材料Mg(AlH4)2在110℃—200℃的反应为: Mg(AlH4)2=MgH2+2Al+3H2↑,每生成27gAl转移电子的物质的量为__________
(4)镁的一种化合物氯酸镁[Mg(ClO3)2]常用作催熟剂、除草剂等。为了确定实验室制备的Mg(ClO3)2•6H2O的纯度,做如下试验:
步骤1:准确称量3.50g产品配成100mL溶液.
步骤2:取10mL于锥形瓶中,加入10mL稀硫酸和20mL 1.000mol•L-1的FeSO4溶液,微热.
步骤3:冷却至室温,用0.100mol•L-1 K2Cr2O7溶液滴定至终点,此过程中反应的离子方程式为:Cr2O72-+6Fe2++14H+═2Cr3++6Fe3++7H2O.
步骤4:将步骤2、3重复两次,平均消耗K2Cr2O7溶液15.00mL.
产品中Mg(ClO3)2•6H2O的纯度为__________(用百分号表示,精确到小数点后一位)
(5)一种有机镁化合物可用于制造光学元件的涂布液,化学式可表示为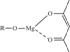 ,它可以发生如下反应:
,它可以发生如下反应:
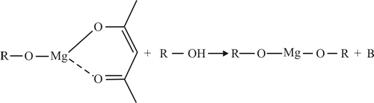
ROH与B的核磁共振氢谱如下图:
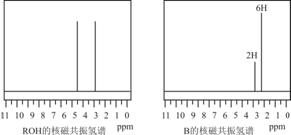
ROH由C、H、O、F四种元素组成的含氟化合物,分子中只有一个氧原子,所有氟原子化学环境相同,相对分子质量为168,则ROH的结构简式为_______________;B的结构简式为_________________
查看答案和解析>>
科目:高中化学 来源: 题型:
绿色化学的目标是 ( )
A.减少对环境的污染 B.防患于未然,最终杜绝化学污染源
C.设计对人类健康和环境更安全的化合物
D.研究变换基本原料和起始化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
已知下列分子或离子在酸性条件下都能氧化KI,自身发生如下变化
H2O2 → H2O IO3- →I MnO4- → Mn2+ HNO3 → NO
如果用等物质的量的这些物质氧化足量的KI,得到I2最多的是( )
A.H2O2 B. IO3- C. MnO4- D.HNO3
查看答案和解析>>
科目:高中化学 来源: 题型:
甲烷中混有乙烯,欲除乙烯得到纯净的甲烷,可依次将其通过下列哪组试剂的洗气瓶( )
A.澄清石灰水,浓H2SO4 B.溴水,浓H2SO4
C.酸性高锰酸钾溶液,浓H2SO4 D.浓H2SO4,酸性高锰酸钾溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
现将0.1mol某烃完全燃烧生成的气体全部依次通过浓硫酸和氢氧化钠溶液,经测定,前者增重10.8g ,后者增重22g(假定气体全部吸收)。试通过计算推断该烃的分子式(要有计算过程)。若该烃的一氯代物只有一种,试写出该烃的结构简式。
查看答案和解析>>
科目:高中化学 来源: 题型:
一定量的Zn与过量的稀硫酸反应制取氢气,一定温度下为了加快反应速率而不影响氢气的量,可向其中加入 ( )
A.KNO3固体 B.Zn粉 C. Cu粉 D.CH3COONa晶体
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
A.强电解质溶液的导电能力一定比弱电解质溶液的导电能力强
B.物质的量浓度相同的磷酸钠(Na3PO4)溶液和磷酸(H3PO4)溶液中PO43-的物质的量浓度相同
C.足量Zn分别和等体积、等物质的量浓度的盐酸和醋酸反应时,产生H2的量相同,放出H2的速率不等
D.因为CH3COOH是弱电解质,HCl是强电解质,所以中和等体积等物质的量浓度的醋酸和盐酸时,中和醋酸消耗的NaOH比盐酸消耗的NaOH用量少
查看答案和解析>>
科目:高中化学 来源: 题型:
工业合成氨与制备硝酸一般可连续生产,流程如图所示:
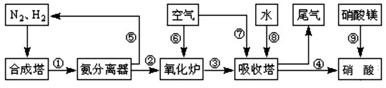
(1)工业生产时,制取氢气的一个反应为:CO+H2O(g) CO2+H2
CO2+H2
T℃时,往1L密闭容器中充入0.2mol CO和0.3mol水蒸气。反应建立平衡后,体系中c(H2)=0.12mol·L-1。该温度下此反应的平衡常数K=_____(填计算结果)。
(2)合成塔中发生反应N2(g)+3H2(g) 2NH3(g);△H<0。下表为不同温度下该反应的平衡常数。由此可推知,表中T1____573K(填“>”、“<”或“=”)。
2NH3(g);△H<0。下表为不同温度下该反应的平衡常数。由此可推知,表中T1____573K(填“>”、“<”或“=”)。
| T/℃ | T1 | 300 | T2 |
| K | 1.00×107 | 2.45×105 | 1.88×103 |
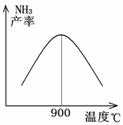
(3)N2和H2以铁作催化剂从145℃就开始反应,不同温度下NH3的产率如图所示。温度高于900℃时,NH3产率下降的原因是
(4)硝酸厂的尾气直接排放将污染空气,目前科学家探索利用燃料气体中的甲烷等将氮氧化物还原为氮气和水,其反应机理为:
CH4(g)+4NO2=(g)=4NO(g)+CO2(g)+2H2O(g); △H=-574kJ·mol-1
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g); △H=-1160kJ·mol-1
则甲烷直接将NO2还原为N2的热化学方程式为:
(5)氨气在纯氧中燃烧,生成一种单质和水。科学家利用此原理,设计成氨气-氧气燃料电池,则通入氨气的电极碱性条件下发生反应的电极反应式为
。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com