
| 温度/℃ | 700 | 800 | 830 | 1 000 | 1 200 |
| 平衡常数 | 0.4 | 0.6 | 1.0 | 1.1 | 1.6 |
分析 ①平衡常数是指一定温度下,可能反应到达平衡时生成物浓度系数次幂的乘积与反应物浓度系数次幂的乘积的比;
由表中数据可知,随温度升高平衡常数增大,说明升高温度平衡向正反应方向移动;
②设参加反应的A为xmol,表示出平衡时各组分的物质的量,由于反应前后气体的体积不变,用物质的量代替浓度代入平衡常数表达式列方程计算;
增大某一反应物的浓度,平衡正向移动,其它反应物的转化率增大,自身转化率减小.
解答 解:①A(g)+B(g)═C(g)+D(g)的平衡常数表达式K=$\frac{c(C)×c(D)}{c(A)×c(B)}$,由表中数据可知,随温度升高平衡常数增大,说明升高温度平衡向正反应方向移动,正反应为吸热反应,故△H>0,
故答案为:$\frac{c(C)×c(D)}{c(A)×c(B)}$;>;
②设参加反应的A为xmol,则:
A(g)+B(g)═C(g)+D(g)
起始量(mol):0.2 0.6 0 0
变化量(mol):x x x x
平衡量(mol):0.2-x 0.6-x x x
由于反应前后气体的体积不变,可以用物质的量代替浓度计算平衡常数,则$\frac{x×x}{(0.2-x)×(0.6-x)}$=1,解得x=0.15,故A的转化率为$\frac{0.15mol}{0.2mol}$×100%=75%;
再向该密闭容器中再充入1molA气体,平衡向正反应移动,平衡时A的转化率减小,
故答案为:75%;右;减小.
点评 本题考查化学平衡计算、平衡常数等,难度不大,旨在考查学生对基础知识的理解掌握.


科目:高中化学 来源: 题型:填空题
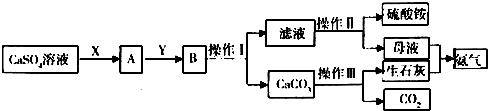
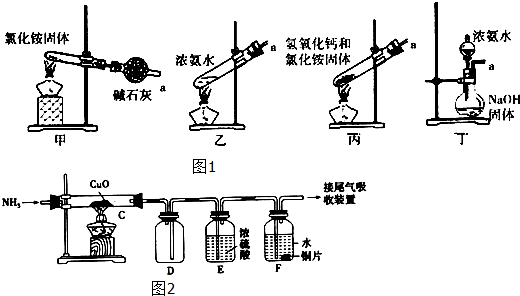
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 盛待测液的锥形瓶用蒸馏水洗后未用待测液润洗 | |
| B. | 滴定管尖嘴部分在滴定前有气泡 | |
| C. | 滴定管在滴定前未将刻度调在“0.00”,而调在“2.40” | |
| D. | 滴定达终点时,滴定管尖嘴部分有气泡 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 为了使反应均匀进行,可以向酸(碱)中分次加入碱(酸) | |
| B. | 为了准确测定反应混合溶液的温度,实验中温度计水银球应一直插入溶液中 | |
| C. | 用0.5 mol•L-1 NaOH溶液分别与0.5mol•L-1的盐酸、醋酸溶液反应,如所取的溶液体积相等,则测得的中和热数值相同 | |
| D. | 为了使反应更完全,可以使酸或碱的浓度适当过量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 水;无水氯化钙 | B. | 饱和NaHCO3溶;浓硫酸 | ||
| C. | 浓硫酸;饱和Na2CO3溶液 | D. | 饱和Na2CO3溶液;稀硫酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | K+、MnO4-、Na+、Cl- | B. | Na+、Cl-、NO3-、SO42- | ||
| C. | K+、Na+、NO3-、HCO3- | D. | Fe3+、Na+、CO32-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
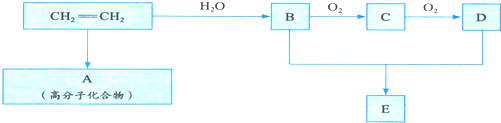
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com