
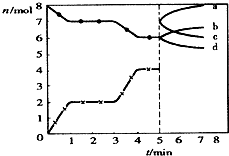
 炼铁的还原剂CO是由焦炭和CO2反应而得.现将焦炭和CO2放入体积为2L的密闭容器中,高温下进行下列反应:C(s)+CO2(g)?2CO(g)△H=QkJ/mol.如图为CO2、CO的物质的量n随时间t的变化关系图.下列说法正确的是( )
炼铁的还原剂CO是由焦炭和CO2反应而得.现将焦炭和CO2放入体积为2L的密闭容器中,高温下进行下列反应:C(s)+CO2(g)?2CO(g)△H=QkJ/mol.如图为CO2、CO的物质的量n随时间t的变化关系图.下列说法正确的是( )A、0~lmin,v(CO)=1mol/(L?min);1~3min时,v(CO)=v(CO2);该反应的平衡常数表达式为k=
| ||
B、当容器内的压强不变时,该反应一定达到平衡状态,且
| ||
C、3min时温度由T1升高到T2,则Q>O,重新平衡时
| ||
| D、5min时再充入一定量的CO,c、b曲线分别表示n(CO)、n(CO2)的变化 |
| ||
| 1min |
| c2(CO) |
| c(CO2) |
(
| ||
|
| 2 |
| 7 |
| c2(CO) |
| c(CO2) |
(
| ||
|
| 4 |
| 3 |
| K(T2) |
| K(T1) |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| A、可食用植物油含有的高级脂肪酸甘油酯是人体的营养物质 |
| B、分馏、干馏都是物理变化,裂化、裂解都是化学变化 |
| C、淀粉、蛋白质、葡萄糖都是高分子化合物 |
| D、汽油、生物柴油、酒精都是碳氢化合物,都可作燃料 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、常温常压下11.2L的甲烷气体含有甲烷分子数为0.5NA个 |
| B、24gMg变为Mg2+时失去的电子数为2NA |
| C、32gO2和O3混合气体中含有氧原子的个数为2NA |
| D、1L1mol/LNaCl溶液中含有钠离子的个数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
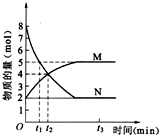 化学反应速率与化学平衡的理论研究对工农业生产有重要的意义.一定温度下,在容积为20L的密闭容器中进行a N(g)?b M(g) 的化学反应,M、N 的物质的量随时间的变化曲线如图所示:
化学反应速率与化学平衡的理论研究对工农业生产有重要的意义.一定温度下,在容积为20L的密闭容器中进行a N(g)?b M(g) 的化学反应,M、N 的物质的量随时间的变化曲线如图所示:查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氮化硅陶瓷是新型无机非金属材料属共价化合物 |
| B、C60由原子直接组成的晶体,可用于制造纳米材料 |
| C、纤维素、蛋白质、酚醛树脂都属于天然高分子材料 |
| D、单晶硅常用于制造半导体材料和光导纤维 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com