
将盛有NH4HCO3粉末的小烧杯放入盛有少量醋酸的大烧杯中。然后向小烧杯中加入盐酸,反应剧烈,醋酸逐渐凝固。由此可见 ( )
| A.NH4HCO3和盐酸的反应是放热反应 |
| B.该反应中,热能转化为产物内部的能量 |
| C.反应物的总能量高于生成物的总能量 |
| D.反应的热化学方程式为NH4HCO3+HCl―→NH4Cl+CO2↑+H2O ΔH=+Q kJ·mol-1 |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:单选题
工业生产水煤气的反应为:C(s)+H2O(g)=CO(g)+H2(g) ΔH=+131.4 kJ·mol-1,下列判断正确的是 ( )。
| A.反应物能量总和大于生成物能量总和 |
| B.CO(g)+H2(g)=C(s)+H2O(l)ΔH=-131.4 kJ·mol-1 |
| C.水煤气反应中生成1 mol H2(g)吸收131.4 kJ热量 |
| D.水煤气反应中生成1体积CO(g)吸收131.4 kJ热量 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
北京奥运会开幕式在李宁点燃鸟巢主火炬时达到高潮。奥运火炬采用的是环保型燃料——丙烷,其燃烧时发生反应的化学方程式为C3H8+5O2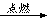 3CO2+4H2O。下列说法中不正确的是( )
3CO2+4H2O。下列说法中不正确的是( )
| A.火炬燃烧时化学能只转化为热能 |
| B.所有的燃烧反应都会释放热量 |
| C.1mol C3H8和5mol O2所具有的总能量大于3mol CO2和4mol H2O所具有的总能量 |
| D.丙烷完全燃烧的产物对环境无污染,故丙烷为环保型燃料 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
一定量的氢气在一定条件下完全燃烧生成气态水,放出热量值为Q1,等量的H2在同样条件下完全燃烧生成液态水,放出热量值为Q2,则Q1与Q2的关系为( )
| A.Q1>Q2 | B.Q1=Q2 | C.Q1<Q2 | D.无法确定 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
有关键能数据如表所示:
| 化学键 | N≡N | H—H | H—N |
| 键能/kJ·mol-1 | x | 436 | 391 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
已知乙炔与苯蒸气完全燃烧的热化学方程式如下所示:
①2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l)
ΔH=-2 600 kJ·mol-1
②2C6H6(g)+15O2(g)=12CO2(g)+6H2O(l)
ΔH=-6 590 kJ·mol-1
下列说法正确的是( )
| A.2 mol C2H2(g)完全燃烧生成气态水时放热大于2 600 kJ |
| B.2 mol C6H6(l)完全燃烧生成液态水时放热大于6 590 kJ |
| C.相同条件下,等质量的C2H2(g)与C6H6(g)完全燃烧,C6H6(g)放热更多 |
| D.C2H2(g)三聚生成C6H6(g)的过程属于放热反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列说法中正确的是( )
| A.熵减的吸热反应可能是自发反应 |
| B.需要加热的化学反应,生成物的总能量一定高于反应物的总能量 |
| C.使用催化剂既不会改变反应的限度又不会改变反应的焓变 |
D.已知2C(s)+2O2(g) 2CO2(g) ΔH1; 2CO2(g) ΔH1; |
 2CO(g) ΔH2,则ΔH1>ΔH2
2CO(g) ΔH2,则ΔH1>ΔH2查看答案和解析>>
科目:高中化学 来源: 题型:单选题
在298 K、1.01×105 Pa下,将22 g CO2通入750 mL 1 mol·L-1NaOH溶液中充分反应,测得反应放出x kJ的热量。已知在该条件下,1 mol CO2通入1 L 2 mol·L-1 NaOH溶液中充分反应放出y kJ的热量。则CO2与NaOH溶液反应生成NaHCO3的热化学方程式为( )
A.CO2(g)+NaOH(aq) NaHCO3(aq) ΔH=-(2y-x)kJ·mol-1 NaHCO3(aq) ΔH=-(2y-x)kJ·mol-1 |
B.CO2(g)+NaOH(aq) NaHCO3(aq) ΔH=-(2x-y)kJ·mol-1 NaHCO3(aq) ΔH=-(2x-y)kJ·mol-1 |
C.CO2(g)+NaOH(aq) NaHCO3(aq) ΔH=-(4x-y)kJ·mol-1 NaHCO3(aq) ΔH=-(4x-y)kJ·mol-1 |
D.CO2(g)+NaOH(aq) NaHCO3(aq) ΔH=-(8x-2y)kJ·mol-1 NaHCO3(aq) ΔH=-(8x-2y)kJ·mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
化学与环境、材料、信息、能源关系密切,下列说法错误的是 ( )。
| A.低碳生活注重节能减排,减少温室气体的排放 |
| B.我国首艘航母“辽宁舰”上用于舰载机降落的拦阻索是特种钢缆,属于金属材料 |
| C.半导体行业中有一句话:“从沙滩到用户”,计算机芯片的材料是二氧化硅 |
| D.页岩气是从页岩层中开采出来的天然气,产气页岩分布广、厚度大,且普遍含气,故可以成为提供廉价而充足的新型燃料来源 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com