
【题目】磷化铝(AlP)和磷化氢(PH3)都是粮食储备常用的高效熏蒸杀虫剂。
(1)磷元素在元素周期表中的位置:________________。AlP遇水蒸气会发生反应放出PH3气体,该反应的另一种产物的化学式为________。
(2)PH3具有强还原性,能与CuSO4溶液反应,配平该反应的化学方程式:
________CuSO4+_____PH3+_____H2O=_____Cu3P↓+_____H3PO4+_____H2SO4
(3)工业制备PH3的流程如图所示。

①次磷酸属于________元酸。
②白磷和烧碱溶液反应的化学方程式为:____________________________________。
③若起始时有1 mol P4参加反应,则整个工业流程中共生成________mol PH3。(不考虑产物的损失)
【答案】第3周期第VA族 Al(OH)3 24 11 12 8 3 24 1 P4 + 3NaOH + 3H2O=PH3↑+ 3NaH2PO2 2.5
【解析】
(1)原子结构中电子层数等于周期数,最外层电子数等于族序数,AlP遇水蒸气会发生反应放出PH3气体,根据元素守恒确定该反应的另一种产物的化学式;
(2)配平化学方程式,就是通过在各物质的化学式前面添加系数,使反应中每种原子个数在反应前后相等的过程,但对于复杂的化学反应通常通过观察,找出变化的特点或规律,常使用化合价来配平,保证化合价升高与降低的数相等即可;
(3)①根据物质电离出的氢离子数目确定酸的元数;
②根据图示信息:白磷和烧碱溶液反应生成PH3、NaH2PO2,据此书写方程式;
③根据发生反应的过程寻找关系式,进行计算即可。
(1)P处于第3周期ⅤA族,AlP遇水蒸气会发生反应放出PH3气体,根据元素守恒,确定该反应的另一种产物是Al(OH)3,故答案为:第3周期第VA族;Al(OH)3;
(2)该方程式中Cu价态由+2下降为+1,P价态由-3升高为+5,为保证化合价升降数相等,Cu3P与H3PO4计量数分别为8、3,CuSO4的系数是24,H2SO4系数是24,根据元素守恒,得到:![]() ,故答案为:24,11,12,8,3,24;
,故答案为:24,11,12,8,3,24;
(3)①根据氢氧化钠过量时只能生成NaH2PO2可知次磷酸只能电离出1个氢离子,因此次磷酸属于一元酸,故答案为:1;
②根据图示信息:白磷和烧碱溶液反应生成PH3、NaH2PO2,方程式为:![]() ;故答案为:
;故答案为:![]() ;
;
③P4+3NaOH+3H2O=PH3↑+3NaH2PO2;2H3PO2=PH3↑+H3PO4,即P4~2.5PH3,若起始时有1molP4参加反应,则整个工业流程中共生成2.5molPH3;故答案为:2.5。


科目:高中化学 来源: 题型:
【题目】某研究小组取50g含十二水硫酸铝铵〔NH4Al(SO4)2·12H2O俗称铝铵矾〕的样品投入200mL稀硫酸中,待固体全部溶解后,向所得溶液中加入NaOH溶液,生成沉淀的物质的量(n)与加入NaOH溶液的体积(V)的关系如图所示:
(假设铝铵矾中的杂质不溶于H2SO4,也不溶于NaOH)
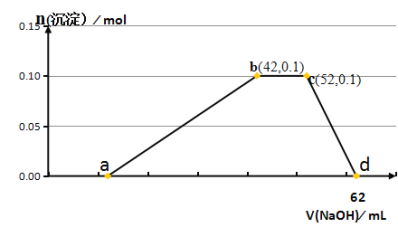
请回答下列问题:
(1)cd段反应的离子方程式是___;
(2)图中b点溶液中的溶质有___;
(3)铝铵矾溶于水时的电离方程式是___;
(4)H2SO4的物质的量的浓度为___;
(5)该样品中铝铵矾的质量分数为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,已知有机物A的相对分子质量是28,它的产量是衡量一个国家石油化工水平的标志,B和D都是日常生活食品中常见的有机物,F是一种高聚物,生活中用于制造食物保鲜膜。
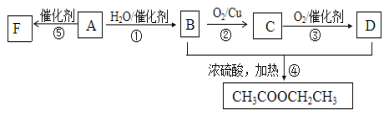
(1)请写出A的分子式:_____________。
(2)请写出下列反应的类型:④_____________,⑤_____________。
(3)请写出下列反应的化学方程式:
①_____________;⑤_____________;
(4)某实验小组用下列装置模拟上述反应②的转化过程。
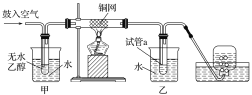
实验过程中铜网出现黑色和红色交替的现象。
①红色变成黑色的反应是2Cu+O2![]() 2CuO;
2CuO;
②黑色变为红色的化学方程式为____________________________________________。甲和乙两个水浴作用不相同,甲的作用是________(填“加热”或“冷却”);反应进行一段时间后,试管a中能收集到多种物质,它们是______(任写两种即可)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲、乙两烧杯中各盛有100 mL 3 mol·L-1的盐酸和氢氧化钠溶液,向两烧杯中分别加入等质量的铝粉,反应结束后生成的气体的体积比为甲∶乙=1∶2,则加入铝粉的质量为( )
A.5.4 gB.3.6 gC.2.7 gD.1.8 g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是部分短周期元素原子半径与原子序数的关系图。则下列说法正确的是
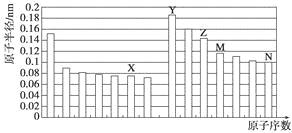
A. Z、N两种元素的离子半径相比,前者较大
B. X、N两种元素的气态氢化物的沸点相比,前者较低
C. 由X与M两种元素组成的化合物不能与任何酸反应,但能与强碱反应
D. Z的氧化物能分别溶解于Y的氢氧化物和N的氢化物的水溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚硝酸盐与钻形成的一种配合物1Co(NH3)5N02]C12的制备流程如下:
CoC12·6H20![]() [Co(NH3)5C1]C12
[Co(NH3)5C1]C12![]() [Co(NH3)5NO2]C12
[Co(NH3)5NO2]C12
(1)Co2+基态核外电子排布式为_______________。
(2)配合物[Co(NH3)5C1]C12中与Co3+形成配位键的原子为___________(填元素符号);配离子[Co(NH3)5N02]2+的配体中氮原子的杂化轨道类型为___________。
(3)与NO2-互为等电子体的单质分子为___________(写化学式)。
(4)H202与H20可以任意比例互溶,除因为它们都是极性分子外,还因为 _______________。
(5)亚硝酸盐在水体中可转化为强致癌物亚硝胺,亚硝胺NDMA的结构、简式如图所示,lmolNDMA分子中含有![]() 键的数目为______________mol.
键的数目为______________mol.
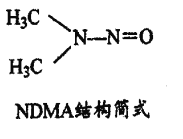
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对可逆反应4NH3(g)+5O2(g)![]() 4NO(g)+6H2O(g),下列叙述正确的是
4NO(g)+6H2O(g),下列叙述正确的是
A.达到化学平衡时,4v正(O2) = 5v逆(NO)
B.若单位时间内生成x mol NO的同时,消耗x mol NH3,则反应达到平衡状态
C.达到化学平衡时,若增加容器体积,则正反应速率减小,逆反应速率增大
D.化学反应速率关系是:2v正(NH3) = 3v正(H2O)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由硫铁矿“烧渣”(主要成分:Fe3O4、Fe2O3和FeO)制备绿矾(FeSO4·7H2O))的流程如图:

已知:FeS2(S的化合价为-1)难溶于水。
(1)①中加入的酸为___,滤渣2的主要成分是___。
(2)①中生成Fe3+的离子方程式为Fe3O4+8H+=2Fe3++Fe2++4H2O、___。
(3)检验②中Fe3+已经完全转化成Fe2+的实验方法:取适量溶液2,___。
(4)通过③得到绿矾晶体的实验操作:加热浓缩、冷却结晶、___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中国科学院科研团队研究表明,在常温常压和可见光下,基于LDH(一种固体催化剂)合成NH3的原理示意图如下。下列说法不正确的是( )
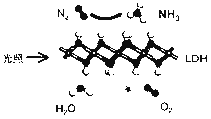
A. 该过程将太阳能转化成为化学能 B. 该过程中,涉及极性键与非极性键的断裂与生成
C. 氧化产物与还原产物的物质的量之比为3∶4 D. 该反应为放热反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com