
【题目】硼镁泥是硼镁矿生产硼砂晶体(Na2B4O7·10H2O)时的废渣,其主要成分是MgO,还含有Na2B4O7、CaO、Fe2O3、FeO、MnO、SiO2等杂质。以硼镁泥为原料制取七水硫酸镁的工艺流程如下:

回答下列问题:
(l)Na2B4O7·10H2O中B的化合价为__________。
(2)Na2B4O7易溶于水,也易发生水解:B4O72-+7H2O![]() 4H3BO3(硼酸)+2OH-(硼酸在常温下溶解度较小)。写出加入硫酸时Na2B4O7发生反应的化学方程式:______________。
4H3BO3(硼酸)+2OH-(硼酸在常温下溶解度较小)。写出加入硫酸时Na2B4O7发生反应的化学方程式:______________。
(3)滤渣B中含有不溶于稀盐酸但能溶于热浓盐酸的黑色固体,写出生成黑色固体的离子方程式____________。
(4)加入MgO的目的是___________________。
(5)已知MgSO4、CaSO4的溶解度如下表:
温度(℃) 溶解度(g) | 40 | 50 | 60 | 70 |
MgSO4 | 30.9 | 33.4 | 35.6 | 36.9 |
CaSO4 | 0.210 | 0.207 | 0.201 | 0.193 |
“操作A”是将MgSO4和CaSO4混合溶液中的CaSO4除去,根据上表数据,简要说明“操作A”步骤为____________________。
(6)硼砂也能在工业上制取NaBH4,NaBH4被称为有机化学中的“万能还原剂”。
①写出NaBH4的电子式:___________。
②“有效氢含量”可用来衡量含氢还原剂的还原能力,其定义是:每克含氢还原剂的还原能力相当于多少克H2的还原能力。NaBH4的有效氢含量为_________(保留两位小数)。
③在碱性条件下,在阴极上电解NaBO2也可制得硼氢化钠,写出阴极室的电极反应式:________。
【答案】 +3 Na2B4O7+H2SO4+5H2O=Na2SO4+4H3BO3↓ ClO- +Mn2++H2O=MnO2+Cl-+2H+ 调节溶液的pH值,使Fe3+转化为氢氧化铁沉淀除去 蒸发浓缩、趁热过滤 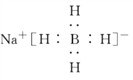 0.21 BO2-+6H2O+8e-=BH4-+8OH-
0.21 BO2-+6H2O+8e-=BH4-+8OH-
【解析】(1)设B的化合价为x价,根据化合物中各元素化合价代数和为零可得,![]() ,解得
,解得![]() ,所以
,所以![]() 中
中![]() 的化合价为+3价。
的化合价为+3价。
(2)Na2B4O7易溶于水,也易发生水解:B4O72-+7H2O![]() 4H3BO3(硼酸)+2OH-(硼酸在常温下溶解度较小)。加入硫酸时促进了B4O72-的水解,所以Na2B4O7与硫酸发生反应的化学方程式:Na2B4O7+H2SO4+5H2O=Na2SO4+4H3BO3↓。
4H3BO3(硼酸)+2OH-(硼酸在常温下溶解度较小)。加入硫酸时促进了B4O72-的水解,所以Na2B4O7与硫酸发生反应的化学方程式:Na2B4O7+H2SO4+5H2O=Na2SO4+4H3BO3↓。
(3)由硼镁泥的成分推断可知,不溶于稀盐酸但能溶于浓盐酸的黑色固体为![]() ,即
,即![]() 被
被![]() 氧化成
氧化成![]() ,则其反应离子方程式为
,则其反应离子方程式为![]() 。(4)
。(4)![]() 属于碱性氧化物,能够与溶液中的
属于碱性氧化物,能够与溶液中的![]() 反应,从而改变溶液的
反应,从而改变溶液的![]() 值,因此可通过改变
值,因此可通过改变![]() 加入量来调节溶液的
加入量来调节溶液的![]() ,达到使
,达到使![]() 以
以![]() 沉淀的形式除去的目的。
沉淀的形式除去的目的。
(5)因为CaSO4 微溶于水,MgSO4 易溶于水,“操作A”是将MgSO4和CaSO4混合溶液中的CaSO4除去,根据上表数据,操作A采用结晶的方法除去CaSO4,步骤为蒸发浓缩、趁热过滤。
(6)①写出NaBH4的电子式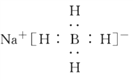
②![]() 中
中![]() 显-1价,
显-1价,![]() 中
中![]() 显0价,两者的还原产物均为
显0价,两者的还原产物均为![]() (
(![]() 显+1价),
显+1价),![]()
![]() 的可以失去
的可以失去![]() 电子,
电子,![]() 可以失去
可以失去![]() 电子,则
电子,则![]() 的
的![]() 的还原能力等价于
的还原能力等价于![]() 的
的![]() ,则根据“有效氢含量”的定义可知,
,则根据“有效氢含量”的定义可知,![]() 的有效氢含量为
的有效氢含量为![]() 。
。
③在NaBO2 中,B的化合价为+3,![]() 中B化合价为+5,在碱性条件下,在阴极上电解NaBO2,制硼氢化钠的电极反应式:BO2-+6H2O+8e-=BH4-+8OH-。答案为BO2-+6H2O+8e-=BH4-+8OH-。
中B化合价为+5,在碱性条件下,在阴极上电解NaBO2,制硼氢化钠的电极反应式:BO2-+6H2O+8e-=BH4-+8OH-。答案为BO2-+6H2O+8e-=BH4-+8OH-。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】下列离子方程式书写正确的是
A. 稀硝酸与铁屑反应:2Fe+6H+=2Fe3++3H2↑
B. 往NH4HCO3溶液中加过量的NaOH溶液并加热:NH4++OH-=NH3↑+H2O
C. 往酸性碘化钾溶液中滴加适量的双氧水:2I-+2H++H2O2=I2+2H2O
D. HS-的电离:HS-+H2O![]() OH-+HS-
OH-+HS-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列溶液中粒子的物质的量浓度关系正确的是( )
A. 0.1![]()
![]() 溶液与0.1
溶液与0.1![]()
![]() 溶液等体积混合,所得溶液中:
溶液等体积混合,所得溶液中:![]()
B. 20![]() 0.1
0.1![]()
![]() 溶液与10
溶液与10![]() 0.1
0.1![]()
![]() 溶液混合后溶液呈酸性,所得溶液中:
溶液混合后溶液呈酸性,所得溶液中:![]()
C. 室温下,![]() 的盐酸与
的盐酸与![]() 的氨水等体积混合,所得溶液中:
的氨水等体积混合,所得溶液中:![]()
D. 0.1![]()
![]() 溶液与0.1
溶液与0.1![]()
![]() 溶液等体积混合,所得溶液中:
溶液等体积混合,所得溶液中:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,向容积固定为a L的密闭容器中充入1 mol X气体和2 mol Y气体,发生反应X(g)+2Y(g) ![]() 2Z(g),此反应达到平衡状态的标志是( )
2Z(g),此反应达到平衡状态的标志是( )
A. 容器内气体密度不随时间变化 B. 容器内各物质的浓度不随时间变化
C. 容器内X、Y、Z的浓度之比为1∶2∶2 D. 单位时间内消耗0.1 mol X,同时生成0.2 mol Z
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生产生活、科技、环境等密切相关,下列说法正确的是:
A. 黑火药是我国古代四大发明之一,配方为“一硫二硝三木炭”,其中的硝是指硝酸
B. 可以用氢氧化钠鉴别地沟油和矿物油
C. 用漂白精和洁厕灵(主要成分是盐酸)混合后的浓溶液清洗马桶效果更好
D. 明矾可以用于海水提纯制淡水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)下列物质中,物质的量最大的是__________,含分子个数最多的是________,含原子个数最多的是_________,质量最大的是__________(填字母)。
A.6g氢气 B.0.5molCO2 C.1.204×1023个CO分子 D.147g H2SO4 E.92g乙醇(C2H5OH)
(2)NA表示阿伏加德罗常数的值
①1.204×1023个水分子中共________mol氢原子。
②某气体在同温同压下对H2相对密度为32,则该气体的相对分子质量为__________。
③某气体的质量是14.2g,体积是4.48L(标准状况),该气体的摩尔质量是___g/mol。
④25g CuSO4·5H2O晶体中含有氧原子______个。
⑤16gO2含有的氧分子数与______g CO2含有的氧原子数相等。
⑥标准状况下,11.2 L CH4中含有的氢原子数为________个。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,向一定体积0.1mol·![]() 的氨水中逐滴加入等浓度的盐酸,溶液中
的氨水中逐滴加入等浓度的盐酸,溶液中![]() 与pH的变化关系如下图所示。下列说法不正确的是
与pH的变化关系如下图所示。下列说法不正确的是

A. M点和N点溶液中![]() 的电离程度相同
的电离程度相同
B. Q点溶液中,![]()
C. M点溶液的导电性小于Q点溶液的导电性
D. N点溶液加水稀释,![]() 变小
变小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】恒温条件下,可逆反应:2NO(g)+O2(g) ![]() 2NO2(g)在体积固定的密闭容器中进行,达到平衡状态的标志的是
2NO2(g)在体积固定的密闭容器中进行,达到平衡状态的标志的是
①NO的体积分数不再改变的状态 ②单位时间内生成n mol O2的同时生成2n mol NO
③混合气体的颜色不再改变的状态 ④混合气体的密度不再改变的状态
⑤混合气体的平均相对分子质量不再改变的状态
A. ①③⑤ B. ②③⑤ C. ①④⑤ D. 全部
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钠硫电池作为一种新型储能电池,其应用逐渐得到重视和发展。钠硫电池以熔融金属钠、熔融硫和多硫化钠(Na2SX)分别作为两个电极的反应物,固体Al2O3陶瓷(可传导Na+)为电解质,其反应原理如图1所示:


(1)根据表数据,请你判断该电池工作的适宜应控制
在_____(填字母)范围内。
A.100℃以下 B.100~300℃
C.300~350℃ D.350~2050℃
物质 | Na | S | Al2O3 |
熔点/℃ | 97.8 | 115 | 2050 |
沸点/℃ | 892 | 444.6 | 2980 |
(2)放电时,电极A为_____极,电极B发生_____反应(填“氧化或还原”)。
(3)充电时,总反应为Na2Sx=2Na+xS,则阳极的电极反应式为:________________。
(4)若把钠硫电池作为电源,电解槽内装有KI及淀粉溶液如图2所示,槽内的中间用阴离子交换膜隔开。通电一段时间后,发现左侧溶液变蓝色,一段时间后,蓝色逐渐变浅。则右侧发生的电极方程式:________________;试分析左侧溶液蓝色逐渐变浅的可能原因是:___________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com