
 把一块镁铝合金投入到1mol/L 盐酸里,待合金完全溶解后,往溶液里加入1mol/L NaOH溶液,生成沉淀的物质的量随加入NaOH溶液体积变化的关系如下图所示.下列说法中不正确的是( )
把一块镁铝合金投入到1mol/L 盐酸里,待合金完全溶解后,往溶液里加入1mol/L NaOH溶液,生成沉淀的物质的量随加入NaOH溶液体积变化的关系如下图所示.下列说法中不正确的是( )| A. | 生成Al(OH)3沉淀的最大质量为0.78g | B. | 加入70ml NaOH 时溶液呈碱性 | ||
| C. | $\frac{n(Mg)}{n(Al)}$的最大值为1.5 | D. | a的取值范围为0≤a<45mL |
分析 根据图可知,首先发生反应:H++OH-=H2O,说明加入的NaOH过量;然后发生反应:Mg2++2OH-=Mg(OH)2↓、Al3++3OH-=Al(OH)3↓,最后是Al(OH)3的溶解:Al(OH)3+OH-=AlO2-+2H2O,从横坐标60mL到70mL这段可以求出n[Al(OH)3]=n(NaOH)=1mol/L×0.01L=0.01mol,则n(Al)=n[Al(OH)3]=0.01mol,所以Al3+消耗的NaOH溶液的体积为$\frac{0.01mol×3}{1mol/L}$=0.03L=30mL,据此进行解答.
解答 解:根据图可知,首先发生反应:H++OH-=H2O,说明加入的NaOH过量;然后发生反应:Mg2++2OH-=Mg(OH)2↓、Al3++3OH-=Al(OH)3↓,最后是Al(OH)3的溶解:Al(OH)3+OH-=AlO2-+2H2O,从横坐标60mL到70mL这段可以求出n[Al(OH)3]=n(NaOH)=1mol/L×0.01L=0.01mol,则n(Al)=n[Al(OH)3]=0.01mol,所以Al3+消耗的NaOH溶液的体积为$\frac{0.01mol×3}{1mol/L}$=0.03L=30mL,
A.根据分析可知,生成Al(OH)3沉淀的最大物质的量为0.01mol,最大质量为:78g/mol×0.01mol=0.78g,故A正确;
B.加入70mL NaOH 时,反应后溶质为NaCl和偏铝酸钠,偏铝酸根离子水解,溶液呈碱性,故B正确;
C.Mg消耗HNaOH溶液体积小于60mL-30mL=30mL,Mg的物质的量小于$\frac{1mol/L×0.03L}{2}$=0.015mol,则$\frac{n(Mg)}{n(Al)}$≤$\frac{0.15mol}{0.1mol}$=1.5,故C正确;
D.根据C可知,n(Mg)<0.015mol,当a=0.015mol时,a=0,当n(Mg)=0时,a<60mL-30mL=30mL,所以0≤a<30mL,故D错误;
故选D.
点评 本题考查镁铝及其化合物的性质、混合物计算,题目难度中等,明确图象曲线对应反应实质为关键,注意利用极限法进行解答,试题培养了学生的分析能力及化学计算能力.


科目:高中化学 来源:2017届宁夏高三上学期第三次月考化学试卷(解析版) 题型:选择题
我国有广阔的海岸线,建设海峡经济区,海水的综合利用大有可为,下图所示为海水综合利用部分流程,有关说法正确的是

A.上述工艺流程中涉及到化合、分解、复分解和置换反应
B.①只发生了化学变化,②是工业上用电解熔融NaCl制备Cl2
C.③④涉及的反应均为氧化还原反应,⑤只需要蒸馏即可得到单质Br2
D.④中反应的离子方程式为SO2+Br2+2H2O===4H++SO42-+2Br-
查看答案和解析>>
科目:高中化学 来源:2017届辽宁省高三上模拟一化学试卷(解析版) 题型:选择题
将一定量的SO2通入FeCl3溶液中,取混合溶液,分别进行下列实验,能证明SO2与FeCl3溶液发生氧化还原反应的是( )
操作 | 现象 | |
A | 加入NaOH溶液 | 有红褐色沉淀 |
B | 加入Ba(NO3)2溶液 | 有白色沉淀 |
C | 加入酸性KMnO4溶液 | 紫色褪去 |
D | 加入K3[Fe(CN)6](铁氰化钾)溶液 | 有蓝色沉淀 |
查看答案和解析>>
科目:高中化学 来源:2017届辽宁省高三上模拟一化学试卷(解析版) 题型:选择题
下列叙述错误的是( )
A.10mL质量分数为98%的H2SO4,用10mL水稀释后,H2SO4的质量分数大于49%
B.配制0.1mol/L的Na2CO3溶液480ml,需用500ml容量瓶
C.在标况下,将22.4L氨气溶于1L水中,得到1mol/L的氨水
D.向两等份不饱和的烧碱溶液中分别加入一定量的Na2O2和Na2O,使溶液均恰好饱和,则加入的Na2O2与Na2O的物质的量之比等于1:1(保持温度不变)
查看答案和解析>>
科目:高中化学 来源:2017届辽宁省高三上模拟二化学试卷(解析版) 题型:选择题
下列有关叙述正确的是( )
A.“歼﹣20”飞机上大量使用的碳纤维是一种新型的有机高分子材料
B.铝合金的大量使用是因为人们能用氢气等还原剂从氧化铝中获取铝
C.酸碱指示剂变色、煤的液化、海水提溴、皂化反应都涉及化学变化
D.金属镁着火可使用干粉灭火器灭火,但不可用泡沫灭火器灭火
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 如图是银锌原电池装置的示意图,以硫酸铜为电解质溶液.回答下列问题:
如图是银锌原电池装置的示意图,以硫酸铜为电解质溶液.回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 +3Br2→
+3Br2→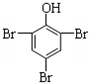 ↓+3HBr;反应类型取代反应.
↓+3HBr;反应类型取代反应. ;反应类型取代反应.
;反应类型取代反应. ;反应类型加聚反应.
;反应类型加聚反应.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子序数:X>W>Y>Z | B. | 原子半径:W>X>Z>Y | ||
| C. | 氧化性:X+>W3+ | D. | 氢化物稳定性:HZ>H2Y |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com