
【题目】能源是国民经济发展的重要基础,我国目前使用的能源主要是化石燃料.
(1)在25℃、101kPa时,16g CH4完全燃烧生成液态水时放出的热量是890.31kJ,则CH4燃烧的热化学方程式是 .
(2)已知:
C(s)+O2(g)═CO2(g);△H=﹣437.3kJmol﹣1
H2(g)+ ![]() O2(g)═H2O(g);△H=﹣285.8kJmol﹣1
O2(g)═H2O(g);△H=﹣285.8kJmol﹣1
CO(g)+ ![]() O2(g)═CO2(g);△H=﹣283.0kJmol﹣1
O2(g)═CO2(g);△H=﹣283.0kJmol﹣1
则煤的气化主要反应的热化学方程式是:C(s)+H2O(g)═CO(g)+H2(g);△H=kJmol﹣1 , 该反应是(填“吸热”或者“放热”)反应,此法相比于传统的直接将煤中提取的C燃烧,你觉得可能的优点是什么? .
【答案】
(1)CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=﹣890.31kJ/mol
(2)+131.5;吸热;固体煤经处理变成气体燃料后,不仅可以大大减少SO2和烟尘对空气造成的污染,而且燃烧效率高,也便于运输
【解析】解:(1)16g即1molCH4在氧气中燃烧生成CO2和液态水,放出889kJ热量,则热化学方程式为:CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=﹣890.31KJ/mol,所以答案是:CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=﹣890.31KJ/mol;(2)①C(s)+O2(g)═CO2(g)△H1=﹣437.3kJmol﹣1②H2(g)+ ![]() O2(g)═H2O(g)△H3=﹣285.8kJmol﹣1③CO(g)+
O2(g)═H2O(g)△H3=﹣285.8kJmol﹣1③CO(g)+ ![]() O2(g)═CO2(g)△H=﹣283.0kJmol﹣1
O2(g)═CO2(g)△H=﹣283.0kJmol﹣1
依据盖斯定律①﹣②﹣③,得到:C(s)+H2O(g)═CO(g)+H2(g) n△H=+131.5kJmol﹣1 , 反应为吸热反应,此法是煤的气化,相比于传统的直接将煤中提取的C燃烧可以减少污染气体的排放,增大燃烧效率,便于运输和储存,所以答案是:+131.5;吸热;固体煤经处理变成气体燃料后,不仅可以大大减少SO2和烟尘对空气造成的污染,而且燃烧效率高,也便于运输.


科目:高中化学 来源: 题型:
【题目】欲用98%的浓硫酸(ρ=1.84g/mL)配制浓度为0.5molL﹣1的稀硫酸500mL.
(1)选用的主要仪器有:量筒,烧杯,玻璃棒,试剂瓶,还缺少仪器的名称是;
(2)请将下列各操作,按正确的操作顺序序号填在横线上;
A.用量筒量取浓H2SO4
B.反复颠倒摇匀
C.用胶头滴管加蒸馏水至环形刻度线
D.稀释浓H2SO4
E.将溶液冷却至室温后转入容量瓶
(3)简要回答下列问题:
①所需浓硫酸的体积为mL;
②如果实验室有15mL、20mL、50mL规格的量筒,应选用mL的量筒最好,量取时发现量筒不干净用水洗净后直接量取将使浓度(“偏高”、“偏低”、“无影响”).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为实验室某浓盐酸试剂瓶标签上的有关数据,试根据标签上的有关数据
回答下列问题: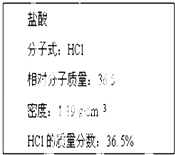
(1)该浓盐酸中HCl的物质的量浓度为 .
(2)取用任意体积的该盐酸溶液时,下列物理量中不随所取体积的多少而变化的是 .
A.溶液中HCl的物质的量
B.溶液的浓度
C.溶液中Cl﹣的数目
D.溶液的密度
(3)某学生欲用上述浓盐酸和蒸馏水配制500mL物质的量浓度为0.4000molL﹣1的稀盐酸.
可供选用的仪器有:①胶头滴管;②玻璃棒;③烧杯;④药匙;⑤量筒;⑥托盘天平.
请回答下列问题:
①配制稀盐酸时,还缺少的仪器有(写仪器名称);该仪器上标有以下五项中的;
A.温度 B.浓度 C.容量 D.压强 E.刻度线
②该学生需要量取mL上述浓盐酸进行配制.
③在配制过程中,下列实验操作对所配制的稀盐酸的物质的量浓度有何影响?
(在括号内填A表示“偏大”、填B表示“偏小”、填C表示“无影响”).
a.用量筒量取浓盐酸时俯视观察凹液面.
b.量筒量取浓盐酸后有用蒸馏水洗涤2~3次,并将洗液移入容量瓶中.
(4)①假设该同学成功配制了0.400molL﹣1的盐酸,他又用该盐酸中和含0.4gNaOH的NaOH溶液,则该同学需取mL盐酸.②假设该同学用新配制的盐酸中和含0.4gNaOH的NaOH溶液,发现比①中所求体积偏小,则可能的原因是 .
A.浓盐酸挥发,浓度不足
B.配制溶液时,未洗涤烧杯
C.配制溶液时,俯视容量瓶刻度线
D.加水时超过刻度线,用胶头滴管吸出.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组用如图装置制备家用消毒液,并探究其性质.
(1)写出装有浓盐酸的仪器名称 , A中烧瓶内进行的反应中浓盐酸体现出的化学性质是
(2)写出装置B中发生的所有反应化学方程式
(3)装置c的作用是
反应停止后,各取洗气瓶中无色溶液5mL分别进行了如下实验:
操作 | 现象 |
A.测溶液pH,并向其中滴加2滴酚酞 | pH=13,溶液变红,5min后褪色 |
B. 向其中逐滴加入盐酸 | 溶液逐渐变成黄绿色 |
(4)查阅资料:酚酞的变色范围为8.2~10,且酚酞在强碱性溶液中红色会褪去
为探究操作A中溶液褪色的原因,又补充了如下实验:
操作 | 现象 |
取 NaOH溶液,向其中滴加2滴酚酞 | 溶液变红,30min后褪色 |
获得结论:此实验小组制备的消毒液具有漂白性.
(5)操作B中溶液变成黄绿色的原因:(用离子方程式表示).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一密闭容器中发生反应N2+3H22NH3 , △H<0,达到平衡后,只改变某一个条件时,反应速率与反应时间的关系如图1所示: 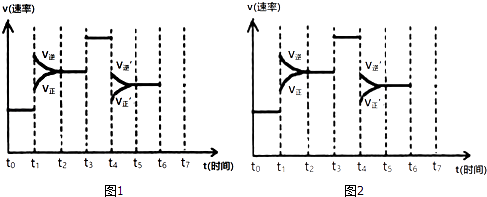
回答下列问题:
(1)处于平衡状态的时间段是(填选项).
A.t0~t1
B.t1~t2
C.t2~t3
D.t3~t4
E.t4~t5
F.t5~t6
(2)t1、t3、t4时刻分别改变的一个条件是:t1时刻;t3时刻;t4时刻 . (填选项).
A.增大压强 B.减小压强 C.升高温度
D.降低温度 E.加催化剂 F.充入氮气
(3)依据(2)中结论,下列时间段中,氨的百分含量最高的是(填选项).
A.t0~t1
B.t2~t3
C.t3~t4
D.t5~t6
(4)一定条件下,合成氨反应达到平衡时,若将密闭容器体积缩小一半,则对反应产生的影响是(填选项).
A.正反应速率减小,逆反应速率增大
B.正反应速率增大,逆反应速率减小
C.正、逆反应速率都减小
D.正、逆反应速率都增大
(5)如果在t6时刻,从反应体系中分离出部分氨,t7时刻反应达到平衡状态,请在图2中画出反应速率的变化曲线.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将a克Fe2O3 、Al2O3 样品溶解在过量的200mL c(H+)=0.1molL﹣1 的硫酸溶液中,然后向其中加入NaOH溶液使Fe3+、Al3+ 刚好完全沉淀,用去NaOH溶液100mL,则NaOH 溶液的浓度为( )
A.0.1 molL﹣1
B.0.2 molL﹣1
C.0.4 molL﹣1
D.0.8 molL﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知pH=-lgc(H+),标准状况下,某同学向100 mL H2S饱和溶液中通入SO2 , 所得溶液pH变化如图所示,下列分析中,正确的是( )
A.ab段反应是:SO2+2H2S=3S↓+2H2O
B.亚硫酸是比氢硫酸更弱的酸
C.原H2S溶液的物质的量浓度为0.05mol/L
D.b点对应的溶液导电性最强
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com