
���� ��1����ҵұ��������ԭ����ӦΪFe2O3+3CO$\frac{\underline{\;����\;}}{\;}$2Fe+3CO2�����ݷ�Ӧ�����������������ɼ���μӷ�Ӧ����������������
��2��4.80g�����������ʵ���Ϊ��$\frac{4.80g}{160g/mol}$=0.03mol��4.80g���������������������4.56gʱ�������������ʵ���Ϊ$\frac{4.80g-4.56g}{16g/mol}$=0.015�������������������������ʵ���Ϊ��0.03��3-0.015=0.075mol�������������ʵ���֮��Ϊ��0.03��2��0.075=1��1.25����Fe3O4�������������ʵ���֮��Ϊ��1��1.33����FeO�������������ʵ���֮��Ϊ��1��1����Fe2O3�������������ʵ���֮��Ϊ��1��1.5�����Թ������������Fe2O3��FeO��Fe3O4��FeO��Ȼ������Ե����ʵ�����
��3����1��������Ũ���ᷴӦ���ɵ���ȫΪ�������������ݷ�ӦC+4HNO3��Ũ��$\frac{\underline{\;\;��\;\;}}{\;}$CO2��+4NO2��+2H20��Fe+6HNO3��Ũ��$\frac{\underline{\;\;��\;\;}}{\;}$Fe��NO3��3+3NO2��+3H2O��֪����CΪ0ʱ��������������٣���10g����ȫ��Ӧ���ɶ������������ʵ���Ϊ��$\frac{10g}{56g/mol}$��3��0.536mol��0.300mol�������������ᷴӦ���ɵ�����ΪNO��NO2�Ļ����ٸ���������50.00mL 12.00mol/L��NaOH��Һ����������ԶԶ��������ȫ���պ�ֻ���������ο�֪�����ɵ���Ϊ̼���ƺ��������ƣ�˵�����ɵ�NO��NO2�����ʵ�����ȣ���NO��NO2�����ʵ�����Ϊx����̼�ظ��к���CΪy�����ݷ�ӦC+4HNO3��Ũ��$\frac{\underline{\;\;��\;\;}}{\;}$CO2��+4NO2��+2H20��֪��ymolC��Ũ���ᷴӦ����ymol������̼��4ymol��������������Ũ���ᷴӦ���ɵĶ�������Ϊ��x-4y�����ݷ�ӦFe+6HNO3��Ũ��$\frac{\underline{\;\;��\;\;}}{\;}$Fe��NO3��3+3NO2��+3H2O��Fe+4HNO3$\frac{\underline{\;\;��\;\;}}{\;}$Fe��NO3��3+NO��+2H2O��֪���ø��к����������ʵ���Ϊ��$\frac{3}{2}$x+$\frac{1}{3}$��x-4y�������ݸøֵ������ɵã���[x+$\frac{1}{3}$��x-4y��]��56+12y=10.00���ٸ�������������ʵ����ɵã���y+2x=0.3�������٢ڼ����x��y���ټ�����ø����ĺ�̼����
��2�����ݣ�1������������ӦC+4HNO3��Ũ��$\frac{\underline{\;\;��\;\;}}{\;}$CO2��+4NO2��+2H20��Fe+6HNO3��Ũ��$\frac{\underline{\;\;��\;\;}}{\;}$Fe��NO3��3+3NO2��+3H2O��Fe+4HNO3$\frac{\underline{\;\;��\;\;}}{\;}$Fe��NO3��3+NO��+2H2O�������Ӧ����������������ʵ�����
��� �⣺��1������Ҫ�����������Ϊx
Fe2O3+3CO$\frac{\underline{\;����\;}}{\;}$ 2Fe+3CO2
160 112
x��70% 1t��96%
$\frac{160}{x��70%}=\frac{112}{1t��96%}$����֮�ã�x=1.96t
��������Ҫ70%�ij�����1.96��Fe2O3��FeO 1��2��
��2��4.80g�����������ʵ���Ϊ��$\frac{4.80g}{160g/mol}$=0.03mol��4.80g���������������������4.56gʱ�������������ʵ���Ϊ$\frac{4.80g-4.56g}{16g/mol}$=0.015�������������������������ʵ���Ϊ��0.03��3-0.015=0.075mol�������������ʵ���֮��Ϊ��0.03��2��0.075=1��1.25����Fe3O4�������������ʵ���֮��Ϊ��1��1.33����FeO�������������ʵ���֮��Ϊ��1��1����Fe2O3�������������ʵ���֮��Ϊ��1��1.5�����Թ������������Fe2O3��FeO��Fe3O4��FeO�������Fe2O3��FeO�Ļ��������ߵ����ʵ����ֱ�Ϊ��xmol��ymol����$\frac{1.5x+y}{x+y}=1.25$����֮��$\frac{x}{y}=\frac{1}{2}$�������Fe3O4��FeO�Ļ�������������ʵ���֮��Ϊ��1��1����Fe2O3��FeO�Ļ�������֮��Ϊ1��2������Fe3O4��FeO�Ļ����������ʵ���֮��Ϊ��1��1��
��3����1��������Ũ���ᷴӦ���ɵ���ȫΪ�������������ݷ�ӦC+4HNO3��Ũ��$\frac{\underline{\;\;��\;\;}}{\;}$CO2��+4NO2��+2H20��Fe+6HNO3��Ũ��$\frac{\underline{\;\;��\;\;}}{\;}$Fe��NO3��3+3NO2��+3H2O��֪����CΪ0ʱ��������������٣���10g����ȫ��Ӧ���ɶ������������ʵ���Ϊ��$\frac{10g}{56g/mol}$��3��0.536mol��0.300mol�������������ᷴӦ���ɵ�����ΪNO��NO2�Ļ����ٸ���������50.00mL 12.00mol/L��NaOH��Һ����������ԶԶ��������ȫ���պ�ֻ���������ο�֪�����ɵ���Ϊ̼���ƺ��������ƣ�˵�����ɵ�NO��NO2�����ʵ�����ȣ���NO��NO2�����ʵ�����Ϊx����̼�ظ��к���CΪy��
���ݷ�ӦC+4HNO3��Ũ��$\frac{\underline{\;\;��\;\;}}{\;}$CO2��+4NO2��+2H20��֪��ymolC��Ũ���ᷴӦ����ymol������̼��4ymol����������
����Ũ���ᷴӦ���ɵĶ�������Ϊ��x-4y�����ݷ�ӦFe+6HNO3��Ũ��$\frac{\underline{\;\;��\;\;}}{\;}$Fe��NO3��3+3NO2��+3H2O��Fe+4HNO3$\frac{\underline{\;\;��\;\;}}{\;}$Fe��NO3��3+NO��+2H2O��֪���ø��к����������ʵ���Ϊ��$\frac{3}{2}$x+$\frac{1}{3}$��x-4y�������ݸøֵ������ɵã���[x+$\frac{1}{3}$��x-4y��]��56+12y=10.00���ٸ�������������ʵ����ɵã���y+2x=0.3�������٢ڽ�ã�x=0.144mol��y=0.012mol��
�����ø��к���0.012molC���京̼��Ϊ��$\frac{12g/mol��0.012mol}{10.00g}$��100%=1.44%��
�𣺸ø����ĺ�̼��Ϊ1.44%��
��2��0.012molC������������ʵ���Ϊ��0.012mol��4=0.048mol��
����0.144molNO������������ʵ���Ϊ��0.144mol��4=0.576mol��
����Ũ���ᷴӦ���ɶ������������ʵ���Ϊ��0.144mol-0.012mol��4=0.096mol����Ӧ����0.096mol��������������������ʵ���Ϊ��0.096mol��$\frac{6}{3}$=0.192mol��
���Է�Ӧ����������������ʵ���Ϊ��0.048mol+0.576mol+0.192mol=0.816mol��
�𣺲μӷ�Ӧ����������ʵ���Ϊ0.816mol��
���� ���⿼��ʹ�û�ѧ����ʽ���м���ͻ���ﷴӦ�ļ��㣬��Ŀ�ѶȽϴ�ѧ��ע����뻯ѧ����ʽ����һ���Ǵ���������������ܰѻ���������ֱ�Ӵ��뻯ѧ����ʽ���м��㣬����������Ŀ����������������������������жϷ�Ӧ������ɼ����ɹ�������Ϊ���ؼ���ע����ȷһ����������������������������Һ�ķ�Ӧԭ����������ؿ���ѧ���ķ���������������


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����ʱ��NaHA��ҺpH��7��������HA-�ĵ���̶ȴ�����ˮ��̶� | |
| B�� | ��0.1 mol/L��Na2A��Һ�У�c��A2-��+c��HA-��+c��H2A��=0.1 mol/L | |
| C�� | ��0.1 mol/L��NaHA��Һ�У�һ���У�c��Na+����c��HA-����c��H+����c��A2-����c��OH-�� | |
| D�� | �����ݵ����NaHA��Na2A��Ũ�ȱ�Ϊ1��1�Ļ����Һ�зֱ�����ʵ�Ũ�ȵ��������������ƣ���pH������ᡢ�����ı仯ͼ��Ϊ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
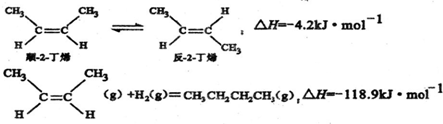
| A�� | ��-2-��ϩ��˳-2-��ϩ�ȶ� | |
| B�� | ˳-2-��ϩ��ȼ������ֵ�ȷ�-2-��ϩС | |
| C�� | ��ѹ������������ƽ�������������鷴Ӧ�����ƶ� | |
| D�� | ��-2-��ϩ�⻯���Ȼ�ѧ����ʽΪ��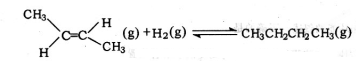 ��H=-123.1kJ•mol-1 ��H=-123.1kJ•mol-1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
 �ס��ҡ����������ʾ�������Ԫ�أ�����Һ�е�ת����ϵ��ͼ��ʾ������˵����ȷ���ǣ�������
�ס��ҡ����������ʾ�������Ԫ�أ�����Һ�е�ת����ϵ��ͼ��ʾ������˵����ȷ���ǣ�������| A�� | ������Al������Al��NO3��3������һ����NaAlO2 | |
| B�� | ������Al2O3������NaAlO2������һ����Al��NO3��3 | |
| C�� | ������Al��NO3��3������NaAlO2������һ����Al��OH��3 | |
| D�� | ������Al��OH��3������Al��NO3��3������һ����NaAlO2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
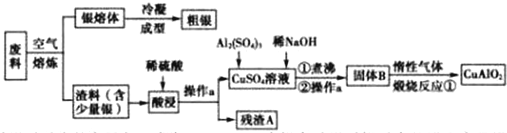
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
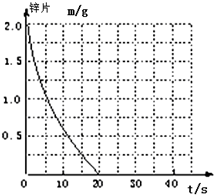 ��ȤС��̽��пƬ�����ᡢ���ᷴӦʱ��Ũ�Ȼ��¶ȶԷ�Ӧ���ʵ�Ӱ�죬�����������»�ѧ��Ʒ��0.20mol/L��0.40mol/L��HCl��Һ��0.2mol/L��0.40mol/L��CH3COOH��Һ��0.10mol/L CuCl2��пƬ����״����С��������ͬ���������̼�������ߡ��ձ�����֧�Թܺͽ�ͷ�ιܣ���Һ�¶ȿ���Ϊ298K��308K��
��ȤС��̽��пƬ�����ᡢ���ᷴӦʱ��Ũ�Ȼ��¶ȶԷ�Ӧ���ʵ�Ӱ�죬�����������»�ѧ��Ʒ��0.20mol/L��0.40mol/L��HCl��Һ��0.2mol/L��0.40mol/L��CH3COOH��Һ��0.10mol/L CuCl2��пƬ����״����С��������ͬ���������̼�������ߡ��ձ�����֧�Թܺͽ�ͷ�ιܣ���Һ�¶ȿ���Ϊ298K��308K��| ʵ���� | �¶ȣ�K�� | ����Ũ�� | ����Ũ�� | ʵ��Ŀ�� |
| �� | 298 | 0.20mol/L | / | a��ʵ��ٺ͢���̽����ͬ�¶ȶ�п�����ᷴӦ���ʵ�Ӱ�죻 b��ʵ��ٺ͢���̽����ͬŨ�ȶ�п�����ᷴӦ���ʵ�Ӱ�죻 c��ʵ��ٺ͢���̽����ͬ�¶��£���ͬŨ�ȵ����ᡢ������п��Ӧ���ʵ����� |
| �� | 308 | 0.20mol/L | / | |
| �� | 298 | 0.40mol/L | / | |
| �� | 298 | / | 0.20 |
| ʵ�鲽�� | Ԥ������ |
| �ٽ������ӵ�ͭ��п�缫����ϡ�����У��ڽ�ͭ��п�缫�õ������ӷ���ϡ������ | �������������ʢڴ��ڢ٣�֤������ԭ��غ���Դ��ӿ췴Ӧ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
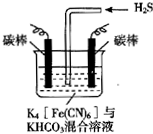 [Fe��CN��6]3-�ɽ���̬�������е�����ת��Ϊ�����õ���������ԭΪ[Fe��CN��6]4-����ҵ�ϳ�������ͼ��ʾ�ĵ��װ�ã�ͨ���⣬Ȼ��ͨ��H2S���Դ���������˵������ȷ���ǣ�������
[Fe��CN��6]3-�ɽ���̬�������е�����ת��Ϊ�����õ���������ԭΪ[Fe��CN��6]4-����ҵ�ϳ�������ͼ��ʾ�ĵ��װ�ã�ͨ���⣬Ȼ��ͨ��H2S���Դ���������˵������ȷ���ǣ�������| A�� | ���ʱ������ӦʽΪ[Fe��CN��6]4--e-�T[Fe��CN��6]3- | |
| B�� | ���ʱ������ӦʽΪ2HCO3-+2 e-�TH2��+2CO32- | |
| C�� | ������������22.4L��״���µ�H2����ʱ����Һ����32gS�������ܽ���Բ��ƣ� | |
| D�� | ������������Ҫ���ϲ���K4[Fe��CN��6]��KHCO3 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com