
| A£® | 8ÖÖ | B£® | 6ÖÖ | C£® | 4ÖÖ | D£® | 3ÖÖ |
·ÖĪö ij±„ŗĶõ„AŌŚĖįŠŌĢõ¼žĻĀĖ®½āµĆµ½ōČĖįBŗĶ“¼C£¬BÓėCµÄ·Ö×ÓŹ½·Ö±šĪŖC5HxOyŗĶC3H8O£¬ŅŃÖŖĖüĆĒµÄĻą¶Ō·Ö×ÓÖŹĮæµÄ¹ŲĻµŹ½ĪŖ£ŗM£ØA£©+36=M£ØB£©+2M£ØC£©£¬ĖµĆ÷ōČĖįĪŖ±„ŗĶ¶žŌŖĖį£¬·Ö×ÓŹ½ĪŖC5H8O4£¬½į¹¹¼ņŹ½ÓŠ4ÖÖ£ŗ£ØHOOC£©2CHCH2CH2COOH”¢HOOCCH2CHCOOHCH3”¢HOOCCH2CH2CH2COOH”¢CH3C£ØCOOH£©2CH3£»±ū“¼£ØC3H8O£©½į¹¹¼ņŹ½ÓŠ2ÖÖ£ŗ£ØCH3CH2CH2OH”¢CH3CHOHCH3£¬ŅŌ“ĖÅŠ¶ĻŠĪ³ÉµÄõ„µÄĶ¬·ÖŅģ¹¹ĢåµÄÖÖĄą£®
½ā“š ½ā£ŗij±„ŗĶõ„AŌŚĖįŠŌĢõ¼žĻĀĖ®½āµĆµ½ōČĖįBŗĶ“¼C£¬BÓėCµÄ·Ö×ÓŹ½·Ö±šĪŖC5HxOyŗĶC3H8O£¬ŅŃÖŖĖüĆĒµÄĻą¶Ō·Ö×ÓÖŹĮæµÄ¹ŲĻµŹ½ĪŖ£ŗM£ØA£©+36=M£ØB£©+2M£ØC£©£¬ĖµĆ÷ōČĖįĪŖ±„ŗĶ¶žŌŖĖį£¬·Ö×ÓŹ½ĪŖC5H8O4£¬½į¹¹¼ņŹ½ÓŠ4ÖÖ£ŗ£ØHOOC£©2CHCH2CH2COOH”¢HOOCCH2CHCOOHCH3”¢HOOCCH2CH2CH2COOH”¢CH3C£ØCOOH£©2CH3£»±ū“¼£ØC3H8O£©½į¹¹¼ņŹ½ÓŠ2ÖÖ£ŗ£ØCH3CH2CH2OH”¢CH3CHOHCH3£¬Ä³±„ŗĶõ„AµÄæÉÄܽį¹¹ÓŠ4”Į2=8£¬¹ŹŃ”A£®
µćĘĄ ±¾Ģāæ¼²éĶ¬·ÖŅģ¹¹ĢåŹżÄæµÄÅŠ¶Ļ£¬ĢāÄæÄѶČÖŠµČ£¬Ć÷Č·“¼µÄÖÖĄąÓėōČĖįµÄÖÖĄąŹĒ½āĢāµÄ¹Ų¼ü£¬×¢ŅāÕĘĪÕĶ¬·ÖŅģ¹¹ĢåµÄŹéŠ“ŌŌņ£®


 ĢģĢģĻņÉĻŅ»±¾ŗĆ¾ķĻµĮŠ“š°ø
ĢģĢģĻņÉĻŅ»±¾ŗĆ¾ķĻµĮŠ“š°ø Š”ѧɜ10·ÖÖÓÓ¦ÓĆĢāĻµĮŠ“š°ø
Š”ѧɜ10·ÖÖÓÓ¦ÓĆĢāĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
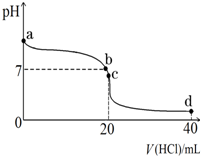 ŹµŃéŹŅÖŠÓŠŅ»Ī“ÖŖÅØ¶ČµÄĻ”ŃĪĖį£¬Ä³Ń§ÉśĪŖ²ā¶ØŃĪĖįµÄÅضČŌŚŹµŃéŹŅÖŠ½ųŠŠČēĻĀŹµŃé£ŗĒėĶź³ÉĻĀĮŠĢīæÕ£ŗ
ŹµŃéŹŅÖŠÓŠŅ»Ī“ÖŖÅØ¶ČµÄĻ”ŃĪĖį£¬Ä³Ń§ÉśĪŖ²ā¶ØŃĪĖįµÄÅضČŌŚŹµŃéŹŅÖŠ½ųŠŠČēĻĀŹµŃé£ŗĒėĶź³ÉĻĀĮŠĢīæÕ£ŗ| ŹµŃ鱹ŗÅ | NaOHČÜŅŗµĪČėµÄĢå»ż£ØmL£© | “ż²āŃĪĖįČÜŅŗµÄĢå»ż£ØmL£© |
| 1 | 22.62 | 20.00 |
| 2 | 22.72 | 20.00 |
| 3 | 22.80 | 20.00 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 1 L 1 mol•L-1µÄNaClO ČÜŅŗÖŠŗ¬ÓŠClO-µÄŹżÄæĪŖNA | |
| B£® | ³£ĪĀ³£Ń¹ĻĀ£¬4.6gCH3CH2OHÖŠŗ¬ÓŠ 6NAøöC-H¼ü | |
| C£® | ³£ĪĀ³£Ń¹ĻĀ£¬14 g ÓÉN2ÓėCO×é³ÉµÄ»ģŗĻĘųĢåŗ¬ÓŠµÄŌ×ÓŹżÄæĪŖNA | |
| D£® | ±ź×¼×“æöĻĀ£¬6.72 L NO2ÓėĖ®³ä·Ö·“Ó¦×ŖŅʵĵē×ÓŹżÄæĪŖ0.1NA |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
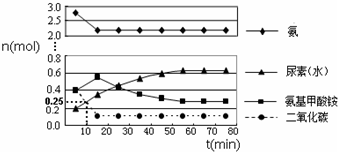
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
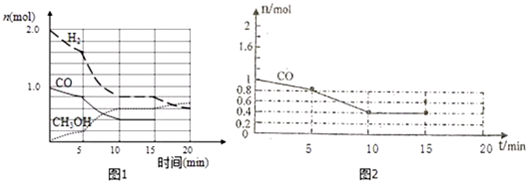
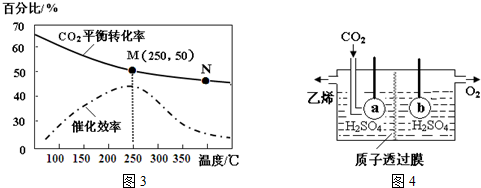
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ½«2mol SO3ĘųĢåĶØČėŅ»¶ØĆܱÕČŻĘ÷ÖŠ£¬·“Ó¦“ļµ½Ę½ŗāŗóĪüŹÕQ kJČČĮ棬ŌņøĆ·“Ó¦µÄČČ»Æѧ·½³ĢŹ½ĪŖ 2SO3£Øg£©?2SO2£Øg£©+O2£Øg£©”÷H=+Q kJ•mol-1 | |
| B£® | Ļņ0.1mol/L”¢pH=1µÄNaHAČÜŅŗÖŠ¼ÓČėNaOHČÜŅŗ£ŗH++OH-=H2O | |
| C£® | ŅŌ½šŹōŅųĪŖŃō¼«µē½ā±„ŗĶĮņĖįĶČÜŅŗ£ŗCu2++2H2O=2Cu+O2”ü+4H+ | |
| D£® | NH4Al£ØSO4£©2ČÜŅŗÖŠ¼ÓČėBa£ØOH£©2ČÜŅŗŹ¹SO42-ĶźČ«³Įµķ£ŗAl3++2SO42-+2Ba2++4OH-=AlO2-+2BaSO4”ż+2H2O |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
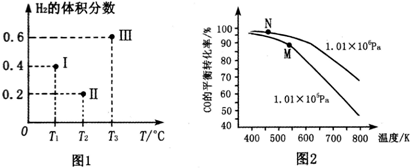
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ŹÆ»ŅŹÆæÉÓĆÓŚĮ¶Ģś”¢ÖĘĖ®Äą”¢ÖĘ²£Į§ | |
| B£® | Ź¹ÓƱ½“śĢę¾Ę¾«²ĮŹĆŹÖ»śĘĮÄ» | |
| C£® | Ķ¬Ī»ĖŲŹ¾×Ł·Ø”¢ŗģĶā¹āĘ׷ض¼ŹĒæĘѧ¼Ņ¾³£Ź¹ÓƵÄŃŠ¾æ»Æѧ·“Ó¦Ąś³ĢµÄŹÖ¶ĪÖ®Ņ» | |
| D£® | Õė¶ŌH7N9ĒŻĮ÷øŠµÄĄ©É¢Ēéæö£¬ŅŖ¼ÓĒæ»·¾³”¢øöČĖµČµÄĻū¶¾Ō¤·Ą£¬æÉŃ”ÓĆŗ¬ĀČĻū¶¾¼Į”¢¾Ę¾«”¢Ė«ŃõĖ®µČ×÷ĪŖĻū¶¾¼Į£¬ÕāÖÖ“¦Ąķ·½·Ø·ūŗĻĀĢÉ«»ÆѧµÄŗĖŠÄ |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com