
【题目】NaHSO4溶于水时和熔融态下电离方式有所不同,向NaHSO4溶液中分别加入下列物质,有气体生成的是( )
A.NaHCO3B.Ba(OH)2C.BaCl2D.CuO
 快乐小博士巩固与提高系列答案
快乐小博士巩固与提高系列答案科目:高中化学 来源: 题型:
【题目】下列关于烃的说法中正确的是
A. 烷烃不能发生加成反应,烯烃不能发生取代反应
B. 烷烃中含饱和键,烯烃、炔烃中含不饱和键
C. 能发生加成反应的一定是烯烃
D. 符合通式CnHn+2的一定是烷烃,符合通式CnH2n的一定是烯烃
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁是应用最广泛的金属,铁的卤化物、氧化物以及高价铁的含氧酸盐均为重要的化合物.
(1)要确定铁的某氯化物FeClx的化学式,可用离子交换和滴定的方法.实验中称取0.54g的FeClx样品,溶解后先进行阳离子交换预处理,再通过含有饱和OH﹣的阴离子交换柱,使Cl﹣和OH﹣发生交换.交换完成后,流出溶液的OH﹣用0.40mol/L的盐酸滴定,滴至终点时消耗盐酸25.00mL.则样品中氯的物质的量为________,x=________;
(2)现有一含有FeCl2和FeCl3的混合物样品,采用上述方法测得n(Fe):n(Cl)=1:2.1,则样品中FeCl3的物质的量分数为________.实验中,FeCl2可用铁粉与_________反应制得,FeCl3可用铁粉与________反应制得;
(3)氧化铁与氢碘酸反应的离子方程式为________;
(4)高铁酸钾(K2FeO4)是一种强氧化剂,可作为水处理剂和高容量电池材料.FeCl3与KClO在强碱性溶液中反应制取(K2FeO4),其反应的离子方程式为 ________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】两种气态烃组成的混合气体0.1 mol,完全燃烧得0.16 mol CO2和3.6 g H2O,下列说法正确的是
A. 混合气体中一定有甲烷 B. 混合气体一定是甲烷和乙烯
C. 混合气体中可能有乙炔 D. 混合气体中一定有乙炔
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如下图是从元素周期表中截取下来的,甲、乙、丙为短周期主族元素,下列说法中正确的是( )
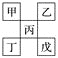
A. 丁一定是金属元素,其金属性比丙强
B. 丙的最高价氧化物水化物显强酸性
C. 乙的氢化物是以分子形式存在,且分子间存在氢键
D. 戊的原子序数一定是甲的5倍,且原子半径比甲大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子在水溶液中能大量共存的是( )
A.K+、HCO3﹣、CO32﹣、Br﹣
B.SO32﹣、HSO3﹣、OH﹣、K+
C.Fe3+、Cu2+、NO3﹣、SO32﹣
D.H+、Na+、NO3﹣、Fe2+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将红热的固体单质M放入浓硝酸中,剧烈反应,产生混合气体A,A在常温下不与空气接触时,发生如图所示的变化。

(1)混合气体A的主要成分是____________。
(2)气体B为__________,蓝色溶液D为____________。
(3)单质M与浓硝酸反应的化学方程式是____________________________。
(4)单质C与稀硝酸反应的化学方程式是________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现将200mL0.01mol/LNaOH与50mL某浓度的Ca (OH)2溶液混合(混合后体积变化忽略不计),所得溶液中OH﹣的物质的量浓度是0.016mol/L,则Ca(OH)2溶液的物质的量浓度是mol/L.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com