
| A、由①知:氢气的燃烧热△H=-241.8 kJ/mol |
| B、由①、②知:2H2S(g)+O2(g)=2S(g)+2H2O(g)△H=-443.4 kJ/mol |
C、 反应②中的能量变化能用图表示 |
| D、若反应②中改用固态硫,放热将大于20.1kJ |


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
| A、HCO3-、NH4+、H+、Cl- |
| B、AlO2-、OH-、Na+、Cl- |
| C、AlO2-、H+、MnO42-、NO3- |
| D、Mg2+、Fe3+、NO3-、SCN- |
查看答案和解析>>
科目:高中化学 来源: 题型:
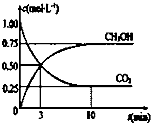 目前工业上也可用CO2来生产燃料甲醇,有关反应为:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.0kj?mol-1,现向体积为1L的密闭容器中,充入1molCO2和3molH2,反应过程中测得CO2和CH3PH(g)的浓度随时间的变化如图所示.
目前工业上也可用CO2来生产燃料甲醇,有关反应为:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.0kj?mol-1,现向体积为1L的密闭容器中,充入1molCO2和3molH2,反应过程中测得CO2和CH3PH(g)的浓度随时间的变化如图所示.| c(CH3OH) |
| c(CO2) |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、轮船水线以下的船壳上装一定数量的锌块 |
| B、镀锌的铁比镀锡的铁耐用 |
| C、纯锌与稀硫酸反应时,滴入少量硫酸铜溶液后速率加快 |
| D、铝片不用特殊方法保存 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氧化性S<O2<F2 |
| B、半径Be2+<Mg2+<K+ |
| C、酸性H2SiO3<H3PO4<H2SO4 |
| D、还原性Se2-<S2-<O2- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、葡萄糖的结构简式:C6H12O6 | ||
| B、NaHCO3的电离:NaHCO3=Na++H++CO32- | ||
C、质子数为53、中子数为78的碘原子:
| ||
D、CO2的电子式: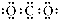 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、NaNO2发生氧化反应 |
| B、每生成1molN2时转移电子的物质的量为6mol |
| C、N2既是氧化产物,又是还原产物 |
| D、NH4Cl中的氮元素被还原 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com