
【题目】在镀锌铁皮的锌镀层厚度的测定过程中,下列操作会导致测定结果偏高的是
A.过早判断反应终点B.在测定铁皮的面积时测得面积比铁皮的实际面积大
C.过迟判断反应终点D.锌在酸中溶解后,铁皮未烘干就去称重
科目:高中化学 来源: 题型:
【题目】实验室为探究铁与浓硫酸(足量)的反应,并验证SO2的性质,设计如图所示装置进行实验,下列说法不正确的是( )

A. 装置C中产生淡黄色的沉淀,体现了SO2的氧化性
B. 装置E的作用是吸收未反应的SO2,防止污染空气
C. 装置D中品红溶液褪色后加热又变红色,可验证SO2溶于水显酸性
D. 实验时将导管a插入浓硫酸中,可防止装置B中的溶液倒吸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示向A中充入1 mol X 、1 mol Y,向B中充入2 mol X、2 mol Y,起始时,v(A)=v(B)=a L。在相同温度和有催化剂存在下,两容器中各自发生下述反应:X+Y![]() 2Z+W;(X、Y、Z、W均为气体)正反应为放热反应,达到平衡时,v(A)=1.2a L。
2Z+W;(X、Y、Z、W均为气体)正反应为放热反应,达到平衡时,v(A)=1.2a L。
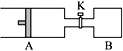
试回答:
(1)A中X的转化率α(A)_______________________________________________________。
(2)A、B中X的转化率的关系:α(A) ___________α(B)。(填“<”“>”或“=”)
(3)打开K,一段时间又达到平衡,A的体积为___________L。(连通管中气体体积不计)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学小组的同学取一定量的Al和Fe2O3的混合物进行铝热反应,并探究熔落物的成分。请回答下列问题:
Ⅰ.(1)引发铝热反应的实验操作是_____________________
(2)做铝热反应时,内层纸漏斗底部剪一小孔用水润湿的目的是_________________
(3)反应的化学方程式为_____________
Ⅱ.已知:Al、Fe的熔、沸点数据如下:
物质 | Al | Fe |
熔点(℃) | 660 | 1 535 |
沸点(℃) | 2 467 | 2 750 |
(1)某同学猜测,铝热反应所得到的熔落物是铁铝合金。理由:该反应放热能使铁熔化,而铝的熔点比铁低,所以铁和铝能形成合金。你认为他的解释是否合理?____________(填“合理”或“不合理”)。设计一个简单的实验方案,证明上述所得的熔落物中含有金属铝:_____________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以下是反应A(g) + 3B(g) 2C(g) + 2D(g) 在四种不同情况下的反应速率,反应速率最大的是
A. υ(A)=0.45mol·L-1·s-1B. υ(B)=0.6mol·L-1·s-1
C. υ(C)=0.4mol·L-1·s-1D. υ(D)=0.45mol·L-1·s-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有一种可做融雪剂的盐,其主要成分的化学式为XY2 , X、Y均为周期表前20号元素,其阳离子和阴离子的电子层结构相同,且1mol XY2含有54mol电子。
(1)该融雪剂的化学式是_________;用电子式表示XY2的形成过程__________________。
(2)主族元素D、E原子的最外层电子数是其电子层数的2倍,D与Y相邻, 则D的离子结构示意图是_________;D与E能形成一种类似于CO2的三原子分子,且每个原子均达到了8e稳定结构,该分子的化学键类型为_________(填“离子键”或“共价键”)。
(3)用化学式回答:
①D与Y的氢化物稳定性________>________;
②D与Y的最高价氧化物对应水化物酸性________>________。
(4)某兴趣小组设计的简易原电池装置如下图所示。回答下列问题:

①锌片为_____极(填“正”或“负”)。
②电池正极的现象是_________________,其电极反应式为_____________________。
③电流由_______经导线流向______(填“锌片”或“碳棒”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2019年是元素周期表诞生150周年,元素周期表(律)在学习、研究和生产实践中有很重要的作用。下表为元素周期表的一部分,回答下列问题。
族 周期 | IA | 0 | ||||||
1 | ① | IIA | IIIA | IVA | VA | VIA | VIIA | |
2 | ② | ③ | ||||||
3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
4 | ||||||||
(1)元素①~⑧中,金属性最强的是________(填元素符号)。
(2)中国青年化学家姜雪峰被国际组织推选为“元素⑦代言人”,元素⑦的原子结构示意图是________,其氢化物的电子式是_________。
(3)元素①和②可以形成多种化合物。下图模型表示的分子中,不可能由①和②形成的是_______(填序号)。
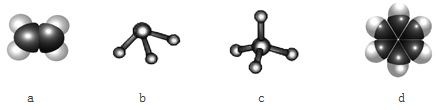
(4)比较元素②、③的最高价氧化物对应水化物的酸性:______>______(填化学式)。说明你判断的理由:_________。
(5)主族元素砷(As)的部分信息如图所示。
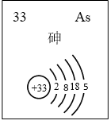
i.砷(As)在周期表中的位置是______。
ii.下列说法正确的是_______(填序号)。
a. 砷元素的最高化合价为+4
b. 推测砷有多种氧化物
c. ③的气态氢化物的还原性大于砷的气态氢化物的还原性
(6)某小组同学设计实验比较VIIA元素的非金属性:Cl>Br>I。
已知:常温下浓盐酸与高锰酸钾反应生成氯气。
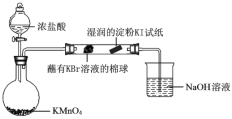
打开分液漏斗的活塞,烧瓶中产生黄绿色气体,蘸有KBr溶液的棉球变为橙红色,湿润的淀粉KI试纸变蓝,据此现象能否说明非金属性:Br > I,并说明理由_________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com