
常温条件下,下列各组离子在指定溶液中能大量共存的是
A.使石蕊试液变红的溶液中:Fe2+、NO 、SO42—、Na+
、SO42—、Na+
B.由水电离出的c(H+)=1×10-14mol/L的溶液中:Ca2+、Cl-、HCO 、K+
、K+
C.c(H+)/c(OH-)=1×1012的溶液中:NH 、Cl-、SO42—、Al3+
、Cl-、SO42—、Al3+
D.c(Al3+)=0.1 mol/L的溶液中:K+、Cl-、SO42—、CO32-
科目:高中化学 来源: 题型:
下列说法正确的是( )
A.因为水分子间的氢键,H2O比H2S稳定
B.氯水、氨水、王水是混合物,水银、水玻璃是纯净物
C.HCl、NH3、BaSO4是电解质,CO2、Cl2、CH3CH2OH是非电解质
D. 原子核外有92个电子,
原子核外有92个电子, 和
和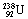 互为同位素
互为同位素
查看答案和解析>>
科目:高中化学 来源: 题型:
【化学—选修3:物质结构与性质】(15分)
氮化钛( Ti3N4)为金黄色晶体,由于具有令人满意的仿金效果,越来越多地成为黄金代替品。以TiCl4为原料,经过一系列反应(如图所示),可以制得Ti3N4和纳米TiO2请回答下列问题:

(1)反应①为置换反应,写出该反应的化学方程式 ;TiCl4分子中4个氯原子不在同一平面上,则TiCl4的空间构型为 。
(2)元素周期表中Ti元素位于第 周期 族。与Ti相邻的元素Zr的基态原子外围电子排布式为 ,
(3)纳米TiO2是一种应用广泛的催化剂,纳米Ti02催化的一个实验如图所示。
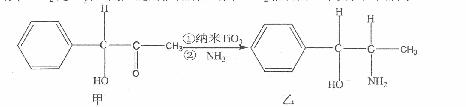
 化合物甲的分子中采取sp2方式杂化的碳原子个数为 ,化合物乙中采取sp3杂化的原子的第一电离能由大到小的顺序为 。
化合物甲的分子中采取sp2方式杂化的碳原子个数为 ,化合物乙中采取sp3杂化的原子的第一电离能由大到小的顺序为 。
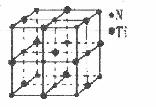
(4)有一种氮化钛晶体的晶胞如图所示,该氮化钛晶胞中
含有 个N原子,晶胞中N、Ti之间的最近距离为
a pm,则该氮化钛的密度为 g.cm-3(NA为阿
伏加德常数的数值,只列算式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
两支试管中分别加入足量的等物质的量浓度的稀硫酸和氢氧化钠溶液,然后分别加入等质量的金属铝,充分反应,放出气体的体积比为
A.2︰3 B.3︰2 C.1︰3 D.1︰1
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各式中,属于正确的电离方程式的是
A.HCO3- + H2O  H2CO3 + OH- B.HCO3- +OH- === H2O + CO32-
H2CO3 + OH- B.HCO3- +OH- === H2O + CO32-
C.NH3 + H+ === NH4+ D.NH3·H2O  NH4+ + OH-
NH4+ + OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关实验操作的说法正确的是
A.可用25ml碱式滴定管量取20.00 ml KMnO4 溶液
B.用pH试纸测定溶液的pH时,需先用蒸馏水润湿试纸
C.用量筒量取5.00 mL 1. 00mol·L-1盐酸于50mL容量瓶中,加水稀释至刻度可配
制0.100mol·L-1盐酸
D.中和滴定时盛待测液的锥形瓶中有少量水对滴定结果无影响
查看答案和解析>>
科目:高中化学 来源: 题型:
常温下,下列各组离子在指定溶液中一定能大量共存的是
A.无色溶液中:K+、Na+、Cu2+、SO42-
B.水电离产生的c(H+)=10-13 mol·L-1的溶液中:Na+、Cl-、NO3-、SO42-
C.0.1 mol·L-1FeSO4溶液中:K+、NH4+、MnO4-、ClO-
D.c(OH-)=10-13 mol·L-1的溶液中:Al3+、NO3-、I-、Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
对于Zn(s)+H2SO4(aq)=ZnSO4(aq)+H2(g) ΔH <0 的化学反应下列叙述不正确的是
A.该反应是放热反应 B.ΔH的值与反应方程式的计量系数有关
C.若将该反应设计成原电池则锌为负极
D.若将其设计为原电池,当有32.5g锌溶解时,正极放出气体一定为11.2L
查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y、Z、W是元素周期表中原子序数依次增大的四种短周期元素,其相关信息如下表:
| 元素 | 相关信息 |
| X | X的最高价氧化物对应的水化物化学式为H2XO3 |
| Y | Y是地壳中含量最高的元素 |
| Z | Z的基态原子最外层电子排布式为3s23p1 |
| W | W的一种核素的质量数为28,中子数为14 |
| T | 常温常压下,T单质是淡黄色固体,常在火山口附近沉积 |
| P | P的价层电子排布为[Ar]3d104s2 |
(1)W位于元素周期表第________周期第________族;W的原子半径比X的________(填“大”或“小”)。
(2)TY2中心原子的杂化方式为_______;XY2中一个分子周围有__________个紧邻分子;堆积方式与XY2晶胞类型相同的金属有_________(从“Cu、 Mg、K、Po”中选出正确的),其空间利用率为_______。
(3)Z的第一电离能比Mg的________(填“大”或“小”);写出Z单质与NaOH溶液反应的化学方程式 。
(4)写出W的最高价氧化物与NaOH溶液反应的离子方程式 ;W的最高价氧化物与XY2的熔点较高的是 ,原因是 。
(5)处理含XO、TO2烟道气污染的一种方法,是将其在催化剂作用下转化为单质T。已知:
XO(g)+ 1/2O2(g)====XO2(g) ΔH=-283.0 kJ·mol-1
T(s)+O2(g)=====TO2(g) ΔH=-296.0 kJ·mol-1
此反应的热化学方程式是______________________________。
(6)P在周期表的 区;P和T形成的化合物PT在荧光体、光导体材料、涂料、颜料等行业中应用广泛。立方PT晶体结构如下图所示,其晶胞边长为540.0 pm,密度为_________ g·cm-3(列式并计算)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com