
【题目】将碱溶液A、盐溶液B按如下程序进行实验,根据下述现象判断: 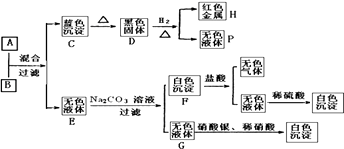
(1)A和B中溶质的化学式A;B、 .
(2)完成下列转化的化学方程式,是离子反应的只写离子方程式.
①A+B→C+E:;
②D+H2→H+P:;
③E+Na2CO3→F+G:;
④F+盐酸→I+E: .
【答案】
(1)Ba(OH)2;CuCl2
(2)Cu2++2OH﹣=Cu(OH)2↓;H2+CuO ![]() Cu+H2O;Ba2++CO32﹣=BaCO3↓;BaCO3+2H+=Ba2++CO2↑+H2O
Cu+H2O;Ba2++CO32﹣=BaCO3↓;BaCO3+2H+=Ba2++CO2↑+H2O
【解析】解:由转化关系图可知,红色金属H为Cu,蓝色沉淀C为Cu(OH)2 , 加热氢氧化铜时,氢氧化铜分解生成黑色固体D为CuO,氧化铜被氢气还原生成铜和水,所以P为H2O;碱溶液A+盐溶液B→Cu(OH)2+无色溶液E,B为铜盐,由无色溶液E和碳酸钠溶液反应生成白色沉淀F及G,G的溶液中加入硝酸银、硝酸得到白色沉淀,故G为氯化钠,无色溶液E含有Cl﹣ , 故盐溶液B为CuCl2 , F为碳酸盐,F和盐酸反应生成无色气体和无色溶液,该无色溶液和稀硫酸反应生成白色沉淀,故无色溶液含有Ba2+ , 故白色沉淀F为BaCO3 , 无色溶液E含有Cl﹣ , 故E为BaCl2 , 再结合碱溶液A+盐溶液B→Cu(OH)2+无色溶液E,故A为Ba(OH)2 , 验证符合转化关系,(1)通过以上分析知,A溶液和B溶液的溶质分别是Ba(OH)2、CuCl2 , 所以答案是:Ba(OH)2、CuCl2;(2)①A+B→C+E是氢氧化钡与氯化铜反应生成氢氧化铜与氯化钡,反应离子方程式为:Cu2++2OH﹣=Cu(OH)2↓;②D+H2→H+P是氢气和氧化铜发生氧化还原反应生成铜和水,反应方程式为:H2+CuO ![]() Cu+H2O;③E+Na2CO3→F+G是氯化钡与碳酸钠反应生成碳酸钡与氯化钠,反应离子方程式为:Ba2++CO32﹣=BaCO3↓;④F+盐酸→I+E是碳酸钡与盐酸反应生成氯化钡、二氧化碳与水,反应离子方程式为:BaCO3+2H+=Ba2++CO2↑+H2O,
Cu+H2O;③E+Na2CO3→F+G是氯化钡与碳酸钠反应生成碳酸钡与氯化钠,反应离子方程式为:Ba2++CO32﹣=BaCO3↓;④F+盐酸→I+E是碳酸钡与盐酸反应生成氯化钡、二氧化碳与水,反应离子方程式为:BaCO3+2H+=Ba2++CO2↑+H2O,
所以答案是:Cu2++2OH﹣=Cu(OH)2↓;H2+CuO ![]() Cu+H2O;Ba2++CO32﹣=BaCO3↓;BaCO3+2H+=Ba2++CO2↑+H2O.
Cu+H2O;Ba2++CO32﹣=BaCO3↓;BaCO3+2H+=Ba2++CO2↑+H2O.


科目:高中化学 来源: 题型:
【题目】向盛有氯气的三个集气瓶中,分别注入约五分之一的下列液体并振荡,观察如图所记录的现象,判断各瓶注入的液体依次是什么.( )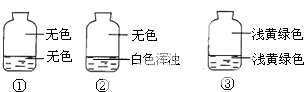
A.AgNO3溶液、NaOH溶液、水
B.NaOH溶液、AgNO3溶液、水
C.水、AgNO3溶液、NaOH溶液
D.AgNO3溶液、水、NaOH溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用铜片、银片、Cu(NO3)2溶液、AgNO3溶液、导线和盐桥(装有琼脂﹣KNO3的U形管)构成一个原电池(如图).以下有关该原电池的叙述正确的是
①在外电路中,电子由铜电极流向银电极
②正极反应为:Ag++e﹣=Ag
③实验过程中取出盐桥,原电池仍继续工作
④将铜片浸入AgNO3溶液中发生的化学反应与该原电池反应相同( )
A.①②
B.①②④
C.②③
D.①③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
A.在原电池的负极和电解池的阴极上都发生失电子的氧化反应
B.用惰性电极电解Na2SO4溶液,阴阳两极产物的物质的量之比为1:2
C.用惰性电极电解饱和NaCl溶液,若有0.1 mol电子转移,则生成0.1 mol NaOH
D.镀层破损后,镀锌铁板比镀锡铁板更易腐蚀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验与对应示意图的关系正确的是( )
A | B | C | D |
NaAlO2溶液中逐滴滴加盐酸至过量 | AlCl3溶液中逐滴滴加氨水至过量 | 明矾溶液中逐滴滴加Ba(OH)2溶液至过量 | 澄清石灰水中缓慢通入CO2至过量 |
|
|
|
|
A.A
B.B
C.C
D.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海水开发利用的部分过程如图所示.下列说法错误的是( ) 
A.向苦卤中通入Cl2是为了提取溴
B.粗盐可采用除杂和重结晶等过程提纯
C.工业生产常选用NaOH作为沉淀剂
D.富集溴一般先用空气和水蒸气吹出单质溴,再用SO2将其还原吸收
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用铜片、银片、Cu(NO3)2溶液、AgNO3溶液、导线和盐桥(装有琼脂﹣KNO3的U形管)构成一个原电池(如图).以下有关该原电池的叙述正确的是
①在外电路中,电子由铜电极流向银电极
②正极反应为:Ag++e﹣=Ag
③实验过程中取出盐桥,原电池仍继续工作
④将铜片浸入AgNO3溶液中发生的化学反应与该原电池反应相同( )
A.①②
B.①②④
C.②③
D.①③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将117g NaCl溶于水配制成1L溶液,
(1)该溶液中NaCl的物质的量浓度为 , 溶液中Cl﹣的物质的量浓度为 .
(2)配制1molL﹣1的NaCl溶液500mL,需该溶液的体积为 .
(3)向该溶液中再通入一定量的HCl气体后,溶液中Cl﹣的物质的量浓度为3molL﹣1(假设溶液体积不变),则溶液中H+的物质的量浓度为 , 通入HCl气体的体积(标准状况下)为 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com