
铁及其化合物在生产、生活中有广泛应用.请回答下列问题:
(一)高炉炼铁过程中发生的主要反应为:
 Fe2O3(s)+CO(g)
Fe2O3(s)+CO(g)
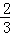 Fe(s)+CO2(g)
Fe(s)+CO2(g)
已知该反应在不同温度下的平衡常数 如下:
温度/℃ 1000 1115 1300
平衡常数 4.0 3.7 3.5
(1)该反应的平衡常数表达式K=___;△H___0(填“>”、“<”或“=”).
(2)欲提高上述反应中CO的平衡转化率,可采取的措施是_____.
A.提高反应温度 B.移出部分CO2
C.加入合适的催化剂 D.减小容器的容积
(3)在一个容积为10L的密闭容器中,1000℃时加入Fe、Fe2O3、CO、CO2各1.0mol,此时υ正___υ逆(填“>”、“<”或“=”).经过10min,在1000℃达到平衡,则该时间范围内反应的平均反应速率υ(CO2)=_____.
(二)高铁酸钾(K2FeO4)是一种集氧化、吸附、絮凝于一体的新型多功能水处理剂.
(4)一定条件下Fe(OH)3与KClO在KOH溶液中反应可制得K2FeO4,其中反应的氧化剂是_____;生成1mol K2FeO4转移电子的物质的量是_____mol.
科目:高中化学 来源:2015-2016学年河北省高二上12月月考化学试卷(解析版) 题型:选择题
据报道,我国拥有完全自主产权的氢氧燃料电池车将在北京奥运会期间为运动员提供服务。某种氢氧燃料电池的电解液为KOH溶液,下列有关该电池的叙述不正确的是
A.正极反应式为:O2+2H2O+4e-=4OH-
B.工作一段时间后,电解液中KOH的物质的量不变
C.该燃料电池的总反应方程式为:2H2+O2=2H2O
D.用该电池电解CuCl2溶液,产生2.24 L Cl2(标准状况)时,有0.1 mol电子转移
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省高一上学期12月月考化学试卷(解析版) 题型:选择题
某溶液中Cl-、Br-、I- 三者物质的量之比为2︰3︰4,要使溶液中Cl-、Br-、I- 物质的量之比为1︰1︰1,则通入Cl2的物质的量是原溶液中I- 物质的量的
A.1/2 B.1/3 C.1/4 D.1/8
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江西省高一上学期12月月考化学试卷(解析版) 题型:选择题
有两种金属组成的混合物粉末20g与足量的稀盐酸反应,生成22.4L(标准状况)H2,则该混合物的组成可能是
A.Fe 和Zn B.Al和Cu C.Na和Mg  D.Mg和Fe
D.Mg和Fe
查看答案和解析>>
科目:高中化学 来源:2016届福建省闽粤联合体高三上学期第三次联考化学试卷(解析版) 题型:实验题
实验室有一包固体粉末样品可能是MgCO3、Fe2O3和FeO的混合物。
I.甲学生设计实验方案,以确定样品中是否含有FeO。除样品外,实验室只提供以下试剂:KMnO4溶液、盐酸、稀硫酸、KSCN溶液、NaOH溶液,请你描述甲学生的实验操作步骤、现象及结论: 。
Ⅱ.经甲学生实验确定该样品中不存在FeO,乙学生想在甲学生的实验基础上进一步来测定混合物中Fe2O3的含量:乙学生准备用如图所示各仪器按一定顺序连接成一套完整的装置进行实验,以测定Fe2O3的质量分数。
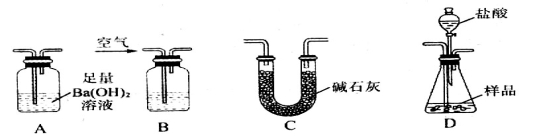
请回答下列问题:
(1)盛装盐酸的仪器的名称是 ,装置的连接顺序是:_____→_____→______→_____(填图中字母序号,各仪器只能选用一次)。
(2)实验过程中需要持续通入空气,其作用除可以起到“搅拌”A、D中反应物以实现充分反应外,还有一个重要作用是:____________________________。
(3)为提高测定的准确度,在B中最应加入的物质是: (填字母编号)。
a.饱和NaHCO3溶液 b.蒸馏水 c.浓硫酸 d.NaOH溶液
(4)在进行乙学生的实验方案评价时,有学生认为不必测定A中沉淀的质量,而只要测出装置A在吸收反应产生的气体前后的质量差,就能完成实验要求。实验证明,若用此法测得Fe2O3的质量分数将__________(填“偏大”、“偏小”或“不变”)。
查看答案和解析>>
科目:高中化学 来源:2016届辽宁省高三上学期12月月考理综化学试卷(解析版) 题型:选择题
下列说法中不正确的是
A.按系统命名法:CH3CH2C(CH3)2CH(C2H5)CH3 的正确名称是3,3,4-三甲基己烷
B.所有的糖、油脂、蛋白质都能水解,但水解产物不同
C.1 mol的  最多能与含5mol NaOH的水溶液完全反应
最多能与含5mol NaOH的水溶液完全反应
D.若完全燃烧,1 mol雄酮(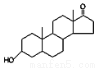 )比雌酮(
)比雌酮(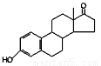 )多消耗3 mol O2
)多消耗3 mol O2
查看答案和解析>>
科目:高中化学 来源:2016届安徽省高三上1月阶段测理综化学试卷(解析版) 题型:实验题
阿司匹林(乙酰水杨酸, )是世界上应用最广泛的解热、镇痛和抗炎药.乙酰水杨酸受热易分解,分解温度为128~135℃.某学习小组在实验室以水杨酸(邻羟基苯甲酸)与醋酸酐[(CH3CO)2O]为主要原料合成阿司匹林,制备基本操作流程如下:
)是世界上应用最广泛的解热、镇痛和抗炎药.乙酰水杨酸受热易分解,分解温度为128~135℃.某学习小组在实验室以水杨酸(邻羟基苯甲酸)与醋酸酐[(CH3CO)2O]为主要原料合成阿司匹林,制备基本操作流程如下:
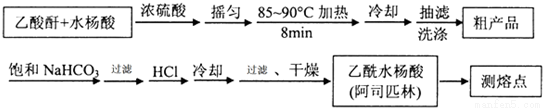
主要试剂和产品的物理常数
名称 | 相对分子质量 | 熔点或沸点(℃) | 水 |
水杨酸 | 138 | 158(熔点) | 微溶 |
醋酸 | 102 | 139.4(沸点) | 反应 |
乙酸水杨酸 | 180 | 135(熔点) | 微溶 |
请根据以上信息回答下列问题:
(1)制备阿司匹林时,要使用干燥的仪器的原因是_____________________;
(2)写出制备阿司匹林的化学方程式_____________________;
(3)①合成阿斯匹林时,最合适的加热方法是____________;
②过滤所得粗产品要用少量冰水洗涤,则洗涤的具体操作是_____________________;
(4)提纯粗产物中加入饱和NaHCO3溶液至没有CO2产生为止,再过滤,则加饱和NaHCO3溶液的目的是_____________________;另一种改进的提纯方法,称为重结晶提纯法.方法如下:
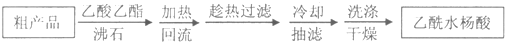
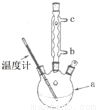
(5)改进的提纯方法中加热同流的装置如下图所示,使用温度计的目的是_______________;冷凝水的流进方向是__________(填“b”或“c”)。
(6)检验产品中是否含有水杨酸的试剂是_______________;
(7)该学习小组在实验中原料用量:2.0g水杨酸、5.0mL醋酸酐(ρ=1.08g/cm3),最终称得产品m=2.2g,则所得乙酰水杨酸的产率为_______________;
查看答案和解析>>
科目:高中化学 来源:2016届浙江省金丽衢十二校高三上学期第一次联考化学试卷(解析版) 题型:选择题
设NA为阿伏加德罗常数的值,下列叙述正确的是
A.25 ℃,pH=12的Na2CO3溶液中含有OH-的数目为0.01NA
B.1 mol苯乙烯( )中含有的碳碳双键数为4NA
)中含有的碳碳双键数为4NA
C.加热条件下,4.6 g金属Na与足量O2反应的产物中阳离子和阴离子总数为0.3NA
D.常温时,1 L 0.1 mol·L-1的硝酸铵溶液中,NH4+和H+总数为0.1NA
查看答案和解析>>
科目:高中化学 来源:2016届黑龙江省高三上期末理综化学试卷(解析版) 题型:选择题
生活中碰到的某些问题和物质,常涉及到化学知识,下列分析不正确的是
A.维生素A: 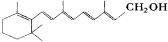 它是一种难溶于水的醇
它是一种难溶于水的醇
B.用灼烧并闻气味的方法区别纯棉织物和纯毛织物
C.某雨水样品采集后放置一段时间,pH值由4.68变为4.28,是因为水中溶解了较多的CO2
D.金属材料都是导体,非金属材料不都是绝缘体
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com