
设NA为阿伏加德罗常数的值。下列说法正确的是( )
A.标准状况下,1.12 L CCl4含有C—Cl键数目为0.2NA
B.标准状况下,2.24 L氯气中含有的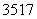 Cl数目一定为 0.2NA
Cl数目一定为 0.2NA
C.常 温常压下,4.4 g CO2与N2O混合气体中含有的原子总数为0.3NA
温常压下,4.4 g CO2与N2O混合气体中含有的原子总数为0.3NA
D.80 mL 10 mol·L-1盐酸与足量MnO2加热反应,产生Cl2分子数为0.2NA
科目:高中化学 来源: 题型:
褪黑素是一种内源性生物钟调节剂,在人体内由食物中的色氨酸转化得到。
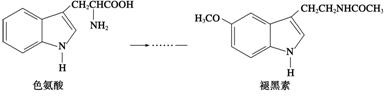
下列说法不正确的是 ( )
A.色氨酸分子中存在氨基和羧基,可形成内盐,具有较高的熔点
B.在色氨酸水溶液中,可通过调节溶液的pH使其形成晶体析出
C.在一定条件下,色氨酸可发生缩聚反应
D.褪黑素与色氨酸结构相似,也具有两性化合物的特性
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于某些社会热点问题的说法中,不正确的是( )
A.禁用含铅汽油是为了提高汽油的燃烧效率
B.甲醇含量超标的酒绝对不能饮用
C.甲醛是某些劣质装饰材料释放的常见室内污染物之一
D.氟氯烃对大气臭氧层具有破坏作用
查看答案和解析>>
科目:高中化学 来源: 题型:
某课外小组设计的实验室制取乙酸乙酯的装置如下图所示,A中盛有浓H2SO4,B中盛有乙醇、无水醋酸钠,D中盛有饱和碳酸钠溶液。
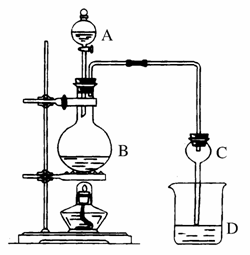
已知:①无水氯化钙可与乙醇形成难溶于水的CaCl2·6C2H5OH。
②有关有机物的沸点:
| 试剂 | 乙醚 | 乙醇 | 乙酸 | 乙酸乙酯 |
| 沸点(℃) | 34.7 | 78.5 | 118 | 77.1 |
请回答:
(1)浓硫酸的作用__________;若用同位素18O示踪法确定反应产物水分子中氧原子的提供者(设18O在CH3CH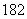 OH中),写出能表示18O位置的化学方程式_____________________________________ ___________________________________。
OH中),写出能表示18O位置的化学方程式_____________________________________ ___________________________________。
(2)球形干燥管C的作用是______________。若反应前向D中加入几滴酚酞,溶液呈红色,产生此现象的原因是(用离子方程式表示):________________________;反应结束后D中的现象是______________________。
(3)从D中分离出的乙酸乙酯中常含有一定量的乙醇、乙醚和水,应先加入无水氯化钙,分离出______________;再加入无水硫酸钠,然后进行蒸馏,收集产品乙酸乙酯时,温度应控制在__________左右。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
A.32 g 18O2中含有的氧原子数是2×6.02×1023
B.1 mol N2和CO的混合气体中含有的分子总数是2×6.02×1023
C.2.3 g Na与O2完全反应生成3.6 g产物时失电子数是0.1×6.02×1023
D.1.0 L 0.1 mol·L-1 NH4NO3溶液中含有的铵根离子数是0.1×6.02×1023
查看答案和解析>>
科目:高中化学 来源: 题型:
NA表示阿伏加德罗常数。下列判断正确的是( )
A.25 ℃,pH=13的NaOH溶液中含有OH-的数目为0.1NA
B.分别为7.8 g的Na2S和Na2O2中含有的 阴离子数分别是0.1NA和0.2NA
阴离子数分别是0.1NA和0.2NA
C.常温常压下,22.4 L CO2中含有的CO2分子数小于NA
D.1 L 0.1 mol/L的氨水含有0.1NA个NH3·H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
在恒温下的密闭容器中,有可逆反应2NO2N2O4,下列描述不能说明反应达到平衡状态的是( )
A.N2O4生成速率与N2O4分解速率相等
B.混合气体平均相对分子质量保持不变
C.NO2的分子数与N2O4分子数之比为2:1
D.体系颜色不再发生改变
查看答案和解析>>
科目:高中化学 来源: 题型:
用CaSO4代替O2与燃料CO反应,既可提高燃烧效率,又能得到高纯CO2,是一种高效、清洁、经济的新型燃烧技术。反应①为主反应,反应②和③为副反应。
①1/4CaSO4(s)+CO(g)1/4CaS(s)+CO2(g)
ΔH1=-47.3 kJ·mol-1
②CaSO 4(s)+CO(g)CaO(s)+CO2(g)+SO2(g)
4(s)+CO(g)CaO(s)+CO2(g)+SO2(g)
ΔH2=+210.5 kJ·mol-1
③CO(g)1/2C(s)+1/2CO2(g)
ΔH3=-86.2 kJ·mol-1
(1)反应2CaSO4(s)+7CO(g)CaS(s)+CaO(s)+6CO2(g)+C(s)+SO2(g)的ΔH=________(用ΔH1、ΔH2和ΔH3表示)。
(2)反应①~③的平衡常数的对数lgK随反应温度T的变化曲线如图所示,结合各反应的ΔH,归纳lgK-T曲线变化规律:
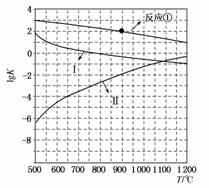
a)__________________________________________________________;
b)_________________________________________________________。
(3)向盛有CaSO4的真空恒容密闭容器中充入CO,反应①于900 ℃达到平衡,c平衡(CO)=8.0×10-5 mol·L-1,计算CO的转化率________(忽略副反应,结果保留两位有效数字)。
(4)为减少副产物,获得更纯净的CO2,可在初始燃料中适量加入________________________________________________________________________。
(5)以反应①中生成的CaS为原料,在一定条件下经原子利用率100%的高温反应,可再生CaSO4,该反应的化学方程式为______________________;在一定条件下,CO2可与对二甲苯反应,在其苯环上引入一个羧基,产物的结构简式为________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
对于反应A(g)+3B(g)  2C(g),下列各数据表示不同条件下的反应速率,其中反应进行得最快的是( )
2C(g),下列各数据表示不同条件下的反应速率,其中反应进行得最快的是( )
A、v(A)=0.01 mol/(L•s) B、v(B)=0.02 mol/(L•s)
C、v(B)=0.60mol/(L•min) D、v(C)=1.0mol/(L•min)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com