
| A. | N2是还原产物 | |
| B. | 有 0.250 mol KNO3 被氧化 | |
| C. | NaN3中氮元素为-3 价 | |
| D. | 被氧化的 N 原子的物质的量为 3.75mol |
分析 该反应中N元素化合价由-$\frac{1}{3}$、+5价变为0价,所以NaN3是还原剂、KNO3是氧化剂,N2既是氧化产物又是还原剂,根据反应方程式可知,每当生成16molN2,则氧化产物比还原产物多14mol,转移电子的物质的量为10mol,被氧化的N原子的物质的量为30mol,有2molKNO3被还原;
现氧化产物比还原产物多1.75mol,则生成2molN2,转移电子的物质的量为1.25mol,被氧化的N原子的物质的量为3.75mol,以此解答该题.
解答 解:该反应中N元素化合价由-$\frac{1}{3}$价、+5价变为0价,所以氧化产物和还原产物都是氮气,假设有16mol氮气生成,氧化产物是15mol、还原产物是1mol,则氧化产物比还原产物多14mol,若氧化产物比还原产物多1.75mol,则参加反应的n(KNO3)=$\frac{1.75mol}{14mol}$=0.25mol,
A.氧化产物和还原产物都是氮气,故A错误;
B.硝酸钾得电子作氧化剂而被还原,故B错误;
C.NaN3中氮元素为-$\frac{1}{3}$ 价,故C错误;
D.被氧化的N原子的物质的量=$\frac{1.75mol}{14mol}$=3.75 mol,故D正确;
故选D.
点评 本题考查氧化还原反应有关计算,侧重考查分析计算能力,明确氧化产物和还原产物关系是解本题关键,注意叠氮化钠中N元素化合价,注意硝酸钾被还原而不是被氧化,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 溶液与胶体的本质区别是丁达尔效应 | |
| B. | 存放碳酸钠溶液的试剂瓶应使用玻璃塞 | |
| C. | 硝酸存放于棕色瓶中 | |
| D. | 试管、坩埚、蒸馏烧瓶都可以用酒精灯直接加热 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②⑤ | B. | ①④⑤ | C. | ②④⑤ | D. | ①③⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 纯净物 | 混合物 | 电解质 | 非电解质 | |
| A | 冰水混合物 | CuSO4•5H2O | 液态 KNO3 | 蔗糖 |
| B | CaO溶液 | 海水 | 铜 | 酒精 |
| C | 氯气 | 铝合金 | AgCl | CO2 |
| D | 氢氧化钠 | 空气 | Na2SO4溶液 | 食醋 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 酒精、汽车在桌面上着火时,立即用水扑灭 | |
| B. | 用蒸发方法使NaCl从溶液中析出时,应将蒸发皿中NaCl溶液全部加热蒸干 | |
| C. | 用浓硫酸配制一定物质的量浓度的稀硫酸时,浓硫酸溶于水后,应立即转移到容量瓶中定容,以减小误差 | |
| D. | 用分液漏斗分液时,下层液体从下口放出,上层液体从上口倒出 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 蔗糖溶液不能导电,故蔗糖溶液时非电解质 | |
| B. | AgCl难溶于水,属于电解质 | |
| C. | SO3溶于水形成的溶液能导电,所以SO3是电解质 | |
| D. | 纯水的导电性很差,所以水不是电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
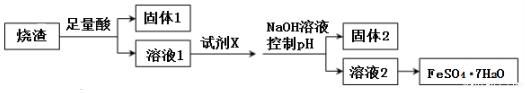
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
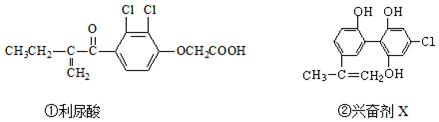
| A. | 利尿酸能发生取代反应、加成反应和酯化反应 | |
| B. | 1mol兴奋剂X与足量浓溴水反应,最多消耗3molBr2 | |
| C. | 可用FeCl3溶液检测利尿酸中是否含有兴奋剂X | |
| D. | 1mol兴奋剂X最多都能和5molNaOH的溶液反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com