
| 选项 | 实验操作 | 现象 | 解释或结论 |
| A | 过量的Fe粉中加入HNO3, 充分反应后,滴入KSCN溶液 | 溶液呈红色 | 稀HNO3将Fe氧化为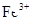 |
| B | AgI沉淀中滴入稀KCl溶液 | 有白色沉淀出现 | AgCl比AgI更难溶 |
| C | Al箔插入稀HNO3中 | 无现象 | Al箔表面被HNO3氧化,形成致密的氧化膜 |
| D | 用玻璃棒蘸取浓氨水点到红色石蕊试纸上 | 试纸变蓝色 | 浓氨水呈碱性 |
 名师金手指领衔课时系列答案
名师金手指领衔课时系列答案科目:高中化学 来源:不详 题型:实验题
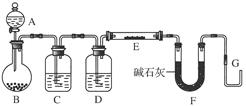
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
 品预处理,得到含有草酸及草酸盐的溶液。
品预处理,得到含有草酸及草酸盐的溶液。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
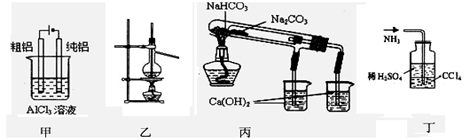
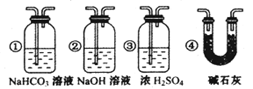
| A.用甲图装置电解精炼铝 | B.用乙图装置可用于石油的分馏 |
| C.丙图装置可验证NaHCO3和Na2CO3热稳定性 | D.丁图装置可吸收含有氨气的尾气 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
 ;
; 中可以燃烧。
中可以燃烧。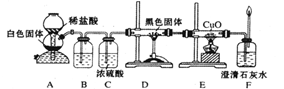
 置C吸收气体中水蒸气的理由是_
置C吸收气体中水蒸气的理由是_ ______。
______。
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.鉴别集气瓶中的甲烷和乙烯:分别点燃,观察火焰的颜色及是否有黑烟 |
| B.检验酒精中的少量水:向酒精中加入足量生石灰 |
| C.制备氯乙烷(C2H5Cl):将乙烷和氯气的混合气放在光照条件下反应 |
| D.除去乙烷中的乙烯气体:将实验室制得的乙烯气体通入NaOH 溶液 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| A.量筒 | B.容量瓶 | C.滴定管 | D.烧杯 |
| 物质 | Cu(OH)2 | Fe(OH)2 | Fe(OH)3 |
| 开始沉淀pH | 6.0 | 7.5 | 1.4 |
| 沉淀完全pH | 13 | 14 | 3.7 |
| 实验步骤 | 实验操作 | 实验操作目的 |
| 步骤1 | | |
| 步骤2 | | |
| 步骤3 | | |
| 步骤4 | 洗涤沉淀 | |
| 步骤5 | | 得到FeSO4溶液 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.某待测液中滴加氯化钡溶液产生白色沉淀,则该待测液中一定含有SO42- |
| B.氯化氢与氨气相遇,有大量的白雾生成 |
| C.漂白粉可敞口贮存 |
| D.稀释浓硫酸时,可将浓硫酸慢慢加入水中并搅拌 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com