
分析 (1)Fe能与氯化铁反应生成氯化亚铁;
(2)FeCl2可与氯气反应生成FeCl3;
(3)铁离子具有强氧化性,可氧化铜;
(4)Na2O2与CO2反应生成碳酸钠和氧气.
解答 解:(1)Fe能与氯化铁反应生成氯化亚铁,则选择除杂试剂为Fe粉,发生的离子反应为2Fe3++Fe=3Fe2+,故答案为:Fe粉;2Fe3++Fe=3Fe2+;
(2)FeCl2可与氯气反应生成FeCl3,可加入氯水或通入氯气,反应的离子方程式为Cl2+2Fe2+═2Fe3+,故答案为:氯水(Cl2); Cl2+2Fe2+═2Fe3+;
(3)铁离子具有强氧化性,可氧化铜,反应的离子方程式为2Cu+2Fe3+═2Fe2++Cu2+,故答案为:2Cu+2Fe3+═2Fe2++Cu2+;
(4)Na2O2与CO2反应生成碳酸钠和氧气,反应的化学方程式为2Na2O2+2CO2═2Na2CO3+O2↑,故答案为:2Na2O2+2CO2═2Na2CO3+O2↑.
点评 本题考查混合物的分离、提纯,把握物质的性质选择合适的试剂为解答本题的关键,侧重除杂、鉴别物质的考查,题目难度不大,注意除杂不能引入新杂质.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
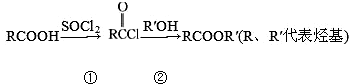 ,①②两步的产率均可达到90%以上,而RCOOH直接转化为RCOOR′产率在 60%左右,则下列说法不正确的是( )
,①②两步的产率均可达到90%以上,而RCOOH直接转化为RCOOR′产率在 60%左右,则下列说法不正确的是( )| A. | ①②两步均为取代反应 | |
| B. | ①②总产率比羧酸直接与醇反应产率高 | |
| C. | SOCl2若与足量羧酸反应产物除了 外,还有硫酸 外,还有硫酸 | |
| D. | SOCl2可以和水反应,故①反应不能用醋酸水溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 能加大反应速率、促进平衡向三氧化硫的方向移动 | |
| B. | 能提高二氧化硫的利用率、使原料不被浪费 | |
| C. | 能提高三氧化硫的平衡浓度 | |
| D. | 加大正逆反应速率,缩短达到平衡的时间 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com