
有一种白色固体A,加入油状无色液体酸B,可得紫黑色固体C,C微溶于水,加入A后C的溶解度增大,成棕色溶液D,将D分成两份,一份中加入无色溶液E,另一份不断通入气体F,两份都腿色成无色透明溶液。E溶液遇酸有淡黄色沉淀,将气体F通入溶液E,在所得溶液中加入BaCl2溶液有白色沉淀,后者难溶于HNO3。问A、B、、C、D、E、F各代表何物?写出各步反应的化学方程式。
分析:利用各有关单质和化合物的物理、化学性质来推知各未知物质是什么物质。这些单质和化合物之间通过一连串化学反应过程有机地联系起来。解题方法常用“反推法”,即从后向前推测。切忌通过一步反应,就确立某一个未知化合物。一般来说,第一个化合物或单质最难确定。因此要进行综合分析。
本题中,要熟知卤素及卤素离子的性质,还要熟悉浓硫酸的氧化性,如H2S2O3的不稳定性,Na2S2O3的还原性。
推测反应产物比写出相应反应的化学方程式容易些,本题中,写反应的化学方程式(3)、(6)较难,在化学方程式(6)中I-具有强还原性,浓硫酸具有强氧化性,这样反应产物才能生成H2S气体,把S从+6价还原为-2价。这就需要通过实验增强感性知识,需要对卤素离子Cl-、Br-、I-在酸性条件下与浓硫酸反应的情况有深入的了解。
解:A为KI,B为浓硫酸,C为I2,D为KI3,E为Na2S2O3,F为Cl2。
各步反应的化学方程式为:
(1)Ba2+ + SO![]() = BaSO4↓
= BaSO4↓
(2)S2O![]() + 2H+ = H2S2O3 H2S2O3 = S↓+ SO2↑+ H2O
+ 2H+ = H2S2O3 H2S2O3 = S↓+ SO2↑+ H2O
(3)S2O![]() + 4Cl2 + 5H2O = 2SO
+ 4Cl2 + 5H2O = 2SO![]() + 8Cl-+ 10H+
+ 8Cl-+ 10H+
(4)I2 + KI = KI3
(5)I![]() + 2 S2O
+ 2 S2O![]() = S4O
= S4O![]() + 3I-
+ 3I-
(6)8KI + 5H2SO4(浓)= 4K2SO4 + 4I2 + H2S + 4H2O


科目:高中化学 来源: 题型:阅读理解
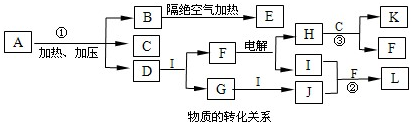


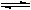 NH4++NH2-
NH4++NH2-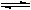 NH4++NH2-
NH4++NH2-查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
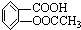 (相对分子质量为180).
(相对分子质量为180).

| 滴定次数 | 0.1mol/L盐酸读数/mL | |
| 滴定前 | 滴定后 | |
| 1 | 0.00 | 17.98 |
| 2 | 1.56 | 16.58 |
| 3 | 0.22 | 15.20 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源:江山市模拟 题型:填空题

查看答案和解析>>
科目:高中化学 来源:2011年浙江省衢州市江山市高考化学模拟试卷(解析版) 题型:填空题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com