
| 选项 | 二氧化碳 | 碳酸钠 | 转移的电子 |
| A | lmol | 2NA | |
| B | 22.4L | lmol | |
| C | 106g | lmol | |
| D | 106g | 2NA |
| A. | A | B. | B | C. | C | D. | D |
分析 由化学方程式:2Na2O2+2CO2═2Na2CO3+O2,根据质量差求出二氧化碳、碳酸钠的物质的量,进而求出碳酸钠的质量和转移的电子数.
解答 解:二氧化碳和过氧化钠反应,当固体质量增加28g时,设参与反应二氧化碳的物质的量为x,生成碳酸钠的物质的量为y,
2Na2O2+2CO2═2Na2CO3+O2 固体质量差
2mol 2mol 56g
x y 28g
$\frac{2mol}{x}$=$\frac{56g}{28g}$
解得:x=1mol,
$\frac{2mol}{y}$=$\frac{56g}{28g}$
解得y=1mol,
碳酸钠的质量=1mol×106g/mol=106g,
因常温常压下发生的反应,1mol二氧化碳的体积>22.4L;
由化学方程式可知;1mol二氧化碳参与反应转移1mol电子,即有 NA个电子转移;
故选C.
点评 本题主要考查化学方程式的书写、有关化学方程式的计算以及氧化还原反应中电子转移数目的计算,为高频考点,侧重于考查学生的计算能力,题目难度中等,答题时注意把握反应的特点,把握化合价的变化以及差量法的运用.


科目:高中化学 来源: 题型:多选题
| A. | 2 L溶液中Ba2+和Cl-的总数为0.8NA | |
| B. | 500 mL溶液中Cl-的浓度为0.2 mol•L-1 | |
| C. | 500 mL溶液中Ba2+的浓度为0.2 mol•L-1 | |
| D. | 500 mL溶液中Cl-的总数为0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Mg2+向正极迁移 | |
| B. | 正极反应为:Mo3S4+2xe-═Mo3S${\;}_{4}^{2{x}^{-}}$ | |
| C. | Mo3S4发生氧化反应 | |
| D. | 负极反应为:xMg-2xe-═xMg2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
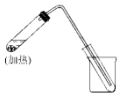 如图是用自来水制取少量蒸馏水的简易装置(加热及固定仪器略),其原理与教材中的实验完全相同.回答下列问题:
如图是用自来水制取少量蒸馏水的简易装置(加热及固定仪器略),其原理与教材中的实验完全相同.回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 漂白粉、漂粉精可用于饮用水及餐具等的消毒 | |
| B. | 福尔马林可用于食品的消毒,如浸泡海鲜,使其不易变质 | |
| C. | 药用酒精可用于食物及饮用水消毒 | |
| D. | 过氧乙酸无须稀释可直接使用消毒,不会对人体造成伤害 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 若在阴极附近的溶液中滴入紫色石蕊试液,溶液呈红色 | |
| B. | 若在阳极附近的溶液中滴入KI溶液,溶液呈棕色 | |
| C. | 电解时在阳极得到氯气,在阴极得到金属钠 | |
| D. | 电解一段时间后,将全部电解液转移到烧杯中,充分搅拌后溶液变回NaCl溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
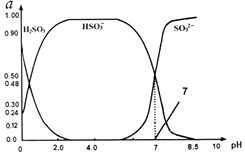 常温下0.1mol•L-1亚硫酸溶液中 H2SO3、HSO3-、SO32-三种微粒所占物质的量分数(a)随pH变化的关系如图所示.下列说法不正确的是( )
常温下0.1mol•L-1亚硫酸溶液中 H2SO3、HSO3-、SO32-三种微粒所占物质的量分数(a)随pH变化的关系如图所示.下列说法不正确的是( )| A. | 由图中数据可计算得到常温下亚硫酸溶液的Ka2 | |
| B. | 在0.1mol•L-1H2SO3溶液中,存在:c2(H+)=c(H+)•c(HSO3-)+2c(H+)•c(SO32-)+Kw | |
| C. | 向pH为7的溶液中滴入少量稀盐酸造成的溶液pH变化小于向pH为4.0的溶液中滴入相同量稀盐酸造成的溶液pH变化 | |
| D. | 在pH=2.0溶液中:c(H2SO3)>c(HSO3-)>c(H+)>c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | ① | ② | ③ | |||||
| 三 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ||
| 四 | ⑩ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com