
| A、14.2g | B、21.4g |
| C、5.8g | D、4g |
| 8.96L |
| 22.4L/mol |
| ||
| ||
| 8.96L |
| 22.4L/mol |
| ||
| ||
|
| 0.2 |
| 2 |


 优加精卷系列答案
优加精卷系列答案科目:高中化学 来源: 题型:
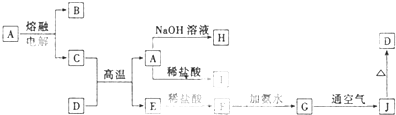
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、22g CO2与标准状况下11.2L HCl含有相同的分子数 |
| B、22.4L N2含有阿伏伽德罗常数个氮分子 |
| C、在标准状况下,22.4L水的质量为18g |
| D、32g O2占有的体积约为22.4L |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、常温常压下,33.6 L氯气与27 g铝充分反应,转移电子数为3NA |
| B、5.6 g铁与足量的稀硫酸反应,失去电子数为0.3NA |
| C、7.8克过氧化钠与足量的水反应,转移的电子总数为0.1 NA |
| D、1 L 1 mol?L-1 Na2CO3溶液中含有NA个CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、稀释浓硫酸时,应将浓硫酸沿杯壁缓慢倒入盛有水的烧杯中,并用玻璃棒搅拌散热 |
| B、常温下,铝遇浓硫酸、浓硝酸时发生钝化,可以用铝制容器贮存浓硫酸或浓硝酸 |
| C、工业上采用电解熔融MgO的方法制备金属Mg |
| D、往火柴杆上涂抹浓硫酸后出现发黑现象,说明浓H2SO4具有脱水性 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、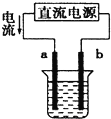 a为阳极,b为阴极 |
B、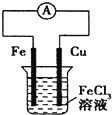 发生的总反应为:Cu+2Fe3+=2Fe2++Cu2+ |
C、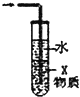 若X为四氯化碳,可用于吸收氨气或氯化氢,并防止倒吸 |
D、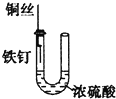 铁钉几乎不发生腐蚀 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①析出的氯化铵纯度更高 |
| B、①的滤液可直接循环使用 |
| C、②析出的氯化铵纯度不高 |
| D、②的滤液可直接循环使用 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com