
【题目】某兴趣小组用0.50 mol/L KI、0.2%淀粉溶液、0.20 mol/L K2S2O8、0.10 mol/L Na2S2O3等试剂,探究反应条件对化学反应速率的影响。
已知:S2O82-+2I-=2SO42-+I2(慢)
I2+2S2O32-=2I-+S4O62-(快)
(1)为探讨反应物浓度对化学反应速率的影响,设计的实验方案如下表:
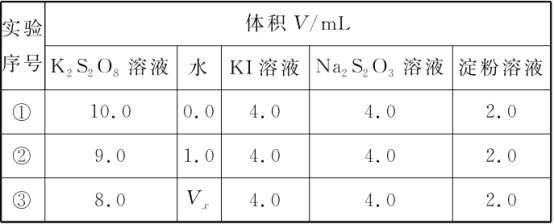
表中Vx=________mL,理由是__________。
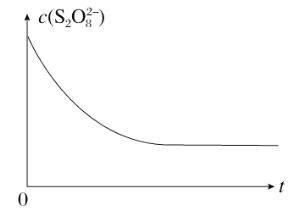
(2)已知某条件下,浓度c(S2O82-)~反应时间t的变化曲线如下图,若保持其他条件不变,请在坐标图中,分别画出降低反应温度和加入催化剂时c(S2O82-)~t的变化曲线示意图(进行相应的标注)。_______
【答案】V=2.0 仅使反应物S2O82-的浓度改变而其他物质浓度不变,才能得出合理的实验结论。 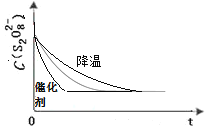
【解析】
(1)由于要保证反应物K2S2O8浓度改变,而其他的不变,才到达实验目的;
(2)降低温度反应速率降低,则需要的反应时间增加。催化剂能加快反应速率,需要的反应时间减少。
(1)由于要保证反应物K2S2O8浓度改变,而其他的不变,才到达实验目的,所以根据实验中的数据可知,溶液的总体积是20mL,因此Vx=20mL-8.0mL-4.0mL-4.0mL-2.0mL=2.0mL;
(2)降低反应温度,反应速率减慢,此时曲线应画在已知曲线的右边;加入催化剂,反应速率明显增大,此时曲线应画在已知曲线的左边,所以正确的图像是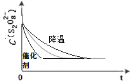 。
。


科目:高中化学 来源: 题型:
【题目】请回答氯碱工业的如下问题:
(1)氯气、烧碱是电解食盐水时按照固定的比率k(质量比)生成的产品。理论上k=_______(要求计算表达式和结果);
(2)原料粗盐中常含有泥沙和Ca2+、Mg2+、Fe3+、SO42-等杂质,必须精制后才能供电解使用。精制时,粗盐溶于水过滤后,还要加入的试剂分别为①Na2CO3、②HCl(盐酸)③BaCl2,这3种试剂添加的合理顺序是______________(填序号);
(3)氯碱工业是高耗能产业,一种将电解池与燃料电池相组合的新工艺可以节(电)能30%以上。在这种工艺设计中,相关物料的传输与转化关系如下图所示,其中的电极未标出,所用的离子膜都只允许阳离子通过。
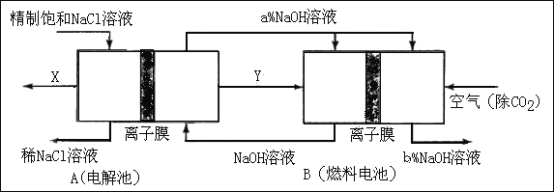
①图中X、Y分别是_____、_______(填化学式),分析比较图示中氢氧化钠质量分数a%与b%的大小_________;
②分别写出燃料电池B中正极、负极上发生的电极反应正极:______;负极:_____;
③这样设计的主要节(电)能之处在于(写出2处)____________、____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温时,1 mol·L-1的HClO2和1 mol·L-1的HMnO4两种酸溶液,起始时的体积均为V0,分别向两溶液中加水进行稀释,稀释后溶液体积为V,所得曲线如图所示。下列说法正确的是( )

A.在0≤pH≤5时,HMnO4溶液满足pH=lg![]() +1
+1
B.当稀释至pH均为3时,溶液中c(ClO2-)>c(MnO4-)
C.稀释前分别用1 mol·L-1的NaOH溶液中和,消耗的NaOH溶液体积:HMnO4>HClO2
D.当稀释至pH均为3时,HMnO4溶液中的V等于1000 V0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法错误的是![]()
![]()
A.近年屡屡引起热议的“抗糖”一词中的“糖”,指的是六大营养物质之一的糖类,由C、H、O三种元素组成
B.培育绣球花的过程中,土壤为酸性时花朵呈蓝色,土壤为碱性时花朵呈红色。为获得红色花朵,可施用硫酸铵
C.“自热火锅”极大的方便了人们的生活,自热包的主要成分为CaO,加水后反应放热,从而加热火锅
D.《神农本草经》中记载:“石膏,味辛,微寒,主中风寒热,心下逆气惊喘。“石膏”的化学式为CaSO4·2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用反应6NO2+8NH3=7N2+12H2O设计的电池装置如图所示,该装置既能有效消除氮氧化物的排放减轻环境污染,又能充分利用化学能。下列说法正确的是( )

A.电池工作时,OH—从左向右迁移
B.电极A上发生氧化反应,电极A为正极
C.当有0.1molNO2被处理时,外电路中通过电子0.4mol
D.电极B的电极反应式为2NO2+8e-+8H+=N2+4H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】标准状况下,三个烧瓶分别盛①混有空气的氨气、②等体积的二氧化氮与氧气的混合气、③二氧化氮,将它们分别倒置于盛足量水的水槽中,当水进入烧瓶中,并使气体充分溶解,假定烧瓶中溶液无损失,所得溶液的物质的量浓度之比为
A. 5:4:5 B. 1:1:1 C. 15: 12: 10 D. 无法计算
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图像符合题意的是
A.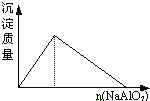 盐酸溶液中逐滴加入NaAlO2
盐酸溶液中逐滴加入NaAlO2
B.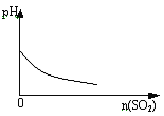 SO2气体逐渐通入溴水中
SO2气体逐渐通入溴水中
C.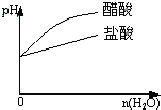 pH=1的醋酸与盐酸溶液分别加水稀释
pH=1的醋酸与盐酸溶液分别加水稀释
D.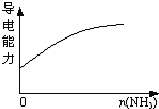 氨气逐渐通入醋酸中
氨气逐渐通入醋酸中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验装置正确且能达到目的的是
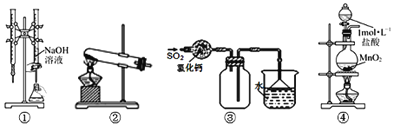
A.装置①可用于已知浓度的氢氧化钠溶液测定未知浓度盐酸的实验
B.装置②可用于氯化铵固体和氢氧化钙固体反应制取少量氨气
C.装置③可用于收集SO2,并吸收多余的SO2
D.装置④可用于制取少量Cl2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】正丁醛是一种化工原料。某实验小组利用如下装置合成正丁醛。

发生的反应如下:
CH3CH2CH2CH2OH![]() CH3CH2CH2CHO
CH3CH2CH2CHO
反应物和产物的相关数据列表如下:
沸点/℃ | 密度/(g·cm-3) | 水中溶解性 | |
正丁醇 | 117.2 | 0.8109 | 微溶 |
正丁醛 | 75.7 | 0.8017 | 微溶 |
实验步骤如下:
将6.0gNa2Cr2O7放入100mL烧杯中,加30mL水溶解,再缓慢加入5mL浓硫酸,将所得溶液小心转移至B中。在A中加入4.0g正丁醇和几粒沸石,加热。当有蒸汽出现时,开始滴加B中溶液。滴加过程中保持反应温度为90—95℃,在E中收集90℃以下的馏分。将馏出物倒入分液漏斗中,分去水层,有机层干燥后蒸馏,收集75—77℃馏分,产量2.0g。
回答下列问题:
(1)实验中,能否将Na2Cr2O7溶液加到浓硫酸中,说明理由_____。
(2)加入沸石的作用是_____。若加热后发现未加沸石,应采取的正确方法是______。
(3)上述装置图中,B仪器的名称是_____,D仪器的名称是_____。
(4)分液漏斗使用前必须进行的操作是_____(填正确答案标号)。
a.润湿 b.干燥 c.检漏 d.标定
(5)将正丁醛粗产品置于分液漏斗中分水时,水在_____层(填“上”或“下”)
(6)反应温度应保持在90—95℃,其原因是_____。
(7)本实验中,正丁醛的产率为_____%。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com