
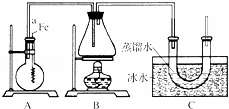
按如图所示的装置和以下实验步骤,可以制取少量的溴苯和溴乙烷.已知乙醇在一定条件下与氢溴酸反应可制备溴乙烷:
C2H5OH+HBr→C2H5Br+H2O
主要实验步骤如下:①连接好装置,检查装置的气密性;②向烧瓶中加入一定量的苯和液溴.向锥形瓶中加入乙醇和浓H2SO4的混合液至稍高于进气导管口处;③将A装置中的纯铁丝小心向下插入混合液中;④点燃B装置中的酒精灯,用小火缓缓对锥形瓶加热10min.
请填写下列空白:
(1)写出制取溴苯的化学方程式: .
(2)步骤③中观察到的现象是: .
(3)C装置中U形管内部用蒸馏水封住管底的作用是: .
(4)反应完毕后,U形管内的现象是: .分离溴乙烷时所用的最主要仪器的名称是(只填一种) .
(5)实验结束,从烧瓶的混合物中分离出粗制黄色的溴苯,产生黄色的原因是其中含有 (填化学式).欲得到无色的溴苯的方法是 (填试剂和操作名称).
考点: 性质实验方案的设计.
分析: (1)纯铁丝和溴反应生成三溴化铁,三溴化铁与苯作用,生成溴苯和铁,铁作催化剂,苯和液溴反应生成溴苯和溴化氢,据此书写方程式;
(2)苯与液溴发生取代反应,该反应为放热反应,溴和苯在烧瓶中变成蒸气;
(3)CH3CH2Br难溶于水,水可以阻止物质的溢出,起到水封的作用,C装置中U形管内部用蒸馏水封住管底可溶解吸收HBr,防止HBr及CH3CH2Br逸出;
(4)反应完毕,U形管内会发生液体分层现象;分液用到分液漏斗;
(5)常温下,氢氧化钠可以和溴单质反应生成溴化钠、次溴酸钠的水溶液,和溴苯不互溶,不反应,欲得到无色的溴苯的方法是用NaOH溶液洗涤分液.
解答: 解:(1)将A装置中的纯铁丝小心向下插入混合液中,铁和溴反应生成三溴化铁,2Fe+3Br2=2FeBr3,三溴化铁与苯作用,生成溴苯和铁,同时有溴化氢生成,铁作催化剂,所以制备溴苯的化学反应方程式为:C6H6+Br2 C6H5Br+HBr,
C6H5Br+HBr,
故答案为:C6H6+Br2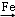 C6H5Br+HBr;
C6H5Br+HBr;
(2)苯和液溴在铁粉催化作用下发生取代反应生成溴苯和溴化氫,该反应为放热反应且反应剧烈,苯和溴单质沸点低,易挥发,溴蒸气为红棕色,所以步骤③中观察到的现象是:剧烈反应,瓶上方有红棕色气体产生,
故答案为:剧烈反应,瓶上方有红棕色气体产生;
(3)CH3CH2Br难溶于水,溴化氢极易溶于水,形成的氢溴酸是强酸,U形管内的蒸馏水用来溶解吸收HBr,防止HBr及CH3CH2Br逸出,
故答案为:一是溶解溴化氢、二是液封(防止产物及溴化氢挥发);
(4)溴乙烷是一种无色的油状液体物质,和水是互不相溶的,反应完毕,U形管内会发生液体分层现象,上层为水层,下层为无色油状液体(溴乙烷),可以采用分液的方法来实现物质的分离,最主要仪器为分液漏斗,
故答案为:U形管中蒸馏水底部有无色油状液体;分液漏斗;
(5)过量的溴溶解在溴苯中而使溴苯显黄色,常温下,氢氧化钠可以和溴单质反应,和溴苯不互溶,不反应,欲得到无色的溴苯可用NaOH溶液洗涤:2NaOH+Br2═NaBr+NaBrO+H2O,再用分液的方法分离,
故答案为:Br2;用NaOH溶液洗涤分液.
点评: 本题主要考查了苯的性质、溴苯和溴乙烷的制备,把握反应原理、实验装置的作用、现象与结论的分析等为解答的关键,平时须注意积累相关反应知识,侧重分析与实验能力的考查,题目难度中等.


 优等生题库系列答案
优等生题库系列答案科目:高中化学 来源: 题型:
下列微粒的核外电子的表示方法中正确的是( )
|
| A. | 碳原子 |
|
| B. | P原子价电子轨道表示式 |
|
| C. | Cr原子的价电子排布式3d44s1 |
|
| D. | Fe2+价电子排布式3d44s2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
3I﹣+S2O82﹣=I3﹣+2SO42﹣的反应速率可以用I3﹣与加入的淀粉溶液显蓝色的时间t来度量,t越小,反应速率越大.某探究性学习小组在20℃进行实验,得到的数据如下表:
| 实验编号 | ① | ② | ③ | ④ | ⑤ |
| c(I﹣)/mol•L﹣1 | 0.040 | 0.080 | 0.080 | 0.160 | 0.160 |
| c(S2O82﹣)/mol•L﹣1 | 0.040 | 0.040 | 0.080 | c1 | 0.080 |
| t/s | 88.0 | 44.0 | 22.0 | 22.0 | t2 |
下列说法不正确的是( )
|
| A. | 该实验的目的是探究I﹣与S2O82﹣浓度对反应速率的影响 |
|
| B. | 若在40℃下进行编号③对应浓度的实验,显色时间的范围为<22.0s |
|
| C. | 实验④c1=0.020 mol•L﹣1 |
|
| D. | 实验⑤显色时间t2=11 s |
查看答案和解析>>
科目:高中化学 来源: 题型:
将0.2mol两种气态组成的混合气完全燃烧后得到6.72升二氧化碳(标准状况下)和7.2克水,下列说法正确的是 ( )
A. 一定有乙烷 B. 一定有甲烷 C. 一定没有甲烷 D. 一定没有乙烷
查看答案和解析>>
科目:高中化学 来源: 题型:
以下有关元素性质的说法不正确的是( )
|
| A. | 具有下列电子式的原子中,①1s22s22p63s23p2②1s22s22p3③1s22s22p2④1s222s2p63s23p4原子半径最大的是① |
|
| B. | 下列原子的价电子排布中,①3s23p1②3s23p2③3s23p3④3s23p4对应的第一电离能最大是③ |
|
| C. | ①Na,K,Rb②N,P,As③O,S,Se④Na,P,Cl元素的电负性随原子序数增大而递增的是④ |
|
| D. | 某元素的逐级电离能分别为738、1451、7733、10540、13630、17995、21703,当它与氯气反应时可能生成的阳离子是X3+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
设NA代表阿伏加德罗常数的数值,下列说法中正确的是( )
|
| A. | 标准状况时,22.4L四氯化碳所含有的分子数为NA |
|
| B. | 34g H2O2中含有的非极性共价键数为 NA |
|
| C. | 碱性锌锰电池中,当有1.3g的锌消耗,则转移的电子数为0.002NA |
|
| D. | 将16gO2与64gSO2在一定的条件下充分反应生成的SO3分子数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
向紫色石蕊试液中加入过量的Na2O2粉末,振荡,观察不到的现象是( )
A.有大量气泡产生
B.溶液颜色先变为蓝色
C.最后溶液褪色
D.最后溶液变为蓝色
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com