
两份质量均为mg的Na2CO3、NaHCO3固体混合物,加热第一份充分反应得到CO2质量是xg,向加热后所得固体中加入足量的盐酸得到CO2 ag;向第二份中直接加入足量盐酸得到CO2的质量是bg.则x等于( )
A.2a B.2b C.b-a D.b-2a
 培优好卷单元加期末卷系列答案
培优好卷单元加期末卷系列答案 一线名师权威作业本系列答案
一线名师权威作业本系列答案科目:高中化学 来源:2015-2016学年甘肃省高二上期末考试化学试卷(解析版) 题型:选择题
甲烷和丙烷混合气的密度与同温同压下乙烷的密度相同,混合气中甲烷和丙烷的体积比是
A.2:1 B.3:1 C.1:3 D.1:1
查看答案和解析>>
科目:高中化学 来源:2016届宁夏中卫一中高三上学期期末理综化学试卷(解析版) 题型:填空题
工业上冶炼冰铜(mCu2O·nFeS)可得到粗铜,冰铜与酸反应可以生成硫化氢(见图1)。完成下列填空:
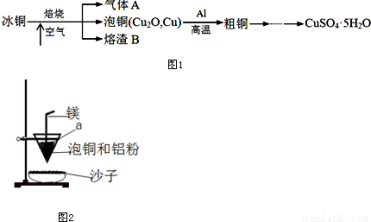
(1)气体A中的大气污染物可选用下列试剂中的________(填序号)吸收。
a.浓H2SO4 b.浓HNO3 c.NaOH溶液 d.氨水
(2)实验室可用如图2的装置完成泡铜冶炼粗铜的反应.
①泡铜冶炼粗铜的化学方程式是____________________;
②装置中镁带的作用是____________________;
③泡铜和铝粉混合物表面覆盖少量白色固体a,a是____________;
(3)将H2S和O2在密闭容器中点燃,充分反应后恢复到原来的温度和压强(120℃、101kPa),气体体积减少30%,求原混合其气体中H2S的体积分数.(不考虑H2S的自身分解)______________已知:氧气不足时:2H2S+O2  2S+2H2O 氧气足量时:2H2S+3O2═2SO2+2H2O;
2S+2H2O 氧气足量时:2H2S+3O2═2SO2+2H2O;
(4)已知:SiCl4(s)+H2(g)=SiHCl3(s)+HCl(g) △H1=47kJ/mol
SiHCl3(s)+H2(g)=Si(s)+3HCl(g) △H2=189kJ/mol
则由SiCl4制备硅的热化学方程式为____________________________。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年甘肃省高二上期末考试化学试卷(解析版) 题型:填空题
(1)2SO2(g)+O2(g) 2SO3(g)反应过程的能量变化如图所示。已知1mol SO2(g)氧化为1mol SO3(g)的ΔH= —99kJ/mol。
2SO3(g)反应过程的能量变化如图所示。已知1mol SO2(g)氧化为1mol SO3(g)的ΔH= —99kJ/mol。
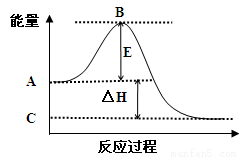 请回答下列问题:
请回答下列问题:
 ①图中A点表示:
①图中A点表示:
C点表示:
E的大小对该反应的反应热 (填“有”或“无”)影响。
 ②图中△H= kJ/mol。
②图中△H= kJ/mol。
(2)由氢气和氧气反应生成1 mol水蒸气,放出241.8 kJ热量(25℃、101 kPa下测得)
①写出该反应的热化学方程式:
②若1 mol水蒸气转化为液态水放热45kJ,则反应H2(g) +1/2O2(g) = H2O( l )的ΔH = kJ/mol。氢气的燃烧热为ΔH = kJ/mol。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年甘肃省高一上期末考试化学试卷(解析版) 题型:选择题
下列反应的离子方程式中,书写正确的是 ( )
A.钠跟水反应:Na + 2H2O = Na+ + 2OH- + H2↑
B.向硫酸溶液中加入Ba(OH)2溶液: H++SO42-+Ba2++OH- =H2O+BaSO4↓
C.向A12(SO4)3溶液中加入过量的氨水:A13++3NH3·H2O=A1(OH)3↓+3NH4+
D.FeCl2溶液跟Cl2反应:Fe2++Cl2 == Fe3++2Cl-
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河南省高一上期末考试化学试卷(解析版) 题型:选择题
根据气象台天气顶报,出现大雾天气将致使高速公路关闭,航班停飞.其中雾属于下列分散系中的( )
A.胶体 B.悬浊液 C.乳浊液 D.溶液
查看答案和解析>>
科目:高中化学 来源:2015-2016学年黑龙江省高一上期末化学试卷(解析版) 题型:实验题
制得的碳酸钠样品中往往含有少量NaCl,现欲测定样品中Na2CO3的质量分数,某探究性学习小组分别设计了如下实验方案。请回答下列有关问题:
方案一:把一定质量的样品溶解后加入过量的CaCl2溶液,将所得沉淀 (填操作名称)、洗涤、烘干、称量、计算。洗涤沉淀的具体操作是 。
方案二:把一定量的样品与足量硫酸反应后,用下图所示装置测定产生CO2的体积,为了确保测定结果的准确性,B中的溶液最好采用 。下图装置中实验仪器a的名称是 。
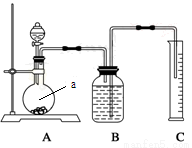
方案三:利用下图所示装置来测定纯碱样品中碳酸钠的质量分数(铁架台、铁夹等在图中均已略去)。实验步骤如下:
①按图连接装置,并检查气密性;
②准确称得盛有碱石灰的干燥管D的质量为33.4g;
③准确称得6g纯碱样品放入容器b中;
④打开分液漏斗a的旋塞,缓缓滴入稀硫酸,至不再产生气泡为止;
⑤打开弹簧夹,往试管A中缓缓鼓入空气数分钟,然后称得干燥管D的总质量为35.6g。
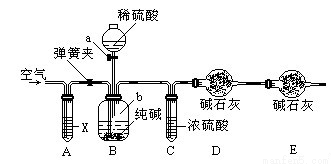
(1)若④⑤两步的实验操作太快,则会导致测定结果 (填“偏大”或“偏小”)。
(2)装置A中试剂X应选用 。
(3)E装置的作用是 。
(4)根据实验中测得的有关数据,计算纯碱样品Na2CO3的质量分数为 (结果保留小数点后一位)。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年黑龙江省高二上期末化学试卷(解析版) 题型:选择题
在恒温恒容密闭容器中,将CO和H2S混合并达到下列平衡:CO (g) +H2S (g)  COS (g) +H2 (g),平衡常数K=1,反应前CO的物质的量为l0mol,平衡后CO物质的量为8mol。下列说法正确的是( )
COS (g) +H2 (g),平衡常数K=1,反应前CO的物质的量为l0mol,平衡后CO物质的量为8mol。下列说法正确的是( )
A.若容器内压强不再变化,则说明该反应己达平衡
B.反应前H2S物质的量为2.5mol
C.CO和H2S达平衡后的转化率相同
D.若平衡后再加入CO,则正反应速率增大,逆反应速率减小
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖南省邵阳市高一上学期第三次月考化学试卷(解析版) 题型:选择题
下列说法中正确的是
A.玛瑙手镯、水晶项链、餐桌上的陶瓷碗盘都是硅酸盐制品
B.二氧化硅晶体广泛用于制作太阳能电池和光导纤维
C.制造水泥、玻璃的原料都有石灰石、纯碱、石英
D.粗硅制备单晶硅涉及氧化还原反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com