
将20mL0.4mol/L硝酸铵溶液跟50mL0.1mol/L氢氧化钡溶液混合,则混合溶液中粒子浓度间的关系正确的是( )
A.c(NO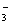 )>c(OH-)>c(NH
)>c(OH-)>c(NH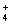 )>c(Ba2+) B.c(NO
)>c(Ba2+) B.c(NO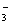 )>c(Ba2+)>c(NH
)>c(Ba2+)>c(NH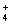 )>c(OH-)
)>c(OH-)
C.c(NO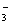 )=c(NH
)=c(NH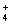 )+c(NH3·H2O)+c(NH3) D.2c(Ba2+)+c(H+)=c(NO
)+c(NH3·H2O)+c(NH3) D.2c(Ba2+)+c(H+)=c(NO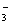 )+c(OH-)
)+c(OH-)
科目:高中化学 来源: 题型:
下列判断正确的是( )
A.向某溶液中加入AgNO3溶液生成白色沉淀,加入稀盐酸时沉淀不溶解,可确定溶液中有Cl-存在
B.对某溶液进行焰色反应时火焰颜色为黄色,则该溶液中一定有Na+,可能有K+
C.加入盐酸时有能使澄清石灰水变浑浊的气体生成,则原溶液中一定有大量的CO 存在
存在
D.分别含有Mg2+、Cu2+、Fe2+和Na+的四种盐溶液,只用NaOH溶液不能一次性鉴别出来
查看答案和解析>>
科目:高中化学 来源: 题型:
某酸的酸式盐NaHY在水溶液中,HY-的电离程度小于HY-的水解程度。有关叙述中正确的是 ( )
A.H2Y在电离时为:H2Y+H2O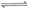 HY-+H3O+
HY-+H3O+
B.在该盐的溶液中,离子浓度为:C(Na+)>C(Y2-)>C(HY-)>C(OH-)>C(H+)
C.在该盐的溶液中,离子浓度为:C(Na+)>C(HY-)>C(Y2-)>C(OH-)>C(H+)
D.HY-水解方程式为:HY-+H2O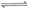 Y2-+H3O+
Y2-+H3O+
查看答案和解析>>
科目:高中化学 来源: 题型:
混合下列各组物质使之充分反应,加热蒸干产物并在300 ℃灼烧至质量不变,最终残留固体不是纯净物的是( )。
A.向红褐色的Fe(OH)3固体中加入过量盐酸
B.等物质的量浓度、等体积的(NH4)2SO4与BaCl2溶液
C.等物质的量的NaHCO3与Na2O2固体
D.向NaBr溶液中通入过量氯气
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组离子中,每个离子都能影响水的电离平衡的一组是( )
A.Zn2+、Ag+、HCO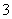 、Cl-、PO
、Cl-、PO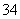 、SO
、SO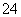 B.Fe3+、Br-、Al3+、H+、CO
B.Fe3+、Br-、Al3+、H+、CO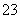 、H2PO
、H2PO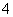
C.Ag+、SO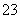 、SiO
、SiO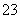 、Fe2+、S2- D.Fe2+、ClO-、NO
、Fe2+、S2- D.Fe2+、ClO-、NO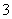 、HS-、Cu2+、HSO
、HS-、Cu2+、HSO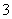
查看答案和解析>>
科目:高中化学 来源: 题型:
在常温下,下列五种溶液:①0.1 mol·L-1 NH4Cl ②0.1 mol·L-1 CH3COONH4
③0.1 mol·L-1 NH4HSO4 ④0.1 mol·L-1 NH3·H2O和0.1 mol·L-1 NH4Cl混合液
⑤0.1 mol·L-1 NH3·H2O。
请根据要求填写下列空白:
(1)溶液①呈________性(填“酸”、“碱”或“中”),其原因是________________________(用离子方程式表示)。
(2)在上述五种溶液中,pH最小的是________;c(NH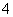 )最小的是________(填序号)。
)最小的是________(填序号)。
(3)比较溶液②、③中c(NH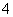 )的大小关系是②________③(填“>”“<”或“=”)。
)的大小关系是②________③(填“>”“<”或“=”)。
(4)在溶液④中,__________的浓度为0.1 mol·L-1;NH3·H2O和__________的物质的量浓度之和为0.2 mol·L-1。
(5)常温下,测得溶液②的pH=7,则说明CH3COO-的水解程度________(填“>”“<”或“=”)NH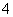 的水解程度,CH3COO-与NH
的水解程度,CH3COO-与NH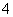 浓度的大小关系是:c(CH3COO-)________c(NH
浓度的大小关系是:c(CH3COO-)________c(NH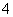 )(填“>”“<”或“=”)。
)(填“>”“<”或“=”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列所列各组物质中,物质之间通过一步反应就能实现如下图所示转化的是( )
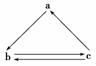
| 选项 | a | b | c |
| A | S | SO2 | SO3 |
| B | HNO3 | NO | NO2 |
| C | Si | SiO2 | H2SiO3 |
| D | NH3 | NO2 | NO |
查看答案和解析>>
科目:高中化学 来源: 题型:
化学与人类生活密切相关,下列与化学有关的说法不正确的是
A.化石燃料燃烧和工业废气中的氮氧化物均是导致“雾霾天气”的元凶
B.开发和推广新能源是实现低碳生活的途径之一
C.粮食酿酒主要经过了淀粉→葡萄糖→乙醇的化学变化过程
D.化学药品着火,都要立即用水或泡沫灭火器灭火
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、C、D四种物质均为下列离子组成的可溶性化合物,组成这四种物质的离子(离子不能重复组合)有:
| 阳离子 | Na+、Al3+、Ba2+、NH4+ |
| 阴离子 | Cl-、OH-、CO32-、SO42- |
分别取四种物质进行实验,实验结果如下:
①A、D溶液呈碱性,B呈酸性,C呈中性
②A溶液与B溶液反应生成白色沉淀,再加过量A,沉淀量减少,但不会完全消失
③A溶液与D溶液混合并加热有气体生成,该气体能使湿润的红色石蕊试纸变蓝
回答下列问题:
(1)A的化学式是_________,用电子式表示C的形成过程:________________ 。
(2)向A溶液中通入适量CO2,使生成的沉淀恰好溶解,所得溶液中各离子物质的量浓度由大到小的顺序是:________________________ 。
(3)写出③的离子方程式_______________________________________________ 。
(4)简述D溶液呈碱性的理由___________________________________________ 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com