
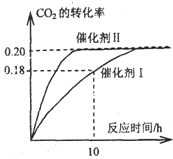
 I.已知CO2可以生产绿色燃料甲醇.CO2(g)+3H2(g)?CH3OH(g)+H2O(g);△H=-87.4kJ?mol-1.300℃时,在一定容积的密闭容器中,当c(CO2)=1.00kJ?mol-1、c(H2)=1.60kJ?mol-1开始反应,结果如图所示,回答下列问题:
I.已知CO2可以生产绿色燃料甲醇.CO2(g)+3H2(g)?CH3OH(g)+H2O(g);△H=-87.4kJ?mol-1.300℃时,在一定容积的密闭容器中,当c(CO2)=1.00kJ?mol-1、c(H2)=1.60kJ?mol-1开始反应,结果如图所示,回答下列问题:| 0.18mol/L |
| 10h |
| c(CH3OH)?c(H2O) |
| c(CO2)?c3(H2) |
| 0.2×0.2 |
| 0.8×1.03 |


科目:高中化学 来源: 题型:
| A、平均相对分子质量不再发生改变 |
| B、压强不再发生改变 |
| C、密度不再发生改变 |
| D、容器内的气体的颜色不再变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、化合物KCrO2中元素为+3价 |
| B、实验①证明Cr2O3是两性氧化物 |
| C、实验②证明氧化性:Cr2O72->I2 |
| D、实验③证明H2O2既有氧化性又有还原性 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、25℃时pH=12的NaOH溶液与pH=12的氨水中:c(Na+)>c(NH4+) |
| B、Na2CO3和NaHCO3混合溶液中一定有:2c(CO32-)+c(OH-)+c(HCO3-)=c(H+)+c(Na+) |
| C、pH=4的0.1mol?L-1的NaHA溶液中:c(HA-)>c(H+)>c(H2A)>c(A2-) |
| D、将①pH=2的CH3COOH溶液、②pH=2的盐酸、③0.01mol/L的氨水、④0.01mol/L的NaOH溶液,分别稀释100倍后溶液中的c(H+):②>①>④>③ |
查看答案和解析>>
科目:高中化学 来源: 题型:
 叠氮化钠(NaN3)是一种无色晶体,广泛用于汽车安全气囊及化工合成等.常见的两种制备方法为:
叠氮化钠(NaN3)是一种无色晶体,广泛用于汽车安全气囊及化工合成等.常见的两种制备方法为:查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
 A、B、C、D均为中学化学常见物质,且含有一种相同的元素,它们之间有如下转化关系,其中A是单质.
A、B、C、D均为中学化学常见物质,且含有一种相同的元素,它们之间有如下转化关系,其中A是单质.查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
 关于如图所示①、②两个装置的评价正确的是( )
关于如图所示①、②两个装置的评价正确的是( )| 选择 | 叙 述 | 评价 |
| A | 装置名称:①电解池,②原电池 | 错误 |
| B | 硫酸浓度变化:①增大,②减小 | 错误 |
| C | 电极反应式:①阳极:4OH--4e-═2H2O+O2↑ ②正极:Zn-2e-═Zn2+ | 正确 |
| D | 离子移动方向:①H+向阴极移动 ②H+向正极移动 | 正确 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com