
【题目】能直接实现下列物质间转化的元素是
单质![]() 氧化物
氧化物![]() 酸或碱
酸或碱![]() 盐.
盐.
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]() .
.
A.![]() B.
B.![]()
C.![]() D.
D.![]()
【答案】D
【解析】
![]() 碳燃烧生成二氧化碳,溶于水形成碳酸,碳酸与氢氧化钠反应生成碳酸钠,故
碳燃烧生成二氧化碳,溶于水形成碳酸,碳酸与氢氧化钠反应生成碳酸钠,故![]() 正确;
正确;
![]() 硫燃烧生成二氧化硫,溶于水形成亚硫酸,亚硫酸与氢氧化钠反应生成亚硫酸钠,故
硫燃烧生成二氧化硫,溶于水形成亚硫酸,亚硫酸与氢氧化钠反应生成亚硫酸钠,故![]() 正确;
正确;
![]() 磷与氧气反应生成五氧化二磷,五氧化二磷与水反应生成磷酸,磷酸与氢氧化钠反应生成磷酸钠等盐,故
磷与氧气反应生成五氧化二磷,五氧化二磷与水反应生成磷酸,磷酸与氢氧化钠反应生成磷酸钠等盐,故![]() 正确;
正确;
![]() 二氧化硅不能与水反应,可以用硅酸钠与酸反应得到硅酸,故
二氧化硅不能与水反应,可以用硅酸钠与酸反应得到硅酸,故![]() 错误;
错误;
![]() 钠与氧气反应生成氧化钠或过氧化钠,与水反应生成氢氧化钠,氢氧化钠与盐酸反应生成氯化钠,故
钠与氧气反应生成氧化钠或过氧化钠,与水反应生成氢氧化钠,氢氧化钠与盐酸反应生成氯化钠,故![]() 正确;
正确;
![]() 钙可以与氧气反应生成氧化钙、氧化钙与水反应生成氢氧化钙、氢氧化钙与盐酸反应生成氯化钙,故
钙可以与氧气反应生成氧化钙、氧化钙与水反应生成氢氧化钙、氢氧化钙与盐酸反应生成氯化钙,故![]() 正确;
正确;
![]() 金属铜和氧气反应生成氧化铜,但氧化铜不溶于水,故
金属铜和氧气反应生成氧化铜,但氧化铜不溶于水,故![]() 错误;
错误;
![]() 铝与氧气反应生成氧化铝,但氧化铝与水不反应,故
铝与氧气反应生成氧化铝,但氧化铝与水不反应,故![]() 错误;
错误;
故答案为D。


 寒假乐园北京教育出版社系列答案
寒假乐园北京教育出版社系列答案科目:高中化学 来源: 题型:
【题目】胡椒乙酸是合成许多药用生物碱的重要中间体,以苯酸为原料制备胡椒乙酸的合成路线如图所示。回答下列问题:
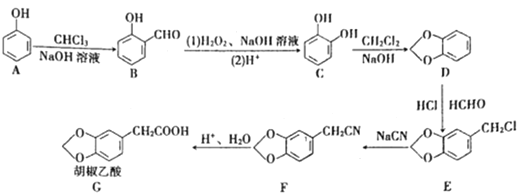
(1)下列关于有机物B的说法正确的是______![]() 填字母
填字母![]() 。
。
a.能与FeCl3溶液发生显色反应 b.核磁共振氢谱中只有3组峰
c.能发生银镜反应 d.能与溴水发生加成反应
(2)有机物C的名称是______,C→D的反应类型是______。
(3)胡椒乙酸(G)的分子式为______,G所含官能团的名称为______。
(4)E生成F的化学方程式为______。
(5)W是G的芳香族化合物同分异构体,0.5molW与足量碳酸氢钠溶液反应生成1molCO2,则W的结构共有______(不含立体异构)种,其中苯环上有2个取代基,且核磁共振氢谱有5组峰的结构简式为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是( )
A.过氧化钠的电子式是 Na+[:O:O:]2-Na+
B.原子最外层电子排布式为4s1和5s1 是同一主族元素
C.电负性差值大于 1.7 的化合物一定是离子化合物
D.配合物[Cu(H2O)4]SO4中,中心离子是Cu2+,配位体是H2O,配位数是 4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲、乙两化学活动小组对中学化学教材中“氨的催化氧化”进行了实验探究。
(1)甲小组设计了如下图所示的实验装置(固定装置已略去)。
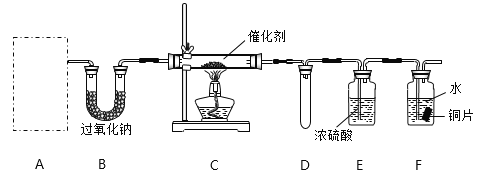
①若装置A中使用的药品是NH4HCO3固体,则A需要的仪器有试管、导管、橡胶塞和_______(填选项序号)。
a.锥形瓶 b.酒精灯 c.烧瓶 d.蒸发皿
②装置B的作用是___________________;装置D的作用是___________________。
③装置C中发生反应的化学方程式为________________________________。
④若A、B中药品足量,则可以观察到装置F中的实验现象是_____________________________。
⑤该装置存在的主要缺陷是___________________________________________________。
(2)乙小组认为可将甲小组的装置中A、B部分换成如图所示装置(其余部分相同)进行实验。
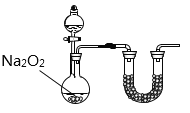
①烧瓶中加入的是过氧化钠固体,则分液漏斗中加入的最佳试剂是___________,U型管中加入的试剂是___________。
②此装置能产生大量氨气的原因是___________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】影响化学反应速率的因素很多,某化学小组用实验的方法进行探究。
Ⅰ.探究一:备选药品:镁片、铝片、0.500 mol·L-1H2SO4、18.4 mol·L-1H2SO4。
甲同学研究的实验报告:
实验步骤 | 现象 | 结论 |
①用砂纸打磨镁片和铝片; ②分别取等体积等浓度的硫酸于两支试管中; ③将镁片和铝片同时投入到试管中。 | 金属的性质越活泼, 反应速率越快 |
(1)甲同学用砂纸打磨镁片和铝片的原因是______________________________;选择H2SO4浓度为________________。
(2) 实验报告中现象为_______________________________________________。
Ⅱ.探究二:实验室经常用Na2S2O3与H2SO4的反应探究化学反应速率的影响因素,利用图1所示装置(夹持装置略去)进行实验,观察到锥形瓶底部有淡黄色浑浊。
(3)请用化学方程式表示出实验原理_________________________________,乙同学在实验过程中对产生的气体进行收集,并在2min内6个时间点对注射器内气体进行读数,记录数据并绘制出图像(如图2)。

0~20s内反应速率υ1=__________mL·s-1,80~100s内反应速率υ2=__________mL·s-1。不考虑实验测量误差,分析速率差异的主要原因是_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】四种短周期主族元素 X、Y、Z、W 的相对位置如表,元素 X 的原子核外电子数是 Z的 2 倍。下列说法不正确的是

A. W 元素的简单气态氢化物的热稳定性比 Z 元素的简 单气态氢化物的高
B. 气体分子(ZW)2 的结构式为 N≡C—C≡N
C. X、Y、W 三种元素的简单离子半径最大的是 Y
D. 元素 X 位于周期表中第三周期、第ⅡA族,其单质制备可用电解熔融 XCl2 的方法。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列事实不能用勒夏特列原理解释的是 ( )
A.氯水中存在Cl2+H2O![]() H++Cl-+HClO,当加入AgNO3溶液后,溶液颜色变浅
H++Cl-+HClO,当加入AgNO3溶液后,溶液颜色变浅
B.分别用等体积的蒸馏水和0.010mol/L硫酸洗涤BaSO4沉淀,后者损失的BaSO4沉淀少
C.SO2催化氧化成SO3的反应,往往需要使用催化剂
D.工业上生产硫酸的过程中使用过量的空气以提高二氧化硫的利用率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究小组为探究铁发生电化学腐蚀的影响因素,将混合均匀的新制铁粉和碳粉置于锥形瓶底部,塞上瓶塞(如图甲)从胶头滴管中滴入几滴醋酸溶液,同时测量容器中的压强变化结果如图,下列叙述错误的是( )
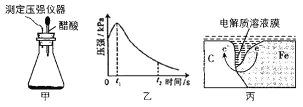
A.图丙中,发生腐蚀时电子转移方向如箭头所示
B.图乙中,t2时容器中压强明显小于起始压强是因为铁粉发生了吸氧腐蚀
C.碳粉表面的电极反应式只有:O2+4e-+2H2O=4OH-
D.若将丙图中的C 换成Zn,铁的腐蚀速率会大大降低,这是是利用了牺牲阳极的阴极保护法
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某密闭容器中充入等物质的量的A和B,一定温度下发生反应A(g)+xB(g) ![]() 2C(g),达到平衡后,在不同的时间段内反应物的浓度随时间的变化如图甲所示,正逆反应速率随时间的变化如图乙所示,下列说法中正确的是( )
2C(g),达到平衡后,在不同的时间段内反应物的浓度随时间的变化如图甲所示,正逆反应速率随时间的变化如图乙所示,下列说法中正确的是( )
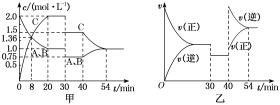
A.30~40 min间该反应使用了催化剂
B.化学方程式中的x=1,正反应为吸热反应
C.30 min时降低温度,40 min时升高温度
D.8 min前A的平均反应速率为0.08 mol·L-1·min-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com