
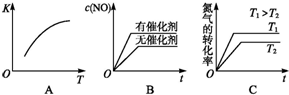
 汽车尾气里含有NO气体是由于内燃机燃烧的高温引起氮气和氧气反应所致:N2(g)+O2(g)?2NO(g)△H>0已知该反应在2404℃时,平衡常数K=64×10-4.请回答:
汽车尾气里含有NO气体是由于内燃机燃烧的高温引起氮气和氧气反应所致:N2(g)+O2(g)?2NO(g)△H>0已知该反应在2404℃时,平衡常数K=64×10-4.请回答:分析 (1)5分钟内,△n(O2)=1mol-0.5mol=0.5mol,由N2(g)+O2(g)?2NO(g),可知△n(N2)=0.5mol,再根据v=$\frac{\frac{△n}{V}}{△t}$计算v(N2);
(2)可逆反应到达平衡时,同种物质的正逆速率相等,各组分的浓度、含量保持不变,由此衍生的其它一些量不变,判断平衡的物理量应随反应进行发生变化,该物理量由变化到不变化说明到达平衡;
(3)A.该反应的正反应为吸热反应,则升高温度平衡向正反应进行,平衡常数增大;
B.加入催化剂,反应速率增大,但平衡不发生移动;
C.升高温度,反应速率增大,平衡向正反应方向移动,氮气的转化率增大;
(4)达到平衡状态后再向其中充入一定量NO等效为在原平衡的基础上增大压强,反应前后气体的物质的量不变,平衡不移动,平衡时相同物质的体积分数相等;
(5)计算此时浓度商Qc,若Qc=K,处于平衡状态,若Qc<K,反应向正反应进行,若Qc>K,反应向逆反应进行.
解答 解:(1)5分钟内,△n(O2)=1mol-0.5mol=0.5mol,由N2(g)+O2(g)?2NO(g)可知△n(N2)=0.5mol,v(N2)=$\frac{\frac{0.5mol}{2L}}{5min}$═0.05mol/(L•min),
故答案为:0.05mol/(L•min);
(2)A.消耗1mol N2等效于消耗1mol O2,同时生成1mol O2,到达平衡状态,故A正确;
B.混合气体总质量不变,容器容积不变,混合气体密度始终不变,故B错误;
C.混合气体总质量不变,反应前后气体物质的量不变,混合气体平均相对分子质量始终不变,故C错误;
D.由方程式可知2v(N2)正=v(NO)正,而2v正(N2)=v逆(NO),则v正(NO)=v(NO)逆,处于平衡状态,故D正确,
故选:AD;
(3)A.该反应的正反应为吸热反应,则升高温度平衡向正反应进行,平衡常数增大,故A正确;
B.加入催化剂,反应速率增大,但平衡不发生移动,NO浓度不变,故B错误;
C.升高温度,反应速率增大,平衡向正反应方向移动,氮气的转化率增大,故C正确,
故答案为:AC;
(4)达到平衡状态后再向其中充入一定量NO等效为在原平衡的基础上增大压强,反应前后气体的物质的量不变,平衡不移动,平衡时相同物质的体积分数相等,此时平衡混合气中NO的体积分数不变,
故答案为:不变;
(5)该温度下,某时刻测得容器内N2、O2、NO的浓度分别为2.5×10-1mol/L、4.0×10-2mol/L和3.0×10-3mol/L,浓度商Qc=$\frac{(3×1{0}^{-3})^{2}}{0.25×0.04}$=9×10-4<K=64×10-4,则反应应向正反应方向进行,
故答案为:向正反应方向进行;浓度商Qc=$\frac{(3×1{0}^{-3})^{2}}{0.25×0.04}$=9×10-4<K=64×10-4.
点评 本题考查化学平衡的有关计算及影响因素、平衡状态判断、化学平衡图象、平衡常数等,题目难度中等,注意平衡常数的计算和应用.


 开心蛙状元测试卷系列答案
开心蛙状元测试卷系列答案科目:高中化学 来源: 题型:解答题
 碘化钠是制备无机和有机碘化物的原料,在医药上用做祛痰剂和利尿剂等.工业上用铁屑还原法制备NaI,其主要流程如图,请回答下列问题:
碘化钠是制备无机和有机碘化物的原料,在医药上用做祛痰剂和利尿剂等.工业上用铁屑还原法制备NaI,其主要流程如图,请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| Al(OH)3 | Fe(OH)2 | Fe(OH)3 | |
| 开始沉淀时 | 3.4 | 6.3 | 1.5 |
| 完全沉淀时 | 4.7 | 8.3 | 2.8 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 族 周期 | I A | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | O |
| 1 | A | |||||||
| 2 | D | E | G | I | ||||
| 3 | B | C | F | H |
 .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③⑤⑥ | B. | ①②④⑥ | C. | ①③⑤⑦ | D. | ①③⑥⑧ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1:2:3 | B. | 2:1:1 | C. | 4:2:1 | D. | 1:2:4 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 采用“绿色化学”工艺,使原料尽可能转化为所需要的物质 | |
| B. | 减少直至不使用对大气臭氧层起破坏作用的氟氯烃 | |
| C. | 大量开采地下水,以满足社会对水的需求 | |
| D. | 节约能源,提高能利用率 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 托盘上各放一张滤纸,然后在右盘上添加2g砝码,称取2.0gNaOH固体 | |
| B. | 保存FeSO4溶液时,可以加入铁钉或铁粉来防止Fe2+被氧化 | |
| C. | 向沸水中边滴加FeCl3溶液边用玻璃棒搅拌,可制得Fe(OH)3胶体 | |
| D. | 检验红砖中的红色物质是否是Fe2O3的操作步骤为:样品→粉碎→加水溶解→过滤→向滤液中滴加KSCN溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com