
【题目】某学习小组用如图所示装置测定铝镁合金中铝的质量分数和铝的相对原子质量。

(1)A中试剂为____________________。
(2)实验前,先将铝镁合金在稀酸中浸泡片刻,其目的是____________________。
(3)检查气密性,将药品和水装入各仪器中,连接好装置后,需进行的操作还有:
①记录C的液面位置;②由A向B中滴加足量试剂;
③将B中剩余固体过滤,洗涤,干燥,称重;
④待B中不 再有气体产生并恢复至室温后,记录C的液面位置;
上述操作的顺序是_________(填序号);记录C的液面位置时,应________________ ,读数时视线_______。
(4)B中发生反应的离子方程式为____________________________________ 。
(5)若实验用铝镁合金的质量为m g,测得氢气体积为a mL(已换算为标准状况), B中剩余固体的质量为n g,则铝的相对原子质量为_____
(6)实验过程中,若未洗涤过滤所得的不溶物,则测得铝的质量分数将________。(填“偏大”、“偏小”或“不受影响”)
【答案】NaOH溶液 除去铝镁表面的氧化膜 ①②④③ 使D和C的液面相平 平视 2Al+2NaOH+2H2O===2NaAlO2+3H2↑ 33600(m-n)/a 偏小
【解析】
(1) 观察实验装置图可知是用排水量气法完成实验目的,铝镁合金中铝与氢氧化钠溶液反应放出氢气;(2)铝镁表面的氧化膜能与酸溶液反应;(3)根据排水量气法分析;(4)B中铝与氢氧化钠反应生成偏铝酸钠和氢气;(5)铝的质量=m-n,根据化学方程式计算铝的相对分子质量;(6)实验过程中,若未洗涤过滤所得的不溶物,则合金中镁的质量偏大。
(1) 观察实验装置图可知是用量气法完成实验目的,铝镁合金中只有铝与氢氧化钠溶液反应,所以A中应盛NaOH溶液;(2)铝镁表面的氧化膜能与酸溶液反应,先将铝镁合金在稀酸中浸泡片刻,其目的是除去铝镁表面的氧化膜;(3)在实验前应检验装置气密性,并记录C中液面位置,再由A向B中加入足量NaOH溶液,直到反应结束,并且恢复到室温,再次记录C中液面位置,最后将剩余固体洗涤、干燥、称重,故顺序为①②④③;读数时除了视线平视外,还要注意C、D两管内液面相平,不要产生液面差,影响读数。(4)B中铝与氢氧化钠反应生成偏铝酸钠和氢气,反应化学方程式是2Al+2NaOH+2H2O===2NaAlO2+3H2↑;(5)设铝的相对分子质量为M
2Al+2NaOH+2H2O===2NaAlO2+3H2↑
2mol 67.2L
![]()
![]()
![]()
M=33600(m-n)/a
(6)实验过程中,若未洗涤过滤所得的不溶物,则合金中镁的质量偏大,所以铝的质量分数将偏小。


 举一反三期末百分冲刺卷系列答案
举一反三期末百分冲刺卷系列答案科目:高中化学 来源: 题型:
【题目】下列根据实验现象所得出的结论中,正确的是( )
A. 无色溶液中加入稀盐酸产生无色无味气体,该气体能使澄清石灰水变浑浊,结论:原溶液可能含有CO32-
B. 某物质焰色反应呈黄色,结论:该物质是钠盐
C. 无色试液加入NaOH溶液,加热产生的气体使红色石蕊试纸变蓝,结论:试液中含NH3
D. 无色溶液中加入BaCl2溶液有白色沉淀产生,再加盐酸,沉淀不消失,结论:原溶液一定含有SO42-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海带中富含碘元素.从海带中提取碘有如下步骤:( ) ①将海带焙烧成灰(生成KI) ②加水使KI溶解,充分搅拌后过滤 ③在滤液通入足量Cl2
④加CCl4振荡 ⑤静置后,用分液漏斗分液 合理的操作顺序是.
A.①②③④⑤
B.②⑤①③④
C.①③⑤②④
D.②①③⑤④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇(CH3OH)是重要的有机化工原料,可用于制取氢气、甲酸甲酯(HCOOCH3)。(1) 在一定条件下用氧气催化氧化甲醇制氢气,原料气中n(O2)/n(CH3OH)对反应的选择性影响如图所示(选择性越大表示生成的该物质越多)。当n(O2)/n(CH3OH)=0.25 时,主要反应的化学方程式为____________,制备H2 时最好控制n(O2)/n(CH3OH)=___________。
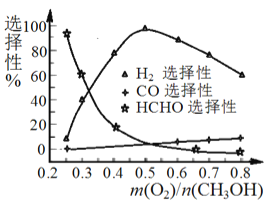
(2)甲醇催化脱氢制甲酸甲酯的反应为:2CH3OH(g)![]() HCOOCH3(g)+2H2(g) △H =a kJ·mol-1
HCOOCH3(g)+2H2(g) △H =a kJ·mol-1
①已知 :CO(g)+ l/2O2(g)=CO2(g) △H1 =-283kJ·mol-1
2CH3OH(g)+O2(g)=2CO2(g)+4 H2(g) △H2 =-386kJ·mol-1
2CO(g)+2 H2(g)=HCOOCH3(g ) △H3 =-134kJ·mol-1
a=_________________。
②在310℃下,将2mol 甲醇置于VL恒容密闭容器中,反应20 分钟后到达平衡,平衡时甲醇和氢气的分压相等。从开始到平衡时甲醇的平均反应速率为____ mol·L-1·min-1,若平衡时气体总压为P总=5×104Pa,Kp=_______。(已知: Kp是用平衡气体分压代替平衡浓度求得的平衡常数。气体分压=气体总压×气体的物质的量分数)。若在310℃下,将2mol 甲醇置于VL恒压密闭容器中,反应到达平衡时甲醇的分压______氢气的分压(填“>”,“=”或“<”)。
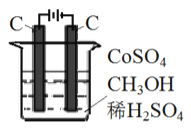
(3) 电解法可消除甲醇对水质造成的污染,原理是: 通电将Co2+ 氧化成Co3+,然后Co3+将甲醇氧化成CO2和H+(用石墨烯吸附除去Co2+)。现用如图所示装置模拟上述过程,请写出:
①阴极的电极反应式_______________________________________。
②除去甲醇的离子方程式为_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家发现对冶金硅进行电解精炼提纯可降低高纯硅制备成本。相关电解槽装置如图所示,用Cu-Si合金作硅源,在950℃利用三层液熔盐进行电解精炼,有关说法不正确的是
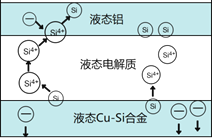
A. 在该液相熔体中Cu优先于Si被氧化,Si4+优先于Cu2+被还原
B. 电子由液态Cu-Si合金流出,从液态铝流入
C. 三层液熔盐的作用是增大电解反应面积,提高硅沉积效率
D. 电流强度不同,会影响硅提纯速率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】汽车剧烈碰撞时,安全气囊中发生反应:10NaN3+2KNO3=K2O+5Na2O+16N2↑下列说法正确的是( )
A. KNO3是还原剂,其中氮元素被氧化
B. 生成物中的N2是氧化产物,K2O是还原产物
C. 每转移1 mol电子,可生成N2的体积为35.84 L
D. 若有65 g NaN3参加反应,则被氧化的N的物质的量为3 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】英国曼彻斯特大学科学家安德烈·海姆和康斯坦丁·诺沃肖洛夫。共同工作多年的二人因“突破性地”用撕裂的方法从石墨中成功获得超薄材料石墨烯而获奖。制备石墨烯方法有石墨剥离法、化学气相沉积法等。石墨烯的球棍模型示意图如图:

(1)下列有关石墨烯说法正确的是______。
a.12 g石墨烯含![]() 键数为NA
键数为NA
b.石墨烯分子中所有原子可以处于同一平面
c.从石墨剥离得石墨烯需克服石墨层与层之间的分子间作用力
d.石墨烯中每个C原子连接3个六元环,每个六元环占有6个C原子
(2)化学气相沉积法是获得大量石墨烯的有效方法之一,催化剂为金、铜、钴等金属或合金,含碳源可以是甲烷、乙炔、苯、乙醇或酞菁等中的一种或任意组合。
①基态铜原子能量最高的电子占据的能级符号是_____;第四周期元素中,最外层电子数与铜相同的元素还有______。
②下列分子属于非极性分子的是______。
a.甲烷 b.二氯甲烷 c.苯 d.乙醇
③乙醇的沸点要高于相对分子质量比它还高的丁烷,请解释原因______。
④酞菁与酞菁铜染料分子结构如下图1,酞菁分子中碳原子采用的杂化方式是______。

⑤金与铜可形成的金属互化物合金(如上图2),它的化学式可表示为______;在Au周围最近并距离相等的Cu有______个,若2个Cu原子核的最小距离为d pm,该晶体的密度可以表示为______g/cm3。(阿伏加德罗常数用NA表示)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com