
【题目】(一)镓、硒、硅等元素的化合物是生产第三代太阳能电池的重要材料。已知:SeO2在常温下是白色的晶体,熔点为340-350℃,则SeO2晶体属于____晶体,SeO2中Se原子采取的杂化类型为___。
(二)A、X、Y、Z、W、M、G等原子序数一次增大的前四周期元素
元素 | 相关信息 |
A | 原子核外电子总数与其周期数相同 |
X | 其羞态原子的L层中有3个未成对电子 |
Y | 荃态原子的2p轨道上有一个电子的自旋方向与2p轨道上其它电子的自旋方向相反 |
Z | 原子核外p电子数比s电子数多l个 |
W | 原子的第一至第四电离能(kJ·mol-1)分别是:I1=578,I2=1817 I3=2745 I4=11575 |
M | 元素的主族数与周期数相差4 |
G | 其基态原子最外层电子数为1,其余各电子层均充满电子 |
(1)画出W基态原子的核外电子排布图______。
(2)A2Y的VSEPR模型名称为____。
(3)已知为X2Y分子中Y原子只与一个X原子相连,请根据等电子原理,写出X2Y的电子式____。
(4)X、G形成的某种化合物的晶胞结构如图所示,则其化学式为______。

(5)已知Z和M形成的化合物的晶体密度为pg·cm-3,阿伏加德罗常效为NA,该晶体中两个距离最近的Z离子中心间距离为_____cm。
【答案】分子 sp2 ![]() 四面体
四面体 ![]() Cu3N
Cu3N 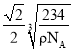
【解析】
(1)SeO2在常温下是白色的晶体,熔点为340-350℃,熔点低,为分子晶体,SeO2中Se原子价层电子对=2+![]() (6-2×2)=3,Se原子采取的杂化类型为sp2杂化,故答案为:分子,sp2。
(6-2×2)=3,Se原子采取的杂化类型为sp2杂化,故答案为:分子,sp2。
(二)有A、X、Y、Z、W、M、G等原子序数依次增大的前四周期元素,A原子核外电子总数与其周期数相同,则A是H;X基态原子的L层中有3个未成对电子,所以X是N;Y基态原子的2p轨道上有一个电子的自旋方向与2p轨道上其它电子的自旋方向相反,所以Y是O;Z原子核外p电子数比s电子数多l个,则Z是Na;W原子的第一至第四电离能(kJ·mol-1)分别是:I1=578,I2=1817,I3=2745,I4=11575,这说明最高价是+3价,则W是Al;M元素的主族数与周期数相差4,则M是Cl;G基态原子最外层电子数为1,其余各电子层均充满电子,因此G是Cu。
(1)基态铝原子的核外电子数是13,则其核外电子排布图为![]() ,故答案为:
,故答案为:![]() 。
。
(2)H2O分子中O的价层电子对数=2+(6-2×1)/2=4,所以VSEPR模型名称为四面体,故答案为:四面体。
(3)已知为N2O分子中O原子只与一个N原子相连,与CO2互为等电子体,则其电子式为![]() ,故答案为:
,故答案为:![]() 。
。
(4)根据晶胞结构可知N原子个数=8×1/8=1,Cu原子个数=12×1/4=3,因此其化学式为Cu3N,故答案为:Cu3N。
(5)氯化钠晶体密度为pg·cm-3,阿伏加德罗常效为NA,该晶体中两个距离最近的钠离子中心间距离为面对角线的一半。晶胞中含有离子的个数均是4个,则晶胞边长是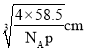 ,则晶体中两个距离最近的钠离子中心间距离为
,则晶体中两个距离最近的钠离子中心间距离为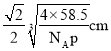 ,故答案为:
,故答案为: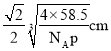 。
。


科目:高中化学 来源: 题型:
【题目】以黄铜矿(主要成分为 CuFeS2,含少量杂质SiO2等)为原料,进行生物炼铜,同时得到副产品绿矾(FeSO4·7H2O)。其主要工艺流程如下:
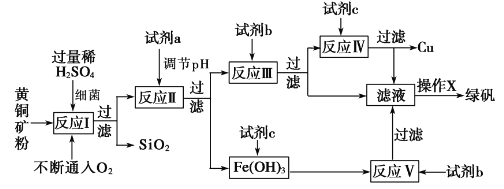
已知:部分阳离子以氢氧化物形式开始沉淀和完全沉淀时溶液的pH如下表。
沉淀物 | Cu(OH)2 | Fe(OH)3 | Fe(OH)2 |
开始沉淀pH | 4.7 | 2.7 | 7.6 |
完全沉淀pH | 6.7 | 3.7 | 9.6 |
下列说法不正确的是
A. 试剂a可以是CuO或Cu(OH)2,作用是调节pH至3.7~4.7之间
B. 反应I的化学反应方程式为4 CuFeS2+2H2SO4+17O2=4CuSO4+2Fe2(SO4)3+2H2O,该反应中铁元素被还原
C. 操作X为蒸发浓缩至溶液表面出现晶膜,再冷却结晶
D. 反应Ⅲ的离子方程式为Cu2++Fe==Cu+Fe2+,试剂c参与反应的离子方程式分别为Fe+2H+=Fe2++H2↑,Fe(OH)3+3H+=Fe 3++3H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】聚合物G可用于生产全生物降解塑料,在“白色污染”日益严重的今天有着重要的作用。有关转化关系如下:
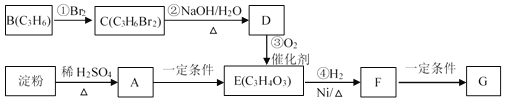
已知:CH3CH2CH2Br + NaOH![]() CH3CH2CH2OH + NaBr
CH3CH2CH2OH + NaBr
请回答下列问题:
(1)物质A的分子式为_______,B的结构简式为_______;
(2)请写出F中含氧官能团的名称_______;
(3)反应①~④中属于加成反应的是_______;
(4)写出由F生成聚合物G的化学方程式_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为某植物叶绿体结构和功能的示意图。请分析回答问题:
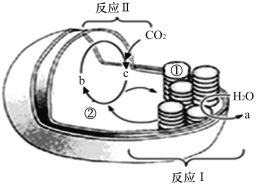
(1)物质a是____________,物质b是________________。
(2)光合作用的光反应阶段发生在_______(填“Ⅰ”或“Ⅱ”),该反应将光能转变为__________________。
(3)叶绿体增加膜面积的方式是____________________________________。在适宜光照和温度条件下培养,由①处转移至②处的物质主要是_____________________。
(4)该植物进行光合作用时,突然停止光照,C3的含量__________(填“升高”或“降低”或“不变”)。若用H![]() O培养该植物,发现叶肉细胞中出现了(CH
O培养该植物,发现叶肉细胞中出现了(CH![]() O),分析其最可能的转化途径是:_______________________(用相关物质、过程和箭头表示)。
O),分析其最可能的转化途径是:_______________________(用相关物质、过程和箭头表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质的转化在给定条件下能实现的是( )
①Fe![]() Fe2O3
Fe2O3![]() Fe2(SO4)3
Fe2(SO4)3
②SiO2![]() Na2SiO3
Na2SiO3![]() H2SiO3
H2SiO3
③AlCl3![]() Al
Al![]() NaAlO2
NaAlO2
④Na![]() Na2O
Na2O![]() NaOH
NaOH
⑤SO2![]() H2SO3
H2SO3![]() H2SO4
H2SO4
⑥饱和NaCl(ag)![]() NaHCO3
NaHCO3![]() Na2CO3
Na2CO3
A. ①②⑤B. ②③⑥C. ②⑤⑥D. ①③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】人体血液内的血红蛋白(Hb)易与O2结合生成HbO2,因此具有输氧能力,CO吸入肺中发生反应:CO+HbO2![]() O2+HbCO,37 ℃时,该反应的平衡常数K=220。HbCO的浓度达到HbO2浓度的0.02倍,会使人智力受损。据此,下列结论错误的是( )
O2+HbCO,37 ℃时,该反应的平衡常数K=220。HbCO的浓度达到HbO2浓度的0.02倍,会使人智力受损。据此,下列结论错误的是( )
A. 当吸入的CO与O2浓度之比大于或等于0.02时,人的智力才会受损
B. 人体吸入的CO越多,与血红蛋白结合的O2越少
C. CO与HbO2反应的平衡常数K=![]()
D. 把CO中毒的病人放入高压氧仓中解毒,其原理是使上述平衡向左移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求回答下列问题:
(1) CH2=CHCH=CH2的系统命名为______________;
(2)3—甲基—2一戊烯的结构简式为______________;
(3)![]() 的分子式为______________;
的分子式为______________;
(4)某烃的分子式为C4H4,它是合成橡胶的中间体,它有多种同分异构体
①试写出它的一种链式结构的同分异构体的结构简式______________.
②它有一种同分异构体,每个碳原子均达饱和,且碳与碳的夹角相同,该分子中碳原子形成的空间构型为______________形
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硝酸工业尾气中的氮氧化合物NOx(NO、NO2、N2O4)常用的处理方法有以下两种:
①碱液(Na2CO3或NaOH溶液)吸收法。用Na2CO3溶液吸收反应原理如下:
NO + NO2 + Na2CO3 == 2NaNO2 + CO2;2NO2 + Na2CO3 == NaNO2 + NaNO3 + CO2
②氨的催化氧化法,反应原理是:NOx + NH3![]() N2 + H2O
N2 + H2O
现将标准状况下2.016 L氮氧化合物NOx 通入50 mL 1.0 mol·L-1的Na2CO3溶液,恰好反应完全,且测得反应后溶液中n(NO2-)∶n(NO3-) = 4∶1,下列说法正确的是
A. 混合气体中V(N2O4) = 0.336 L
B. 混合气体中n(NO)∶n(NO2) = 1∶5
C. NOx能够完全被Na2CO3溶液吸收,则x ≤ 1.5
D. 如采用氨的催化氧化法处理,理论消耗n(NH3) = ![]() mol
mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一块金属钠投入到滴有紫色石蕊试液的盛冷水的烧杯中,甲同学认为可观察到下列现象,其中正确的有( )
①钠投入水中,先沉入水底,后浮出水面
②钠立即与水反应,并有气体产生
③反应后溶液变红
④钠熔成闪亮的小球
⑤小球在水面上四处游动
⑥有“嘶嘶”的响声发出
A. ①②③④ B. ②③④⑤
C. ②④⑤⑥ D. ③④⑥
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com