
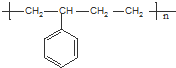
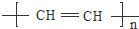
 的单体是
的单体是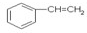 ;CH2=CH2,故答案为:
;CH2=CH2,故答案为: ;CH2=CH2;
;CH2=CH2;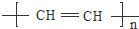 的单体是CH≡CH,故答案为:CH≡CH.
的单体是CH≡CH,故答案为:CH≡CH.


 春雨教育同步作文系列答案
春雨教育同步作文系列答案科目:高中化学 来源: 题型:
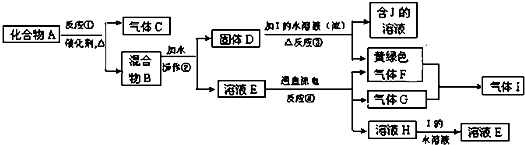
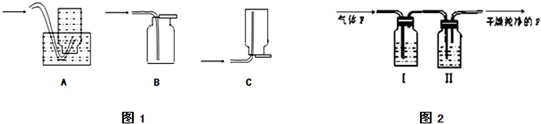
查看答案和解析>>
科目:高中化学 来源: 题型:
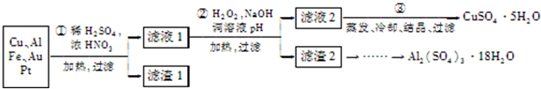
| 沉淀物 | Fe( OH)2 | Fe( OH)3 | Al( OH)3 | Cu( OH)2 |
| 开始沉淀 | 5.8 | 1.1 | 4.0 | 5.4 |
| 完全沉淀 | 8.8 | 3.2 | 5.2 | 6.7 |
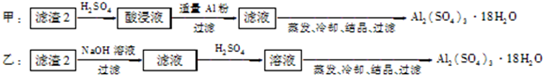
查看答案和解析>>
科目:高中化学 来源: 题型:
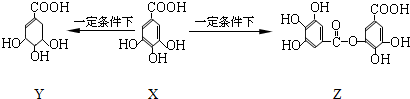
| A、1molX最多能与2molBr2发生取代反应 |
| B、Y分子结构中有2个手性碳原子 |
| C、Y能发生加成、取代、消去、氧化、缩聚反应 |
| D、1mol Z最多能与7molNaOH发生反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
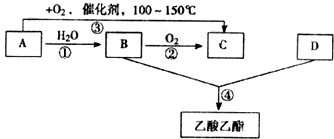 已知:A是石油裂解气的主要成份.A的产量通常用来衡量一个国家的石油化工水平,现以A为主要原料合成乙酸乙酯,其合成路线如图所示.
已知:A是石油裂解气的主要成份.A的产量通常用来衡量一个国家的石油化工水平,现以A为主要原料合成乙酸乙酯,其合成路线如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
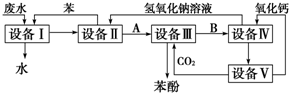
查看答案和解析>>
科目:高中化学 来源: 题型:
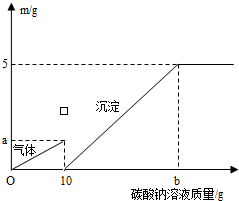 某同学对实验室用石灰石和稀盐酸制取二氧化碳后的溶液进行成分鉴定,取废液的上层清液,开始出现气泡,滴加至10g才开始出现白色沉淀,继续滴加至沉淀不再产生,过滤,测的沉淀的质量为5g,并绘制出下列图象.
某同学对实验室用石灰石和稀盐酸制取二氧化碳后的溶液进行成分鉴定,取废液的上层清液,开始出现气泡,滴加至10g才开始出现白色沉淀,继续滴加至沉淀不再产生,过滤,测的沉淀的质量为5g,并绘制出下列图象.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com