
| A. | 向滴有酚酞的水中加入过量Na2O2粉末并振荡,溶液由无色变红又变无色 | |
| B. | 钠的化学性质非常活泼,钠元素只能以化合态存在于自然界 | |
| C. | 将一小粒金属钠投入水和苯的混合体系中,钠在苯与水的界面处反应并可能作上、下跳动 | |
| D. | 某物质灼烧时,焰色反应为黄色,该物质一定只含钠元素 |
分析 A、过氧化钠与水反应生成氢氧化钠和氧气,氢氧化钠电离生成氢氧根离子,溶液显碱性,Na2O2具有强氧化性,具有漂白性;
B、钠的化学性质非常活泼,易失去最外层电子而被氧化生成化合物;
C、因苯的密度比水小,所以苯在上层,水在下层,又因钠的密度比水小,比苯大,因此介于两者之间;
D、钾元素的紫光必须透过蓝色钴玻璃才能观察到;
解答 解:A、过氧化钠与水反应的化学方程式为2Na2O2+2H2O═4NaOH+O2↑,溶液中有气泡产生,过氧化钠过量,且有强氧化性,能使溶液由无色变红又变无色,故A正确;
B、钠的化学性质非常活泼,易失去最外层电子而被氧化生成化合物,在自然界中只能以化合态存在,故B正确;
C、因苯的密度比水小,所以苯在上层,水在下层,又因钠的密度比水小,比苯大,因此介于两者之间,而钠能与水反应产生气体,在与水反应生成气体后被气体带离水层,进入苯层后停止反应又下沉,如此往复,直至钠反应完,故C正确;
D、钾元素的紫光必须透过蓝色钴玻璃才能观察到,故某物质灼烧时焰色反应为黄色,则一定只含钠元素,也可能含其他元素,如钾元素,故D错误;
故选D.
点评 本题考查钠的性质,难度不大,借助于题目情境,培养了学生分析问题的能力.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | 向某溶液中加入BaCl2溶液,有白色沉淀,则原溶液一定存在Ag+或SO42- | |
| B. | 向某溶液滴加NaOH溶液,将湿润红色石蕊试纸置于试管口,试纸不变蓝,可确定原溶液中无NH4+ | |
| C. | 向某溶液中加入足量的盐酸,放出二氧化碳气体,可证明该溶液中一定含有碳酸盐 | |
| D. | 用洁净铁丝蘸取溶液进行焰色反应,火焰呈黄色,则原溶液中有Na+ |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
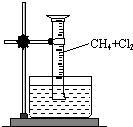 某研究小组为了探究甲烷和氯气反应的情况,设计了几个实验.
某研究小组为了探究甲烷和氯气反应的情况,设计了几个实验.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1 mol氧含有6.02×l023个微粒 | |
| B. | 阿伏加德罗常数数值约等于6.02×l0 23 | |
| C. | 硫的摩尔质量等于它的相对原子质量 | |
| D. | CO2的摩尔质量为44g |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将40 g NaOH固体溶于1 L水中 | |
| B. | 将22.4 L氯化氢气体溶于水配成1L溶液 | |
| C. | 将1L 10mol/L的浓盐酸与9L水混合 | |
| D. | 将10g NaOH固体溶解在水中配成250 mL溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | -252.9 kJ•mol-1 | B. | +252.9 kJ•mol-1 | C. | -604.5 kJ•mol-1 | D. | +604.5 kJ•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
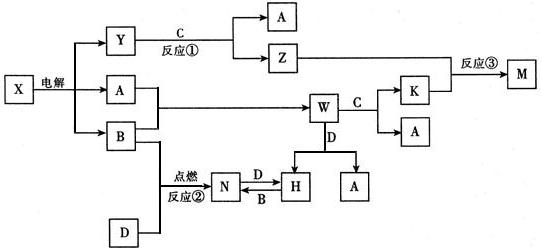
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com