
 R��X��Y��Z��λ��ǰ�����ڵ�Ԫ�أ���̬Rԭ�Ӻ������ռ��3���ܼ�����ÿ���ܼ��ϵ�������ȣ�Y��X������������������Ӹ�����Ϊ1��1��2��1�ͻ����ZX2�dz����Ĵ������������͵缫���ϣ�R��X��Y���һ�ֳ����������ˮ��Һ�����ڲ;ߵ�ϴ�Ӽ���R��X��Yԭ�ӵ�������֮�͵���Z����������
R��X��Y��Z��λ��ǰ�����ڵ�Ԫ�أ���̬Rԭ�Ӻ������ռ��3���ܼ�����ÿ���ܼ��ϵ�������ȣ�Y��X������������������Ӹ�����Ϊ1��1��2��1�ͻ����ZX2�dz����Ĵ������������͵缫���ϣ�R��X��Y���һ�ֳ����������ˮ��Һ�����ڲ;ߵ�ϴ�Ӽ���R��X��Yԭ�ӵ�������֮�͵���Z����������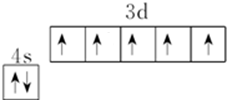 ����������Ԫ���У���һ��������С��Ԫ�صĻ�̬ԭ�Ӻ�����11�ֲ�ͬ�ĵ����˶�״̬��
����������Ԫ���У���һ��������С��Ԫ�صĻ�̬ԭ�Ӻ�����11�ֲ�ͬ�ĵ����˶�״̬������ R��X��Y��Z��λ��ǰ�����ڵ�Ԫ�أ���̬Rԭ�Ӻ������ռ��3���ܼ�����ÿ���ܼ��ϵ�������ȣ���R��CԪ�أ�
Y��X������������������Ӹ�����Ϊ1��1��2��1�ͻ����O��NaԪ�����γ�Na2O��Na2O2���������Y��NaԪ�ء�X��OԪ�أ�
C��O��Na���һ�ֳ���������̼���ƣ���ˮ��Һ�����ڲ;ߵ�ϴ�Ӽ���
C��O��Naԭ�ӵ�������֮�͵���Z������������Z������=6+8+11=25����Z��MnԪ�أ�MnO2�dz����Ĵ������������͵缫���ϣ�
��1��Z��MnԪ�أ���ԭ�Ӻ�����25�����ӣ�3d�ܼ���4s�ܼ�����Ϊ��۵��ӣ�3d�ܼ���5�����ӡ�4s�ܼ���2�����ӣ��ݴ���д��̬Zԭ�ӵļ۵����Ų�ͼ��
Ԫ�صĽ�����Խǿ���һ������ԽС��������Ԫ���е�һ��������С��Ԫ��ΪNaԪ�أ���Ԫ�ػ�̬ԭ�Ӻ����м������Ӿ��м����˶�״̬��
��2��C��O���⻯���У��Ⱥ��Ǽ��Լ����ֺ����Լ��������顢˫��ˮ�����γ�����Ļ�������˫��ˮ��ˮ��
��R���⻯���У�Rԭ���ӻ�����Ϊsp2��sp3����Ħ��������С�DZ�ϩ��
��3��CO32-���ӵ�����ԭ�Ӽ۲���Ӷ���=3+$\frac{1}{2}��$��4+2-3��2 ��=3��Ϊƽ�������Σ�
��4��Na���ʾ��徧����ͼ��ʾ���þ����������Զ��������ԭ��ֱ��������2d=$\sqrt{3}$acm���������=a3cm3���þ�����ԭ�Ӹ���=1+8��$\frac{1}{8}$=2������ԭ�������=[$\frac{4}{3}�У�\frac{\sqrt{3}}{4}a��^{3}$��2]cm3��ԭ��������=$\frac{ԭ�������}{�������}��100%$��
��� �⣺R��X��Y��Z��λ��ǰ�����ڵ�Ԫ�أ���̬Rԭ�Ӻ������ռ��3���ܼ�����ÿ���ܼ��ϵ�������ȣ���R��CԪ�أ�
Y��X������������������Ӹ�����Ϊ1��1��2��1�ͻ����O��NaԪ�����γ�Na2O��Na2O2���������Y��NaԪ�ء�X��OԪ�أ�
C��O��Na���һ�ֳ���������̼���ƣ���ˮ��Һ�����ڲ;ߵ�ϴ�Ӽ���
C��O��Naԭ�ӵ�������֮�͵���Z������������Z������=6+8+11=25����Z��MnԪ�أ�MnO2�dz����Ĵ������������͵缫���ϣ�
��1��Z��MnԪ�أ���ԭ�Ӻ�����25�����ӣ�3d�ܼ���4s�ܼ�����Ϊ��۵��ӣ�3d�ܼ���5�����ӡ�4s�ܼ���2�����ӣ���̬Mnԭ�ӵļ۵����Ų�ͼΪ ��
��
Ԫ�صĽ�����Խǿ���һ������ԽС��������Ԫ���е�һ��������С��Ԫ��ΪNaԪ�أ���Ԫ�ػ�̬ԭ�Ӻ����м������Ӿ��м����˶�״̬����ԭ����11�����ӣ�������ԭ�Ӻ��������11���˶�״̬��
�ʴ�Ϊ�� ��11��
��11��
��2��C��O���⻯���У��Ⱥ��Ǽ��Լ����ֺ����Լ�����CH3CH3��H2O2�����γ�����Ļ�������H2O2��H2O��
��R���⻯���У�Rԭ���ӻ�����Ϊsp2��sp3����Ħ��������С�DZ�ϩ����ṹ��ʽΪCH2=CHCH3��
�ʴ�Ϊ��CH3CH3��H2O2��H2O2��H2O��CH2=CHCH3��
��3��CO32-���ӵ�����ԭ�Ӽ۲���Ӷ���=3+$\frac{1}{2}��$��4+2-3��2 ��=3��Ϊƽ�������Σ�
�ʴ�Ϊ��3��ƽ�������Σ�
��4��Na���ʾ��徧����ͼ��ʾ���þ����������Զ��������ԭ��ֱ��������2d=$\sqrt{3}$acm����d=$\frac{\sqrt{3}}{2}a$cm���������=a3cm3���þ�����ԭ�Ӹ���=1+8��$\frac{1}{8}$=2������ԭ�������=[$\frac{4}{3}�У�\frac{\sqrt{3}}{4}a��^{3}$��2]cm3��ԭ��������=$\frac{ԭ�������}{�������}��100%$=$\frac{\frac{4}{3}�У�\frac{\sqrt{3}}{4}a��^{3}��2c{m}^{3}}{{a}^{3}c{m}^{3}}��100%$=68%��
�ʴ�Ϊ��$\frac{\sqrt{3}}{2}a$cm��68%��
���� ���⿼�����ʽṹ�����ʣ��漰�������㡢���ռ乹���жϡ�ԭ���ӻ�����������Ų���֪ʶ�㣬��Щ���Ǹ�Ƶ���㣬�ѵ��Ǿ������㣬��ȷ�������ļ���ԭ��ֱ�������ǽ⣨4����ؼ�����Ŀ�Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ϡ�����������м��Ӧ��Fe+4H++NO3-=Fe3++NO��+2H2O | |
| B�� | ���������Һ�м�����������������Һ��NH4++OH-=NH3��+H2O | |
| C�� | �Ȼ�����Һ�м��������ˮ��Al3++4NH3•H2O=AlO2-+4 NH4++2H2O | |
| D�� | Na2SO3��Һʹ����KMnO4��Һ��ɫ��5SO32-+6H++2MnO4-=5SO42-+2Mn2++3H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
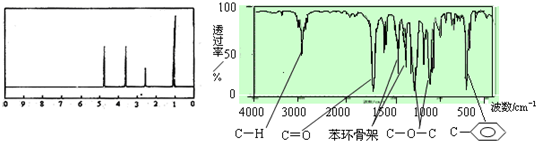
| A�� | ��������A���ӽṹ�������л����ж��� | |
| B�� | A��һ�������¿���4 mol H2�����ӳɷ�Ӧ | |
| C�� | A����������������һ���������ܷ���ˮ�ⷴӦ | |
| D�� | ��A����ͬ������ͬ���칹��ֻ��2�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | m g����ϩ�ͱ�ϩ��ɵĻ������ȫȼ����������Ϊ$\frac{24m}{7}$g | |
| B�� | 14g��ϩ�ͱ�ϩ����ﺬ��3NA��ԭ�� | |
| C�� | ����ϩ���巢���ӳɷ�Ӧ����1��2һ���������֪��ϩ���ӵ�̼̼˫������һ�������ȶ����������� | |
| D�� | �����к���ϩ���ʿ���������KMnO4��Һ��ȥ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���տ�����CO2 ���� | |
| B�� | NaOH�벣�����ã���������CO2 ���� | |
| C�� | NaOH���Na2CO3 | |
| D�� | ��Һ�е�ˮ�ֲ������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���� | B�� | ���� | C�� | ������ | D�� | ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A������0.10mol•L-1NaOH��Һ | B����ȥCO�е�CO2 | C������ȡ��ˮ��I2���ֳ�ˮ���IJ��� | D����¼�ζ��յ����Ϊ12.20mL |
 | 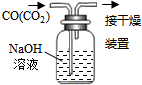 |  | 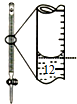 |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | V��B��=0.6 mol/��L•min�� | B�� | V��A��=0.3 mol/��L•min�� | ||
| C�� | V��B��=0.02/��L•S�� | D�� | V��C��=0.5 mol/��L•min�� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com