
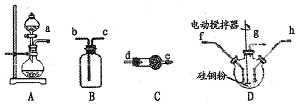
分析 由图可知:SiH2Cl2在D中生成,则A装置为制HCl气体的装置,SiH2Cl2沸点低,挥发,在B中收集,因为SiH2Cl2遇水水解,故装置中应无水,则装置顺序为,A装置制取HCl,连接C装置干燥,为a-d-e,从f进入D中反应,SiH2Cl2从g处挥发,在B装置中收集,SiH2Cl2密度比空气重,导气管应长进短出,为防止空气中的水进入B中,则应在B后接干燥管,故顺序为:adefgbcde,据此分析.
解答 解:(1)利用浓硫酸、浓盐酸为原料,浓硫酸有吸水性,使浓盐酸更易挥发出HCl,故答案为:吸水;
(2)D装置中生成二氯二氢硅的化学方程式为Si+2HCl$\frac{\underline{\;250~260℃\;}}{\;}$SiH2Cl2,故答案为:Si+2HCl$\frac{\underline{\;250~260℃\;}}{\;}$SiH2Cl2;
(3)A装置制取HCl,连接C装置干燥,为a-d-e,从f进入D中反应,SiH2Cl2从g处挥发,在B装置中收集,SiH2Cl2密度比空气重,导气管应长进短出,为防止空气中的水进入B中,则应在B后接干燥管,故顺序为:adefgbcde;
故答案为:d;e;f;g;b;c;d;
(4)C装置干燥氯化氢气体,故应选酸性P2O5或中性CaCl2干燥剂,后面装置C的作用为尾气处理和防止空气中的水进入B中;
故答案为:P2O5或CaCl2;尾气处理和防止空气中的水进入B中;
(5)反应除生成二氯二氢硅之外,还会发生反应3Si+10HCl$\frac{\underline{\;高温\;}}{\;}$2SiHCl3+SiCl4+4H2,生成H2和SiCl4、SiHCl3等;
故答案为:SiCl4;SiHCl3;
(6)往硅粉中先通入Cl2在300-350℃反应生成SiCl4,然后再与HCl在250-260℃反应,可以大大提高产率.如果通人气体次序相反,结果会SiH2Cl2与Cl2反应,SiH2Cl2+2Cl2$\frac{\underline{\;\;△\;\;}}{\;}$SiCl4+2HCl (或SiH2Cl2+Cl2$\frac{\underline{\;\;△\;\;}}{\;}$SiHCl3+HCl),
故答案为:SiH2Cl2+2Cl2$\frac{\underline{\;\;△\;\;}}{\;}$SiCl4+2HCl (或SiH2Cl2+Cl2$\frac{\underline{\;\;△\;\;}}{\;}$SiHCl3+HCl).
点评 本题考查了化学实验方案设计,物质制备实验装置的分析判断,注意操作过程中仪器的作用分析,题目难度中等,注意掌握实验原理.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:多选题
| A. | 冰融化成水放出热量 | |
| B. | 化学键断裂过程一定放出能量 | |
| C. | 生成物的总能量一定低于反应物的总能量 | |
| D. | 化学键的断裂和形成是化学反应中能量变化的主要原因 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
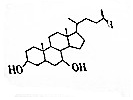 鹅去氧胆酸是目前世界上用量最大的治胆结石药物之一,其结构简式如图所示,下列关于鹅去氧胆酸的说法正确的是( )
鹅去氧胆酸是目前世界上用量最大的治胆结石药物之一,其结构简式如图所示,下列关于鹅去氧胆酸的说法正确的是( )| A. | 分子中含有4个苯环 | |
| B. | 1mol鹅去氧胆酸和足量NaHCO3溶液反应产生3molCO2 | |
| C. | 不能使酸性KMnO4溶液褪色 | |
| D. | 能发生取代、氧化等反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
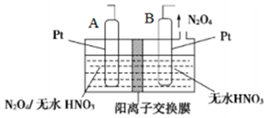 氮的氧化物种类较多,有N2O、NO、N2O3、NO2、N2O4、N2O5等,他们应用广泛.
氮的氧化物种类较多,有N2O、NO、N2O3、NO2、N2O4、N2O5等,他们应用广泛.查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验操作和现象 | 结论 |
| A | 向某溶液中滴加CCl4,振荡、静置,下层溶液显紫色 | 原溶液中含有I- |
| B | 常温下,0.1mol/LNaHSO3溶液的pH约为5 | HSO3-的电离程度大于其水解程度 |
| C | 相同温度下,测得饱和亚硫酸溶液的pH小于饱和碳酸溶液的pH | 亚硫酸的酸性强于碳酸 |
| D | 向稀HNO3中加入过量的Fe粉,充分反应后,滴入KSCN溶液不显红色 | 稀HNO3将Fe氧化为Fe2+ |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 醋酸铵与稀盐酸反应:CH3COONH4+H+→CH3COOH+NH4+ | |
| B. | 氯化铁溶液中通入硫化氢气体:2Fe3++S2-→2Fe2++S↓ | |
| C. | 硫酸铜溶液中加入过量的氢氧化钡:Ba2++SO42-→BaSO4↓ | |
| D. | 溴化亚铁溶液中通入足量的氯气:3Cl2+2Fe2++4Br-→6Cl-+2Fe3++2Br2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com