
| ŹµŃé·½°ø | ŹµŃéĻÖĻó |
| ¢Ł½«ŠĀÖĘĀČĖ®µĪ¼Óµ½NaBrČÜŅŗÖŠ£¬Õńµ“ŗó¼ÓČėŹŹĮæCCl4ČÜŅŗ£¬Õńµ“£¬¾²ÖĆ | A£®ø”ŌŚĖ®ĆęÉĻ£¬ČŪ³ÉŠ”Ēņ£¬ĖÄ“¦ÓĪ¶Æ£¬ĖęŗóĻūŹ§ |
| ¢Ś½«Ņ»Š”æ齚ŹōÄĘ·ÅČėĄäĖ®ÖŠ | B£®·Ö²ć£¬ÉĻ²ćĪŽÉ«£¬ĻĀ²ć×ĻÉ« |
| ¢Ū½«äåĖ®µĪ¼Óµ½NaIČÜŅŗÖŠ£¬Õńµ“ŗó¼ÓČėŹŹĮæCCl4ČÜŅŗ£¬Õńµ“£¬¾²ÖĆ | C£®ø”ŌŚĖ®ĆęÉĻ£¬ČŪ³ÉŠ”Ēņ£¬ĖÄ“¦ÓĪ¶Æ£¬²¢°éÓŠĒįĪ¢µÄ±¬ÕØÉł£¬ŗÜæģĻūŹ§ |
| ¢Ü½«Ņ»Š”æ齚Źō¼Ų·ÅČėĄäĖ®ÖŠ | D£®·Ö²ć£¬ÉĻ²ćĪŽÉ«£¬ĻĀ²ćŗģ×ŲÉ« |
| ŹµŃé·½°ø | ŹµŃéĻÖĻó | »Æѧ·½³ĢŹ½ |
| ¢Ł | D | Cl2+2NaBrØT2NaCl+Br2 |
| ¢Ś | A | 2Na+2H2OØT2NaOH+H2”ü |
| ¢Ū | B | Br2+2NaIØT2NaBr+I2 |
| ¢Ü | C | 2K+2H2OØT2KOH+H2”ü |
·ÖĪö øĆĶ¬Ń§µÄŹµŃéÉę¼°ĮĖĀ±ĖŲµÄÖĆ»»·“Ó¦ŗĶ¼ī½šŹōÄĘ”¢¼ŲÓėĖ®µÄ·“Ó¦£¬ŹµŃéÄæµÄŹĒĢ½¾æĶ¬Ö÷×åŌŖĖŲŠŌÖŹµÄĻąĖĘŠŌŗĶµŻ±äŠŌ£»½įŗĻŹµŃé·½°øŗĶŹµŃéĻÖĻóæÉĶĘ²ā³öĖłÓƵ½µÄŅĒĘ÷£®½įŗĻŌŖĖŲ¼°»ÆŗĻĪļµÄŠŌÖŹæÉŠ“³ö·“Ó¦·½³ĢŹ½£¬
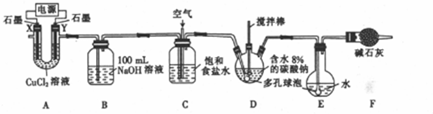
£Ø1£©ŅĄ¾ŻĢāøÉŠÅĻ¢½įŗĻŹµŃé¹ż³ĢŗĶĻÖĻóæÉÖŖŹĒŃŠ¾æĶ¬Ö÷×åŌŖĖŲŠŌÖŹµÄµŻ±ä¹ęĀÉ£»
£Ø2£©øł¾ŻŅĒĘ÷µÄ×÷ÓĆєȔŅĒĘ÷£¬ĪļÖŹŠŌÖŹŹµŃéŠčŅŖŹŌ¹Ü”¢ÉÕ±”¢½ŗĶ·µĪ¹ÜµČŅĒĘ÷£»
£Ø3£©ŅĄ¾ŻŹµŃé²½ÖčŗĶŹµŃéĻÖĻ󣬽įŗĻĪļÖŹŠŌÖŹŗĶ·“Ó¦ĻÖĻó½ųŠŠ¶ŌÓ¦£¬Š“³ö·“Ó¦µÄ»Æѧ·½³ĢŹ½£¬¢Ū½«äåĖ®µĪ¼Óµ½NaIČÜŅŗÖŠ·“Ӧɜ³Éµāµ„ÖŹ£»
£Ø4£©·ÖĪö½šŹōŗĶ·Ē½šŹō·“Ó¦µÄ²śĪļŗĶ¾ēĮŅ³Ģ¶Č£¬½įŗĻ½šŹōŠŌŗĶ·Ē½šŹōŠŌĒæČõµÄÅŠ¶ĻŅĄ¾Ż·ÖĪöÅŠ¶Ļ£¬Ķ¬Ö÷×å“ÓÉĻµ½ĻĀŹ§µē×ÓÄÜĮ¦ŅĄ“ĪŌöĒ棬µĆµē×ÓÄÜĮ¦ŅĄ“Ī¼õČõ£®
½ā“š ½ā£ŗ£Ø1£©ŅĄ¾ŻÄ³Ķ¬Ń§×öĶ¬Ö÷×åŌŖĖŲŠŌÖŹĻąĖĘŠŌ”¢µŻ±äŠŌŹµŃ鏱£¬×Ō¼ŗÉč¼ĘĮĖŅ»Ģ׏µŃé·½°ø£¬½įŗĻŹµŃé¹ż³ĢŗĶŹµŃéĻÖĻóæÉÖŖŹµŃéÄæµÄŹĒĢ½¾æĶ¬Ö÷×åŌŖĖŲŠŌÖŹµÄĻąĖĘŠŌŗĶµŻ±äŠŌ£¬
¹Ź“š°øĪŖ£ŗĢ½¾æĶ¬Ö÷×åŌŖĖŲŠŌÖŹµÄĻąĖĘŠŌŗĶµŻ±äŠŌ£»
£Ø2£©øĆŹµŃéÉę¼°µĪ¼ÓČÜŅŗ×öŹµŃ飬ŌņŠč½ŗĶ·µĪ¹Ü£¬ŹµŃé¹ż³ĢÖŠĄė²»æŖŹŌ¹Ü”¢ÉÕ±£¬
¹Ź“š°øĪŖ£ŗŹŌ¹Ü£»ÉÕ±£»½ŗĶ·µĪ¹Ü£»
£Ø3£©¢Ł½«ĀČĖ®µĪ¼Óµ½NaBrČÜŅŗÖŠ£¬Õńµ“ŗóŌŁ¼ÓČėŹŹĮæCCl4£¬Õńµ“£¬¾²ÖĆ£¬D”¢·Ö²ć£¬ÉĻ²ćĪŽÉ«£¬ĻĀ²ć³ČŗģÉ«£¬·“Ó¦ĪŖCl2+2NaBrØT2NaCl+Br2 £»
¢Ś½«Ņ»Š”æ齚ŹōÄĘ·ÅČėµ½ĄäĖ®ÖŠ£¬A”¢ø”ŌŚĖ®ĆęÉĻ£¬ČŪ³ÉŠ”Ēņ£¬²»¶ØĻņŅĘ¶Æ£¬ĖęÖ®ĻūŹ§£¬·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ 2Na+2H2OØT2NaOH+H2”ü£»
¢Ū½«äåĖ®µĪ¼Óµ½NaIČÜŅŗÖŠ£¬Õńµ“ŗóŌŁ¼ÓČėŹŹĮæ CCl4£¬Õńµ“£¬¾²ÖĆ£¬B”¢·Ö²ć£¬ÉĻ²ćĪŽÉ«£¬ĻĀ²ć×ĻŗģÉ«£¬·“Ó¦ĪŖ Br2+2NaIØT2NaBr+I2 £»
¢Ü½«Ņ»Š”æ齚Źō¼Ų·ÅČėĄäĖ®ÖŠ£¬C”¢ø”ŌŚĖ®ĆęÉĻ£¬ČŪ³ÉŠ”Ēņ£¬²»¶ØĻņŅĘ¶Æ£¬²¢°éÓŠĒįĪ¢µÄ±¬ÕØÉł£¬ŗÜæģĻūŹ§£¬·“Ó¦ĪŖ2K+2H2OØT2KOH+H2”ü£¬
¹Ź“š°øĪŖ£ŗ
| ŹµŃéÄŚČŻ | ŹµŃéĻÖĻó | »Æѧ·½³ĢŹ½ |
| ¢Ł | ||
| ¢Ś | ||
| ¢Ū | B | Br2+2NaIØT2NaBr+I2 |
| ¢Ü | C | 2K+2H2OØT2KOH+H2”ü |
µćĘĄ ±¾ĢāŹĒŅ»øöŹµŃéÉč¼ĘĢā£¬ĢāÄæ½ĻĮé»ī£¬æ¼²é»ł“”ÖŖŹ¶ŗĶŌĖÓĆÖŖŹ¶µÄÄÜĮ¦£®¶ŌŹµŃéÄæµÄĆčŹö£¬ŅŖ×¢ŅāĢāÖŠÓŠŠ§ŠÅĻ¢µÄĢįČ”£¬²¢×¢ŅāÓļŃŌµÄ×¼Č·ŠŌ£¬ĢāÄæÄѶČÖŠµČ£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2016-2017ѧğŗŚĮś½“óĒģŅ»ÖŠøßŅ»ÉĻ10ŌĀŌĀæ¼»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
Fe3+”¢SO42-”¢Al3+ŗĶXĖÄÖÖĄė×ÓŅŌĪļÖŹµÄĮæÖ®±Č2:4:1:1“óĮæ¹²“ęÓŚĶ¬Ņ»ČÜŅŗÖŠ£¬XæÉÄÜŹĒ( )
A£®Na+ B£®OH- C£®CO32- D£®Cl-
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
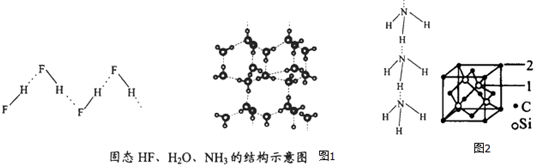
| ĪļÖŹ | Ēā¼üX-H”Y | ¼üÄÜkJ£®mol-1 |
| £ØHF£©n | D-H”F | 28.1 |
| ±ł | O-H”O | 18.8 |
| £ØNH3£©n | N-H”N | 5.4 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ŌŚ±ź×¼×“æöĻĀ£¬NAøöĖ®·Ö×ÓĖłÕ¼µÄĢå»żŌ¼ĪŖ22.4L | |
| B£® | 5.6gĢśÓėĀČĘųĶźČ«·“Ó¦£¬Ź§Č„µē×ӵďżÄæĪŖ0.2NA | |
| C£® | 1 mol Na2O2Óė×ćĮæCO2³ä·Ö·“Ó¦£¬×ŖŅʵĵē×ÓŹżĪŖ2NA | |
| D£® | ŌŚ±ź×¼×“æöĻĀ£¬22.4LÓÉN2”¢N2O×é³ÉµÄ»ģŗĻĘųĢåÖŠĖłŗ¬µÄµŖŌ×ÓŹżĪŖ2NA |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
 £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Al£ØOH£©3+NaOHØTNaAlO2+2H2O | B£® | 2Na+2H2OØT2NaOH+H2”ü | ||
| C£® | Na2O+CO2ØTNa2CO3 | D£® | 2NaHCO3ØTNa2CO3+CO2”ü+H2O |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 2øö | B£® | 3øö | C£® | 4øö | D£® | 5øö |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | SO2”śSO3£ŗ2SO2+O2ØT2SO3 | |
| B£® | Fe”śFe2+£ŗFe+2H+ØTFe2++H2”ü | |
| C£® | Cl-”śCl2£ŗ2Cl-+I2ØTCl2+2I- | |
| D£® | Cu”śCu£ØNO3£©2£ŗ3Cu+8HNO3£ØÅØ£©ØTCu£ØNO3£©2+NO”ü+4H2O |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com