
【题目】常温下,向20.00 mL 0.100 mol·L-1 CH3COONa溶液中逐滴加入0.100 0 mol·L-1盐酸,溶液的pH与所加盐酸体积的关系如下图所示(不考虑挥发)。下列说法正确的是

A. 点①所示溶液中:c(CH3COOH)=c(Cl-)>c(OH-)=c(H+)
B. 点②所示溶液中:c(Na+)>c(Cl-)>c(CH3COO-)>c(CH3COOH)
C. 点③所示溶液中:c(CH3COOH)>c(Na+)>c(H+)>c(CH3COO-)
D. 整个过程中可能出现:c(H+)+c(Na+)=c(CH3COOH)+c(CH3COO-)
【答案】A
【解析】
写出溶液中的电荷守恒c(Na+)+c(H+)=c(CH3COO-)+c(Cl-)+c(OH-)和物料守恒c(Na+)=c(CH3COOH)+c(CH3COO-),可判断出D错误;①中溶液呈中性c(H+)=c(OH-),故综合两守恒可得c(CH3COOH)=c(Cl-),A正确;②点溶液中有等浓度的CH3COOH、CH3COONa和NaCl,溶液呈酸性,可仅考虑醋酸电离,则c(CH3COO-)>c(Cl-),B错误;③点溶液中有等浓度的CH3COOH和NaCl,由于醋酸有少部分电离,故c(Na+)>c(CH3COOH),醋酸每电离生成一份CH3COO-的同时就会生成一份H+,同时水也电离生成少量H+,故c(H+)>c(CH3COO-),所以C错误。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】某实验小组同学把小块木炭在酒精灯上烧至红热,迅速投入热的浓硝酸中,发生剧烈反应,同时有大量红棕色气体产生,液面上木炭迅速燃烧发出亮光。经查阅资料可知浓硝酸分解产生NO2和O2。为了探究“液面上木炭迅速燃烧发出亮光”的原因,该小组同学用如图装置完成以下实验:

序号 | 实验I | 实验II |
集气瓶中所盛气体 | O2 | 加热浓硝酸 产生的气体 |
现象 | 木炭迅速燃烧发出亮光 | 木炭迅速燃烧发出亮光 |
下列说法正确的是
A. 浓硝酸分解产生的V(NO2):V(O2)=1:1
B. 红棕色气体的产生表明木炭与浓硝酸发生了反应
C. 能使液面上木炭迅速燃烧发出亮光的主要气体是氧气
D. 以上实验不能确定使液面上木炭迅速燃烧发出亮光的主要气体一定是NO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求填空
(1)乙醇同分异构体的结构简式__________,磁铁矿主要成分的化学式__________;
(2)氯气和水反应的离子方程式____________________________________________;
(3)铝和氢氧化钠溶液反应的化学方程式____________________________________;
(4)碳酸氢钠的电离方程式________________________________________________;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应的离子方程式正确的是 ( )
A. 用石墨作电极电解 AlC13 溶液:2Cl- +2H2O![]() Cl2↑+H2↑+2OH
Cl2↑+H2↑+2OH
B. 酸性高锰酸钾溶液与 H2O2 溶液混合:2MnO4 + 3H2O2 + 6H+= 2Mn2++ 4O2↑+6H2O
C. 向硫代硫酸钠溶液中滴加稀硫酸:3S2O32-+2H+=2SO42-+4S↓+H2O
D. 向 Mg(HCO3)2 溶液中加入足量 Ca(OH)2 的溶液:Mg2++2HCO3- +4OH- +2Ca2+=3H2O+2CaCO3↓+ Mg(OH)2↓
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 反应 2Mg+CO2 ![]() 2MgO+C△H<0 从熵变角度看,可自发进行
2MgO+C△H<0 从熵变角度看,可自发进行
B. 在密闭容器发生可逆反应:2NO(g)+2CO(g)N2(g)+2CO2(g)△H=-113.0kJ/mol,达到平衡后,保持温度不变,缩小容器体积,重新达到平衡后,△H 变小
C. 根据 HClO 的 Ka=3.0×108,H2CO3 的 Ka1=4.3×107,Ka2=5.6×1011,可推测相同状况 下,等浓度的 NaClO 与 Na2CO3 溶液中,pH 前者小于后者
D. 已知:Ksp(AgCl)=1.8×1010,Ksp(Ag2CrO4)=2.0×1012,将等体积浓度为1.0×10﹣4mol/L 的 AgNO3 溶液滴入到浓度均为 1.0×10﹣4mol/L 的 KCl 和 K2CrO4 的混合溶液中产生两种不同沉淀,且 Ag2CrO4 沉淀先产生
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】装置(Ⅰ)为铁镍(Fe﹣Ni)可充电电池:Fe+NiO2![]() Fe(OH)2+Ni(OH)2;装置(Ⅱ)为电解示意图,当闭合开关 K 时,Y 附近溶液先变红.下 列说法正确的是( )
Fe(OH)2+Ni(OH)2;装置(Ⅱ)为电解示意图,当闭合开关 K 时,Y 附近溶液先变红.下 列说法正确的是( )

A. 闭合 K 时,X 的电极反应式为:2H++2e═H2↑
B. 给装置(Ⅰ)充电时,OH通过阴离子交换膜,移向 A 电 极
C. 给装置(Ⅰ)充电时,B 极参与反应的物质被氧化
D. 闭合 K 时,A 电极反应式为:NiO2 + 2e +2H+═Ni(OH)2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NH3 作为一种重要化工原料,被大量应用于工业生产,与其有关性质反应的 催化剂研究曾被列入国家 863 计划。
(1)催化剂常具有较强的选择性,即专一性。已知:反应 I :4NH3(g) +5O2(g)![]() 4NO(g) +6H2O(g)△H= 905.0 kJ·mol-1 反应 II : 4NH3(g)+3O2(g)
4NO(g) +6H2O(g)△H= 905.0 kJ·mol-1 反应 II : 4NH3(g)+3O2(g)![]() 2N2(g) +6H2O(g) △H= 1266.6 kJ·mol-1 写出 NO 分解生成 N2 与 O2 的热化学方程式_________。
2N2(g) +6H2O(g) △H= 1266.6 kJ·mol-1 写出 NO 分解生成 N2 与 O2 的热化学方程式_________。
(2)在恒温恒容装置中充入一定量的 NH3 和 O2,在某催化剂的作用下进行反应 I ,测得不同时 间的 NH3 和 O2,的浓度如下表:
时间(min) | 0 | 5 | 10 | 15 | 20 | 25 |
c(NH3)/mol·L1 | 1.00 | 0.36 | 0.12 | 0.08 | 0.072 | 0.072 |
c(O2)/mol L1 | 2.00 | 1.20 | 0.90 | 0.85 | 0.84 | 0.84 |
则下列有关叙述中正确的是_____。
A.使用催化剂时,可降低该反应的活化能,加快其反应速率
B.若测得容器内 4v 正(NH3) =6v 逆(H2O)时,说明反应已达平衡
C.当容器内n(NO)/n(NH3)=1 时,说明反应已达平衡
D.前 10 分钟内的平均速率 v( NO)=0.088 mol·L-1·min-1
(3)制备催化剂时常产生一定的废液,工业上常利用氢硫酸检测和除去废液中的 Cu2+。 已知:25℃时,K1(H2S) =1.3×107,K2(H2S) =7.1×1015,Ksp(CuS) =8.5×1045
①在计算溶液中的离子浓度时,涉及弱酸的电离通常要进行近似处理。则 0.lmol L1 氢硫 酸的 pH≈______(取近似整数)。
②某同学通过近似计算发现 0.lmol L1 氢硫酸与 0.0lmol L1 氢硫酸中的 c(S2)相等,而且 等于_____mol·L1
③已知,某废液接近于中性,若加入适量的氢硫酸,当废液中 c(Cu2+) >_____mol·L1(计算 结果保留两位有效数字),就会产生 CuS 沉淀。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锂空气充电电池有望成为电动汽车的实用储能设备。工作原理示意图如下,下列叙述正确的是
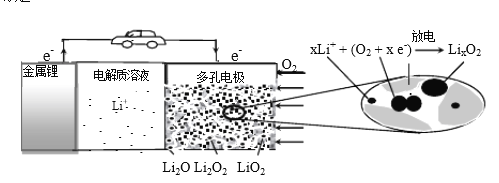
A. 该电池工作时Li+向负极移动
B. Li2SO4溶液可作该电池电解质溶液
C. 电池充电时间越长,电池中Li2O 含量越多
D. 电池工作时,正极可发生: 2Li+ +O2+ 2e-=Li2O2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】富硼渣中含有镁硼酸盐(2MgO·B2O3)、镁硅酸盐(2MgO·SiO2)及少量Al2O3、FeO等杂质。由富硼渣湿法制备硫酸镁晶体和硼酸(H3BO3)晶体的一种工艺流程如下:

已知:生成氢氧化物沉淀的pH(金属离子的起始浓度为0.1mol/L)
Fe(OH)3 | Al(OH)3 | Fe(OH)2 | Mg(OH)2 | |
开始沉淀时 | 1.9 | 3.4 | 7.0 | 9.1 |
完全沉淀时 | 3.2 | 4.7 | 9.0 | 11.1 |
(1)上述流程中能加快反应速率的措施有______、_______等。
(2)酸浸时发生反应:2MgO·SiO2 + 2H2SO4=2MgSO4 + SiO2 + 2H2O,2MgO·B2O3+ 2H2SO4 + H2O=2H3BO3 + 2MgSO4。
①上述反应体现出酸性强弱:H2SO4______H3BO3(填“>”或“<”)。
② 酸浸时,富硼渣中所含Al2O3和FeO也同时溶解,写出相关反应的离子方程式:______、______。
③ 已知硼酸与过量NaOH溶液发生的中和反应为:H3BO3 + OH- B(OH)4-。下列关于硼酸的说法正确的是__(填序号)。
a. 硼酸是一元酸
b. 向NaHCO3固体中滴加饱和硼酸溶液,有气泡产生
c. 硼酸的电离方程式可表示为:H3BO3 + H2O![]() B(OH)4-+H+
B(OH)4-+H+
(3)检验褐色浸出液中的杂质离子:取少量浸出液,______(填操作和现象),证明溶液中含有Fe2+。
(4)除去浸出液中的杂质离子: 用MgO调节溶液的pH至______以上,使杂质离子转化为______(填化学式)沉淀,过滤。
(5)获取晶体:ⅰ.浓缩滤液,使MgSO4和H3BO3接近饱和;ⅱ.控制温度使两种晶体分别从溶液中结晶。结合下图溶解度曲线,简述ⅱ的方法:将浓缩液加入到高压釜中,______(将方法补充完整)。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com