
(5Зж)баОПБэУїЃЌдквЛЖЈЮТЖШКЭбЙЧПЬѕМўЯТЃЌ2 mol H2(g) КЭ1 mol O2(g) ЭъШЋЛЏКЯЩњГЩ2 mol H2O(g) ЫљЗХГіЕФШШСПЃЛЂйгыдкЯрЭЌЬѕМўЯТ2 mol H2O(g) ЭъШЋЗжНтЮЊ2 mol H2(g) КЭ1 mol O2(g) ЫљЮќЪеЕФШШСПдкЪ§жЕЩЯЯрЕШЃЛ ЂкЪЧЯрЭЌЬѕМўЯТ1 mol H2(g) КЭ0.5 mol O2(g) ЭъШЋЛЏКЯЩњГЩ1 mol H2O(g)ЫљЗХГіШШСПЕФ2БЖЃЛЂлБШдкЯрЭЌЬѕМўЯТ2 mol H2(g) КЭ1 mol O2(g) ЭъШЋЛЏКЯЩњГЩ2 mol H2O(l) ЫљЗХГіЕФШШСПЩйЁЃ
гЩДЫЃЌФуПЩЕУГіФФаЉНсТлЃП
 ЬьЬьЯђЩЯвЛБОКУОэЯЕСаД№АИ
ЬьЬьЯђЩЯвЛБОКУОэЯЕСаД№АИ аЁбЇЩњ10ЗжжггІгУЬтЯЕСаД№АИ
аЁбЇЩњ10ЗжжггІгУЬтЯЕСаД№АИ
| ФъМЖ | ИпжаПЮГЬ | ФъМЖ | ГѕжаПЮГЬ |
| ИпвЛ | ИпвЛУтЗбПЮГЬЭЦМіЃЁ | ГѕвЛ | ГѕвЛУтЗбПЮГЬЭЦМіЃЁ |
| ИпЖў | ИпЖўУтЗбПЮГЬЭЦМіЃЁ | ГѕЖў | ГѕЖўУтЗбПЮГЬЭЦМіЃЁ |
| ИпШ§ | ИпШ§УтЗбПЮГЬЭЦМіЃЁ | ГѕШ§ | ГѕШ§УтЗбПЮГЬЭЦМіЃЁ |
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
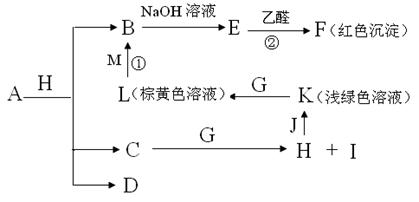
ИїЮяжЪжЎМфЕФзЊЛЛЙиЯЕШчЯТЭМЃЌВПЗжЩњГЩЮяЪЁТдЁЃCЁЂDЪЧгЩXЁЂYЁЂZжаСНжждЊЫизщГЩЕФЛЏКЯЮяЃЌXЁЂYЁЂZЕФдзгађЪ§вРДЮдіДѓЃЌдкжмЦкБэжаXЕФдзгАыОЖзюаЁЃЌYЁЂZдзгзюЭтВуЕчзгЪ§жЎКЭЮЊ10ЁЃDЮЊЮоЩЋЗЧПЩШМадЦјЬхЃЌGЮЊЛЦТЬЩЋЕЅжЪЦјЬхЃЌJЁЂMЮЊН№ЪєЃЌlгаЦЏАззїгУЃЌЗДгІЂйГЃгУгкжЦзїгЁЫЂЕчТЗАхЁЃ
ЧыЛиД№ЯТСаЮЪЬтЃК
ЃЈ1ЃЉаДГіAЕФЛЏбЇЪН ЃЌ CЕФЕчзгЪН ЁЃ
ЃЈ2ЃЉгЩXЁЂYЁЂZШ§жждЊЫиАДдзгИіЪ§БШЮЊ4:1:1аЮГЩЕФЛЏКЯЮяЕФНсЙЙМђЪНЮЊ ЁЃ
ЃЈ3ЃЉаДГіЗДгІЂкЕФЛЏбЇЗНГЬЪНЃЈгаЛњЮягУНсЙЙМђЪНБэЪОЃЉ ЃЌ
гЩXЁЂYСНдЊЫиаЮГЩЕФЗжзгСПЮЊ72ЕФЛЏКЯЮяЕФЭЌЗжвьЙЙЬхЙВга жжЃЌЦфжадкЙтееЯТгыCl2ЗДгІЦфвЛТШШЁДњЮяга4жжЕФЛЏКЯЮяЕФУћГЦЮЊ ЁЃ
ЃЈ4ЃЉвбжЊFШмгкЯЁЯѕЫсЃЌШмвКБфГЩРЖЩЋЃЌВЂЗХГіЮоЩЋЦјЬхЁЃЧыаДГіИУЗДгІЕФЛЏбЇЗНГЬЪН ЁЃ
ЃЈ5ЃЉбаОПБэУїЃКЦјЬхDдквЛЖЈЬѕМўЯТПЩБЛЛЙдЮЊОЇгЈЭИУїЕФОЇЬхNЃЌЦфНсЙЙжадзгЕФХХСаЮЊе§ЫФУцЬхЃЌЧыаДГіNМАЦф2жжЭЌЫивьаЮЬхЕФУћГЦ ЁЂ ЁЂ ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ИїЮяжЪжЎМфЕФзЊЛЛЙиЯЕШчЯТЭМЃЌВПЗжЩњГЩЮяЪЁТдЁЃCЁЂDЪЧгЩXЁЂYЁЂZжаСНжждЊЫизщГЩЕФЛЏКЯЮяЃЌXЁЂYЁЂZЕФдзгађЪ§вРДЮдіДѓЃЌдкжмЦкБэжаXЕФдзгАыОЖзюаЁЃЌYЁЂZдзгзюЭтВуЕчзгЪ§жЎКЭЮЊ10ЁЃDЮЊЮоЩЋЗЧПЩШМадЦјЬхЃЌGЮЊЛЦТЬЩЋЕЅжЪЦјЬхЃЌJЁЂMЮЊН№ЪєЃЌlгаЦЏАззїгУЃЌЗДгІЂйГЃгУгкжЦзїгЁЫЂЕчТЗАхЁЃ
ЧыЛиД№ЯТСаЮЪЬтЃК
ЃЈ1ЃЉаДГіAЕФЛЏбЇЪН ЃЌ CЕФЕчзгЪН ЁЃ
ЃЈ2ЃЉгЩXЁЂYЁЂZШ§жждЊЫиАДдзгИіЪ§БШЮЊ4:1:1аЮГЩЕФЛЏКЯЮяЕФНсЙЙМђЪНЮЊ ЁЃ
ЃЈ3ЃЉаДГіЗДгІЂкЕФЛЏбЇЗНГЬЪНЃЈгаЛњЮягУНсЙЙМђЪНБэЪОЃЉ ЃЌ
гЩXЁЂYСНдЊЫиаЮГЩЕФЗжзгСПЮЊ72ЕФЛЏКЯЮяЕФЭЌЗжвьЙЙЬхЙВга жжЃЌЦфжадкЙтееЯТгыCl2ЗДгІЦфвЛТШШЁДњЮяга4жжЕФЛЏКЯЮяЕФУћГЦЮЊ ЁЃ
ЃЈ4ЃЉвбжЊFШмгкЯЁЯѕЫсЃЌШмвКБфГЩРЖЩЋЃЌВЂЗХГіЮоЩЋЦјЬхЁЃЧыаДГіИУЗДгІЕФЛЏбЇЗНГЬЪН ЁЃ
ЃЈ5ЃЉбаОПБэУїЃКЦјЬхDдквЛЖЈЬѕМўЯТПЩБЛЛЙдЮЊОЇгЈЭИУїЕФОЇЬхNЃЌЦфНсЙЙжадзгЕФХХСаЮЊе§ЫФУцЬхЃЌЧыаДГіNМАЦф2жжЭЌЫивьаЮЬхЕФУћГЦ ЁЂ ЁЂ ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК2012НьЙуЮїЮфУљИпжаИпЖўЩЯбЇЦкЦкФЉПМЪдРэзлЛЏбЇВПЗж ЬтаЭЃКЬюПеЬт
ИїЮяжЪжЎМфЕФзЊЛЛЙиЯЕШчЯТЭМЃЌВПЗжЩњГЩЮяЪЁТдЁЃCЁЂDЪЧгЩXЁЂYЁЂZжаСНжждЊЫизщГЩЕФЛЏКЯЮяЃЌXЁЂYЁЂZЕФдзгађЪ§вРДЮдіДѓЃЌдкжмЦкБэжаXЕФдзгАыОЖзюаЁЃЌYЁЂZдзгзюЭтВуЕчзгЪ§жЎКЭЮЊ10ЁЃDЮЊЮоЩЋЗЧПЩШМадЦјЬхЃЌGЮЊЛЦТЬЩЋЕЅжЪЦјЬхЃЌJЁЂMЮЊН№ЪєЃЌlгаЦЏАззїгУЃЌЗДгІЂйГЃгУгкжЦзїгЁЫЂЕчТЗАхЁЃ

 ЧыЛиД№ЯТСаЮЪЬтЃК
ЧыЛиД№ЯТСаЮЪЬтЃК
ЃЈ1ЃЉаДГіAЕФЛЏбЇЪН ЃЌ CЕФЕчзгЪН ЁЃ
 ЃЈ2ЃЉгЩXЁЂYЁЂZШ§жждЊЫиАДдзгИіЪ§БШЮЊ4:1:1аЮГЩЕФЛЏКЯЮяЕФНсЙЙМђЪНЮЊ
ЁЃ
ЃЈ2ЃЉгЩXЁЂYЁЂZШ§жждЊЫиАДдзгИіЪ§БШЮЊ4:1:1аЮГЩЕФЛЏКЯЮяЕФНсЙЙМђЪНЮЊ
ЁЃ
ЃЈ3ЃЉаДГіЗДгІЂкЕФЛЏбЇЗНГЬЪНЃЈгаЛњЮягУНсЙЙМђЪНБэЪОЃЉ ЃЌ
гЩXЁЂYСНдЊЫиаЮГЩЕФЗжзгСПЮЊ72ЕФЛЏКЯЮяЕФЭЌЗжвьЙЙЬхЙВга жжЃЌЦфжадкЙтееЯТгыCl2ЗДгІЦфвЛТШШЁДњЮяга4жжЕФЛЏКЯЮяЕФУћГЦЮЊ ЁЃ
 ЃЈ4ЃЉвбжЊFШмгкЯЁЯѕЫсЃЌШмвКБфГЩРЖЩЋЃЌВЂЗХГіЮоЩЋЦјЬхЁЃЧыаДГіИУЗДгІЕФЛЏбЇЗНГЬЪН
ЁЃ
ЃЈ4ЃЉвбжЊFШмгкЯЁЯѕЫсЃЌШмвКБфГЩРЖЩЋЃЌВЂЗХГіЮоЩЋЦјЬхЁЃЧыаДГіИУЗДгІЕФЛЏбЇЗНГЬЪН
ЁЃ
ЃЈ5ЃЉбаОПБэУїЃКЦјЬхDдквЛЖЈЬѕМўЯТПЩБЛЛЙдЮЊОЇгЈЭИУїЕФОЇЬхNЃЌЦфНсЙЙжадзгЕФХХСаЮЊе§ЫФУцЬхЃЌЧыаДГіNМАЦф2жжЭЌЫивьаЮЬхЕФУћГЦ ЁЂ ЁЂ ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃКАВЛеЪЁЭСъЯивЛжа09-10бЇФъИпЖўЦкжаПМЪдЪдОэ ЬтаЭЃКЬюПеЬт
[10Зж]ГЌвєЫйЗЩЛњдкЦНСїВуЗЩааЪБЃЌЮВЦјжаЕФNOЛсЦЦЛЕГєбѕВуЁЃПЦбЇМве§дкбаОПРћгУДпЛЏММЪѕНЋЮВЦјжаЕФNOКЭCOзЊБфГЩCO2КЭN2ЃЌЦфЗДгІЮЊЃК2NOЃЋ2CO 2CO2ЃЋN2ЁЃ
2CO2ЃЋN2ЁЃ
ЮЊСЫВтЖЈдкФГжжДпЛЏМСзїгУЯТЕФЗДгІЫйТЪЃЌдкФГЮТЖШЯТгУЦјЬхДЋИаЦїВтЕУВЛЭЌЪБМфЕФNOКЭCOХЈЖШШчБэЃК
|
ЪБМф(s) |
0 |
1 |
2 |
3 |
4 |
5 |
|
c(NO)(mol/L) |
1.00ЁС10Ѓ3 |
4.50ЁС10Ѓ4 |
2.50ЁС10Ѓ4 |
1.50ЁС10Ѓ4 |
1.00ЁС10Ѓ4 |
1.00ЁС10Ѓ4 |
|
c(CO)(mol/L) |
3.60ЁС10Ѓ3 |
3.05ЁС10Ѓ3 |
2.85ЁС10Ѓ3 |
2.75ЁС10Ѓ3 |
2.70ЁС10Ѓ3 |
2.70ЁС10Ѓ3 |
ЧыЛиД№ЯТСаЮЪЬтЃЈОљВЛПМТЧЮТЖШБфЛЏЖдДпЛЏМСДпЛЏаЇТЪЕФгАЯьЃЉЃК
ЃЈ1ЃЉдкЩЯЪіЬѕМўЯТЗДгІФмЙЛздЗЂНјааЃЌдђЗДгІЕФЁїH 0ЃЈЬюаДЁАЃОЁБЁЂЁАЃМЁБЁЂЁАЃНЁБЃЉЁЃ
ЃЈ2ЃЉЧА2sФкЕФЦНОљЗДгІЫйТЪv(N2)ЃН ЁЃ
ЃЈ3ЃЉМйЩшдкУмБеШнЦїжаЗЂЩњЩЯЪіЗДгІЃЌДяЕНЦНКтЪБЯТСаДыЪЉФмЬсИпNOзЊЛЏТЪЕФЪЧ ЁЃ
AЃЎбЁгУИќгааЇЕФДпЛЏМС BЃЎЩ§ИпЗДгІЬхЯЕЕФЮТЖШ
CЃЎНЕЕЭЗДгІЬхЯЕЕФЮТЖШ DЃЎЫѕаЁШнЦїЕФЬхЛ§
ЃЈ4ЃЉбаОПБэУїЃКдкЪЙгУЕШжЪСПДпЛЏМСЪБЃЌдіДѓДпЛЏМСБШБэУцЛ§ПЩЬсИпЛЏбЇЗДгІЫйТЪЁЃЮЊСЫЗжБ№бщжЄЮТЖШЁЂДпЛЏМСБШБэУцЛ§ЖдЛЏбЇЗДгІЫйТЪЕФгАЯьЙцТЩЃЌФГЭЌбЇЩшМЦСЫШ§зщЪЕбщЃЌВПЗжЪЕбщЬѕМўвбОЬюдкЯТУцЪЕбщЩшМЦБэжаЃЌЧыдкЩЯБэПеИёжаЬюШыЪЃгрЕФЪЕбщЬѕМўЪ§ОнЁЃ
|
ЪЕбщ БрКХ |
T(Ёц) |
NOГѕЪМХЈЖШ (mol/L) |
COГѕЪМХЈЖШ (mol/L) |
ДпЛЏМСЕФБШБэУцЛ§(m2/g) |
|
Ђё |
280 |
1.20ЁС10Ѓ3 |
5.80ЁС10Ѓ3 |
82 |
|
Ђђ |
|
|
|
124 |
|
Ђѓ |
350 |
|
|
124 |
ВщПДД№АИКЭНтЮі>>
АйЖШжТаХ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com