
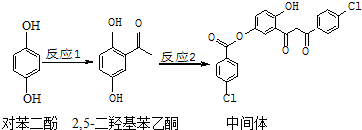
| A. | 对苯二酚在空气中能稳定存在 | |
| B. | 1mol该中间体最多可与11 molH2反应 | |
| C. | 2,5-二羟基苯乙酮能发生加成、取代、缩聚反应 | |
| D. | 该中间体分子中含有1个手性碳原子 |
分析 A.酚羟基不稳定,易被氧化;
B.中间体中苯环、羰基能和氢气在一定条件下发生加成反应;
C.2,5-二羟基苯乙酮含有酚羟基、醛基、苯环,具有酚、醛和苯的性质;
D.连接四个不同原子或原子团的C原子为手性碳原子.
解答 解:A.酚羟基不稳定,易被氧气氧化,所以对苯二酚在空气中不能稳定存在,故A错误;
B.中间体中苯环、羰基能和氢气在一定条件下发生加成反应,所以1mol该中间体最多可与11 molH2反应,故B正确;
C.2,5-二羟基苯乙酮含有酚羟基、醛基、苯环,具有酚、醛和苯的性质,所以2,5-二羟基苯乙酮能发生加成、取代、缩聚反应,故C正确;
D.连接四个不同原子或原子团的C原子为手性碳原子,根据结构简式知,该分子中不含手性碳原子,故D错误;
故选BC.
点评 本题考查有机物结构和性质,为高频考点,明确官能团及其性质关系是解本题关键,侧重考查酚、醛的性质,注意酚能和醛发生缩聚反应,题目难度不大.


 天天练口算系列答案
天天练口算系列答案科目:高中化学 来源: 题型:选择题
| A. | 离子晶体中,只存在离子键,不可能存在其它化学键 | |
| B. | 氧族元素(O、S、Se、Te)的氢化物的沸点依次升高 | |
| C. | NaHSO4、Na2O2晶体中的阴阳离子个数比均为1:1 | |
| D. | 晶体的硬度:金刚石>碳化硅>石英 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1mol NH4Cl | B. | 0.1 mol N2 | ||
| C. | 1.204×1022个CO(NH2)2 | D. | 0.2mol NH3•H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 反应N2(g)+3H2(g)═2NH3(g),其他条件不变时充入N2,正反应速率增大,逆反应速率减小 | |
| B. | 常温下,2NO(g)+O2(g)═2NO2(g)能够自发进行,则该反应的△H<0 | |
| C. | 向0.1mol/L CH3COOH溶液中加入少量的冰醋酸,溶液中$\frac{c(C{H}_{3}CO{O}^{-})}{c(O{H}^{-})}$的值变小 | |
| D. | 电解法精炼铜时,以粗铜作阴极,纯铜作阳极 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 光纤通信使用的光缆主要成分是Si,太阳能电池使用的材料主要是SiO2 | |
| B. | 点燃爆竹后,硫燃烧生产SO3 | |
| C. | 海水中含有溴元素,只进行物理变化就可以得到溴单质 | |
| D. | “地沟油”禁止使用,但可以用来制取肥皂 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 A、B、C三种强电解质,它们在水中电离出的离子如下表所示:
A、B、C三种强电解质,它们在水中电离出的离子如下表所示:| 阳离子 | Na+、K+、Cu2+ |
| 阴离子 | SO42-、OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com